Комплексные соединения.
Общая и неорганическая химия

Единственным распространенным центральным ионом с конфигурацией d1 является Со2*. Он образует довольно много комплексов преимущественно октаэдрического и тетраэдрического строения, хотя общее их число во много раз меньше, чем число комплексов Со (III). Возможность конкуренции между тетраэдрическими и октаэдрическими структурами объясняется малой разностью в энергиях стабилизации полем лигандов… Читать ещё >
Комплексные соединения. Общая и неорганическая химия (реферат, курсовая, диплом, контрольная)
Переходные элементы первого ряда образуют множество комплексных соединений с лигандами различных типов (чистыми а-донорами, аи тг-донорами, о-донорами и тг-акцепторами). Знакомясь в предыдущем разделе с акваи гидроксокомплексами, мы практически уже столкнулись с химией комплексных соединений переходных металлов первого ряда, однако не пытались рассматривать ее с точки зрения электронного строения центральных ионов. Нам известно (гл. 30), что возможность комплексообразования с лигандами того или иного типа, устойчивость и реакционная способность комплексов, их физические свойства сложным образом зависят от природы и состояния окисления металла, однако среди многих характеристик центрального иона число его {/-электронов ({/" -электронная конфигурация) оказывается одной из важнейших, причем соответствующие зависимости можно довольно легко проследить. Поэтому в данном разделе мы кратко рассмотрим свойства комплексных соединений переходных элементов первого ряда в различных состояниях окисления в зависимости от числа {/-электронов. При этом будем руководствоваться следующими простыми соображениями:
- 1. Центральный ион комплексного соединения (атом переходного элемента в соответствующем состоянии окисления) стремится иметь определенный эффективный заряд или определенную суммарную электронную плотность, определяемую зарядом его ядра, размером электронного остова, числом и типом валентных электронов.
- 2. Традиционное понятие степени окисления или состояния окисления металла сложилось применительно к координационным соединениям с лигандами наиболее распространенного типа — о-донорами.
- 3. Окислительно-восстановительные свойства аквакатионов могут служить показателем того, насколько то или иное состояние окисления данного элемента следует считать для него характерным, отвечающим оптимальному эффективному заряду. Например, Сг3 Mn2*, Fe3*, Со2*, Ni2* не проявляют сильных окислительных или восстановительных свойств в кислых средах. Соответственно, эти же ионы образуют устойчивые по отношению к окислению и восстановлению комплексы с большинством лигандов преимущественно а-донорного типа, например [СгО*]3' или [Co (NH3)6]2*.
- 4. Низкие состояния окисления центральных атомов стабилизируются лигандами л-акцепторного типа: СО, RCN, N2, NO, Dipy, Phen, PR3 и другими, например V (CO)6, Cr (CO)6, Mn (CO)5CI, Со (НХ^ХРРЬ3)з.
Стабилизация осуществляется за счет перемещения на лиганды избыточной электронной плотности с центрального атома, который при этом получает некоторый положительный эффективный заряд, стремящийся к оптимальному. Так, в приведенных примерах комплексов V (-1), Сг (0), Мп (+1) и Со (+1) на атомах переходного металла, судя по данным ряда спектральных методов и расчетов МО ЛКАО, сосредоточен небольшой положительный заряд.
- 5. Высокие состояния окисления переходного элемента стабилизируются лигандами тг-донорного типа, в первую очередь О2-, например МпОд, CrOj" .
- 6. Энергия стабилизации полем лигандов может дополнительно стабилизировать комплексы с определенными электронными конфигурациями, причем эта дополнительная стабилизация может быть связана как с повышенной термодинамической устойчивостью, так и с повышенной инертностью (посмотрите об этом в разд. 30.5 и 30.7). Например, особо многочисленны комплексы Сг (Ш) с конфигурацией d3 и Fe (II) и Со (III) с конфигурацией d6.
В табл. 31.6 показаны важнейшие степени окисления переходных элементов первого ряда, проявляемые ими в комплексных соединениях.
Рассмотрим последовательно в порядке увеличения числа d-электронов центрального атома наиболее характерные комплексы, образуемые переходными элементами первого ряда.
Конфигурацию d° имеют элементы от скандия до марганца в высших состояниях окисления, которым отвечают жесткие высокозарядные ионы малого размера. Комплексные соединения для них мало ха рак терны. Кроме рассмотренных в предыдущем разделе аква-, гидроксои оксосоединений можно назвать октаэдрические фторидные комплексы ScF*~, TiFj~, VF^, довольно устойчивые к гидролизу и не проявляющие сильных.
Таблица 31.6 Основные степени окисления переходных элементов первою ряда в комплексных соединениях.
<�г | Sc. | Ti. | V. | Cr. | Mn. | Fe. | Co. | Ni. | Cu. | Zn. |
d° | ||||||||||
d1 | ||||||||||
d2 | ||||||||||
d1 | ||||||||||
d4 | ||||||||||
db | ||||||||||
db | ||||||||||
d1 | ||||||||||
d". | ||||||||||
(P | ||||||||||
d10 |
Примечание. Жирным шрифтом выделены степени окисления, устойчивые и водны) растворах окислительных свойств. Оксоанионы ванадия, хрома и марганца, как отмечено выше, имеют тетраэдрическое строение.
Комплексы с конфигурацией центрального иона dl (Ti3*, V4*, Сг5*, Мп6*) в основном содержат в качестве лигандов кислород и фтор, а также другие галогены. Большинство соединений имеет октаэдрическое строение, они окрашены (поглощение света в видимой области отвечает электронному переходу tg —? eg).
Титан (III) образует много соединений, лучше других изучены галогенидные комплексные ионы TiFj", [TiCl$(H20)]2-, а также аддукты TiCl3 с одной, двумя или тремя донорными молекулами, например TiCl3 ‘ 2N (CH3)3.
Ванадий (IV) — это наиболее распространенное состояние окисления ванадия. Для него характерны комплексы ванадилаоксованадия V02*, например [VO (Dipy)2Cl]* или [V0(C204)2] 2".
Для Cr (V) известно лишь несколько комплексных анионов, присутствующих в твердых солях, например CrOj", CrOCls" и CrOFJ, которые разлагаются при взаимодействии с водой (гидролизуются и диспропорционируют).
Mn (VI) известен лишь в виде иона Мп04" (см. разд. 31.7).
Конфигурация d2 интересна тем, что в изоэлектронном ряду Ti (II), V (III), Cr (IV), Mn (V), Fe (VI) наблюдается переход от сильных восстановителей типа [Ti (H20)6]2*, восстанавливающего воду, к сильным окислителям типа Fe04", ее окисляющих. Поэтому для крайних членов ряда — Ti (II), с одной стороны, и Mn (V) и Fe (VI) с другой — известно очень мало комплексов, для марганца и железа — это лишь тетраоксоанионы Мп04~ и Fe04". Соединения Cr (lV) также неустойчивы в водных растворах, но могут быть получены в твердом состоянии или неводных средах. Например, в растворе в BrF3 идут реакции: 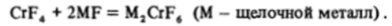
Для ванадия степень окисления (III) характерна, поэтому для V (III) известно много комплексов, в основном это — октаэдрические анионы VXj" (X = F', CN", NCS", V2C20r и т. д.), получаемые из V3* (водн) в присутствии избытка Х', а также катионы [V (H20)6]3* и [V (NH3)6]3*. Большой по размеру ион СГ дает тетраэдрический анион VCU, несмотря на некоторый проигрыш в энергии стабилизации полем лигандов: для октаэдра при конфигурации tg она составила бы 4/5 Д0кт'а Д*1* тетраэдра при конфигурации е2 —6/$Дтстр или приблизительно */5 *4/9 533 V2 Докт (см разд. 30.4).
Конфигурацией d3 обладают ионы V24,, Сг3* и Мп4*, сильно различающиеся своими окислительно-восстановительными свойствами. Ион У2*(водн) восстанавливает воду, он практически не дает комплексов с галогенидными лигандами, но образует устойчивую соль.
V (CN)6] • ЗН20. Марганец (IV), напротив, характеризуется очень сильными окислительными свойствами, для него устойчивы, и то лишь в твердом состоянии, комплексы с лигандами, такими как СГ и F", обладающими л-донорными свойствами.
Наиболее многочисленны среди-комплексов соединения Сг (Ш). Это объясняется двумя причинами: во-первых, степень окисления +3 наиболее характерна для хрома — окисление и восстановление Сг3* (водн) термодинамически затруднено (см. Приложение I), во-вторых, конфигурация d3 способствует высокой инертности этих комплексов (см. разд. 30.7).
Достаточно хорошо изучены октаэдрические комплексы Cr (III) с нейтральными (Н, 0, NH, NR, и др.) и ацидолигандами (F СГ, NCS', CN', С, 04*СН, СОО' и др.). Сами комплексы могут быть нейтральными, катионными или анионными.
Примером интересного нейтрального комплекса может служить ацетилацетонат хрома (III), который можно рассматривать как производное аиетилацетона в енольной форме: СН, -СО-СН=С (ОН) -СН,; анион 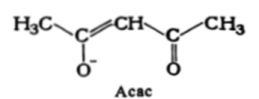
представляет собой бидентатный лиганд, координирующийся к центральному иону через два атома кислорода. Нейтральный комплекс Сг (Асас), принадлежит к так называемым внутрикомплексным соединениям, в которых полидентатные хелатообразующие лиганды насыщают внутреннюю координационную сферу и нейтрализуют заряд центрального иона. Термодинамически устойчивый и кинетически инертный красно-фиолетовый комплекс Сг (Асас), представляет собой довольно летучее твердое вещество с молекулярной кристаллической решеткой. Подобные летучие комплексы могут быть использованы для разделения и очистки переходных металлов.
Многообразие соединений хрома (Ш) связано также с наличием изомеров у разнолигандных комплексов, которые можно разделять и выделять в индивидуальном состоянии благодаря их инертности, и полиядерных комплексов. Полиядерныс соединения, например (Сг2С19)3' или [Сг30(СН3С00)6(Н20)3].
/^1 Сг^ /Сг содержат фрагменты с мостиковыми лигандами (Сг /Сг и О),.
CI.
Сг, но прямые связи Сг-Сг в них отсутствуют, для этого слишком мал размер ионов Сг (Ш).
Многие соединения Сг (Ш) находят широкое практическое применение. Хорошо растворимые в воде хромокалисвые квасцы K, S04 • Cr,(S04), • 24Н, 0 применяют при крашении тканей и дублении кож. В этих процессах роль Сг (Ш) связана с его способностью образовывать комплексы с молекулами белка.
Из комплексообразователей с электронной конфигурацией d4 заслуживают внимания Сг (Н) и Мп (Ш). Аквакатион [Сг (Н20)6]2* и другие одноядерные комплексы Сг (Н) обладают сильными восстановительными свойствами. Хром (II) образует также много диамагнитных солей карбоновых кислот, представляющих собой димеры с коротким расстоянием Сг-Сг, в которых между атомами хрома существует мощная кратная связь (четверная — за счет Спаривания всех четырех-электронов каждого атома), стабилизирующая соединение в целом. Так, димерный ацетат хрома (II) легко осаждается при добавлении раствора, содержащего Сг2* (водн), к насыщенному раствору ацетата натрия и в отличие от мономерных соединений вполне устойчив на воздухе.
Устойчивых комплексов Mn (III) известно не очень много, так как он склонен к диспропорционированию. Комплексы с лигандами слабого поля могут быть стабилизированы за счет хелатного эффекта, например Мп (Асас)з или Кз[Мп (С204)э]-ЗН20, имеющие по четыре неспаренных электрона. Магнитный момент гексацианоманганата (Ш) [Mn (CN)6]3" отвечает двум неспаренным электронам, т. е. случаю сильного поля, при котором энергия стабилизации полем лигандов составляет 8/$ АоктКомплекс устойчив, легко получается при окислении воздухом гексацианоманганата (II) [Mn (CN)6]4".
Центральные ионы с конфигурацией ds четко подразделяются на три категории: сильные восстановители — V (0) и Сг (1); ионы, не обладающие выраженными окислительными или восстановительными свойствами, — Мп (Н) и Fe (III) и сильные окислители — Со (IV). Для первой категории известны единичные комплексы с я-акцепторными лигандами, например V (Dipy)3, V (CO)6, Cr (Dipy)JСо (IV) стабилизирован лишь в нескольких твердых соединениях, в частности C^CoF* и Ва2Со04. Наибольший интерес представляют многочисленные комплексы Мп (Н) и особенно Fe (III).
Большинство комплексов Мп (И) — высокоспиновые, имеющие суммарный спин */а и нулевую энергию стабилизации полем лигандов. Константы устойчивости большинства ацидокомплексов малы, поэтому из их растворов выделяются кристаллогидраты, содержащие акваион (Мп (НаО)4) **, например MnS04 • 7НаО. Розовый сульфат марганца (II) служит удобным исходным препаратом для получения других его соединений, сам он применяется при окраске тканей.
К немногочисленным низкоспиновым комплексам марганца (II) принадлежат его соединения с лигандами сильного поля, например K4[Mn (CN)4J• ЗНаО. Гексацианоманганаты в твердом виде и в растворе постепенно окисляются воздухом.
Железо (Щ) образует большое число комплексов. Среди них более устойчивы ацидокомплексы с лигандами, координированными через кислород, например [ Ре (С204)э]3".
Под действием света в растворе триоксалатоферрата (Ш) идет окислительно* восстановительный процесс:
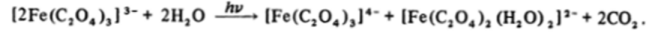
Эта реакция используется для измерения интенсивности света в приборах, называемых ферриоксалатными актинометрами.
С галогенидными анионами железо (III) образует в растворах лабильные и относительно непрочные катионные^ нейтральные и анионные октаэдрические комплексы состава IFeX6.n(H, 0)nl", при большом избытке ионов СГ в концентрированной соляной кислоте образуется тетраэдрический ион (FeCl4Г.
К числу давно известных комплексных соединений железа относятся гексацианоферраты (III) и (II) — анионы IFe (CN)J*‘ и (Fe (CN)#|4* и их красная и желтая кровяные соли K,|Fe (CN)Jw K4|Fe (CN)J.
Низкоспиновые октаэдрические комплексы с электронной конфигурацией d* (/62j) обладают максимальной энергией стабилизации noneN лигандов, равной 12/sAkt" и отличаются повышенной инертностью, поэтому они исключительно многочисленны. В ряду Сг (0), Mn (I), Fe (II), Со (Ш) наибольшее значение как комплексообразователи имеют два последних иона.
Среди комплексов железа (11) особо интересен гемоглобин — комплекс с белком крови, благодаря которому происходит усваивание и перенос молекулярного кислорода кровью животных и человека. Ключом сложного процесса обратимого взаимодействия гемоглобина с кислородом является присоединение молекулы кислорода к исходному высокоспиновому комплексу железа, в котором атом железа связан с четырьмя атомами азота в результате чего образуется низкоспиновый октаэдрический комплекс.
Многочисленные комплексы Со (Ш) послужили Вернеру экспериментальным материалом, на основе которого была создана координационная теория и учение об изомерии комплексных соединений. Именно инертность комплексов позволила, в частности, разделить оптические изомеры этилендиаминовых и других производных кобальта (III).
Лиганды, координированные к кобальту через азот за счет акцептирования ионом кобальта неподеленных электронных пар азота, способствуют стабилизации Со (Ш) по отношению к процессам восстановления. Напомним, что [Со (Н20)6]3* легко окисляет воду (^co'VCo1^ 1.81 В), а [ Co (NH3)6]3*, как и большинство аминокомплексов, не обладает окислительными свойствами. Потенциал пары Co (NH3)J*/Co (NH3)|* составляет лишь 0,11 В, а пары гексацианокомплексов Co (CN)J'/Co (CN)J" еще ниже, он равен -0,83 В.
С биологической точки зрения важен сложный комплекс Со (Ш) — витамин В12* в котором центральный ион с конфигурацией (? находится в окружении пяти координированных к нему атомов азота, а шестое координационное место занято группой СН3, CN или другими.
Единственным распространенным центральным ионом с конфигурацией d1 является Со2*. Он образует довольно много комплексов преимущественно октаэдрического и тетраэдрического строения, хотя общее их число во много раз меньше, чем число комплексов Со (III). Возможность конкуренции между тетраэдрическими и октаэдрическими структурами объясняется малой разностью в энергиях стабилизации полем лигандов для случая слабого поля (см. разд. 30.5). Например, бледно-розовый хлорид СоС12 при растворении образует розовые аквакатионы [Со (Н20)6]2*, а при добавлении хлоридов к этому раствору он приобретает синий цвет за счет тетраэдрических тетрахлорокобальтовых анионов 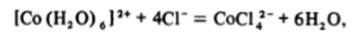
которые можно снова перевести в аквакатионы при добавлении к раствору солей цинка или ртути, дающих более прочные хлоридные комплексы:
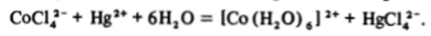
Следствием стабилизации Со (Ш) азотсодержащими лигандами и низких значений потенциалов восстановления таких комплексов до соединений Со (II) является склонность последних к окислению, в частности молекулярным кислородом.
На первой стадии молекула кислорода координируется к иону кобальта (II) и происходит внутримолекулярный перенос электронов с образованием промежуточного перо к си дно го комплекса Co (IV).
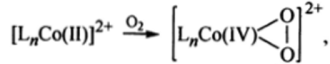
который далее взаимодействует с еще одним комплексом Со (И), образуя биядерный пероксокомплекс Со (Ш).
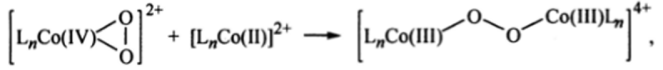
в свою очередь способный терять кислород и восстанавливаться. Подобные процессы лежат в основе каталитического действия комплексов кобальта в реакциях окисления молекулярным кислородом, например при промышленном окислении толуола до фенола.
Среди ионов с конфигурацией d*, перечисленных в табл. 31.6, вновь наблюдается деление на восстановители — Fe (0), Со (1), стабилизируемые тг-акцепторами, окислитель — Cu (III), стабилизируемый кислородом и фтором, и Ni (II), имеющий характерные для никеля состояния окисления и дающий многочисленные комплексы с разнообразными лигандами, которые и представляют для нас наибольший интерес. Особенность центральных ионов с конфигурацией d8 заключается в их склонности к образованию плоских квадратных комплексов с лигандами сильного поля (разд. 30.5), поэтому комплексы никеля (П) могут иметь разные координационные числа и разное строение.
Октаэдрические комплексы никель образует преимущественно с лигандами слабого поля, например |Ni (HaO)e)2 INi (NH>)#|**, NiEn/ Они имеют электронную конфигурацию tgCg с двумя несларенными электронами. Такие соединения термодинамически не очень устойчивы и лабильны, что в значительной степени объясняется малым радиусом иона Nia* и сильным отталкиванием между шестью лигандами.
Примером квадратного комплекса с лигандами сильного поля может служить желтый INi (CN)4|*‘, который образуется при добавлении к растворам солей NKII) некоторого избытка цианид-ионов.
В тех случаях, когда лиганды имеют большой объем и образуют слабое поле, возникает сильное мсжлиганднос отталкивание, которое препятствует образованию не только октаэдрического, но и квадратного комплекса. Поскольку при одинаковых длинах связей металл-лиганд расстояния между лигандами в тетраэдре больше, чем в октаэдре и квадрате, эти условия способствуют образованию тетраэдрических комплексов. Такие комплексы никель (II) образует, в частности, с галогенидами, фосфинами, арсинами, например NiClJ", NiClj (PPh3),.
Из комплексов с конфигурацией центрального иона (Р наибольший интерес представляют соединения меди (Н). В стереохимическом отношении комплексы меди (11)" так же как соединения Ni (Il), достаточно разнообразны. Октаэдрические комплексы образуются лишь с компактными незаряженными лигандами, например [Си (Н20)6]2*, [Си (Н20)6_я (NH3)n]2* (п = 1 -4). Ион [Cu (NH3)6]2* удается получить только в жидком аммиаке.
Наличие девяти с/-элсктронов способствует стабилизации квадратных комплексов с лигандами сильного поля в меньшей степени, чем конфигурация d*, так как дополнительная энергия стабилизации в случае d9 вдвое меньше. Квадратное окружение Cu (II) возникает как предельный случай тетрагонального искажения октаэдра, его возникновению способствует наличие объемистых лигандов, например, в комплексе [Си (Ру)4 |а* или в кристаллах (NH4), CuC14. Группировка СиГanj- может иметь также и структуру искаженного тетраэдра в кристаллах солей с большими катионами, например Cs2Curan4 (Гал = С1, Вг).
Медь (II) образует довольно много комплексов с координационным числом пять. В самых общих чертах это можно объяснить тем, что неподеленная пара е^-элсктронов блокирует одну из вершин октаэдра, в результате чего образуется квадратная пирамида. Этот случай реализуется, если ион Cu (II) встраивается в структуру белка, как, например, в ферменте оксидазс аскорбиновой кислоты, который катализирует окисление витамина С. Если же лиганды стерео химически подвижны, то образуется более симметричная структура тригональной бипирамиды, как, например, в комплексах |CuCl} |3" или |CuDipy3l|*.
Наш обзор завершают ионы с электронной конфигурацией d]0. Это прежде всего ионы Си* н Zn2+. Энергия стабилизации полем лигандов в этом случае равна нулю. Прочность таких комплексов поэтому обычно невелика (константы устойчивости галогенидных комплексов цинка лежат в интервале 10−10), а их стереохимия определяется только размерами центрального иона и лигандов и энергией связи между ними. Так, ион Си* часто образует комплексы с координационным числом 2, например [Cu (NH3)2]* и [СиС12]". Ион Zn2* чаще образует тетраэдрические комплексы, например [Zn (CN4)]2~. Октаэдрическое строение имеют аквакомплексы в растворе, например [Zn (H20)6]2* или [ZnCl4(H20)2]2', это — лабильные соединения со слабыми связями металл-лиганд.
Комплексы цинка представляют определенный интерес в практическом отношении благодаря их лабильности, следствием которой может быть высокая реакционная способность. Дитиокарбаматы цинка (производные (Ra NCS, |") применяются как фунгициды в сельском хозяйстве и ускорители вулканизации каучука. Комплексами цинка являются и некоторые ферменты.