Углерод.
Неорганическая химия

Комплексные соединения монооксида углерода с металлами называют карбонилами. Известны карбонилы большинства d-элементов. Как правило, в координационной сфере содержится столько молекул СО, чтобы электронная оболочка металла достраивалась до конфигурации благородного газа, находящегося в конце того периода, к которому принадлежит металл. При этом молекула СО служит донором электронной пары, металл… Читать ещё >
Углерод. Неорганическая химия (реферат, курсовая, диплом, контрольная)
Элементное состояние.
Известно несколько аллотропных модификаций углерода.
Карбин — кристаллическая модификация углерода с цепочечным строением молекул. Цепи состоят из атомов углерода с ^^-гибридизацией электронных орбиталей. Различают а-карбин или полиин, в цепях которого чередуются тройные и одинарные связи: — С=С—С=С—С=, и p-карбин или поликумулен, в цепях которого атомы углерода соединены двойными связями: =С=С=С=С=С=. Карбин встречается в природе в виде минерала чаоита и получается искусственно.
Графит — темно-серое или черное, мягкое, жирное на ощупь кристаллическое вещество со слабым металлическим блеском. Он теплопроводен и обладает электрической проводимостью. При температуре около 3700 °C и атмосферном давлении графит возгоняется без плавления.
Графит имеет слоистую структуру (рис. 18.1), в которой плоские слои образованы правильными шестиугольниками из атомов углерода с $р2-ги6ридизацией электронных орбиталей атомов углерода. Одинарные связи, образующиеся в результате перекрывания гибридных орбиталей, дополняются делокализованными по всему слою л-связями, поэтому кратность каждой из связей С—С равна 1,33, энергия связи составляет 480 кДж/моль. Атомы углерода каждого слоя располагаются против центров шестиугольников соседних слоев (верхнего и нижнего). Слои графита связаны между собой слабыми силами Ван-дер-Ваальса: энергия связи между слоями равна 17 кДж/моль. Вследствие этого графит легко расслаивается на чешуйки.
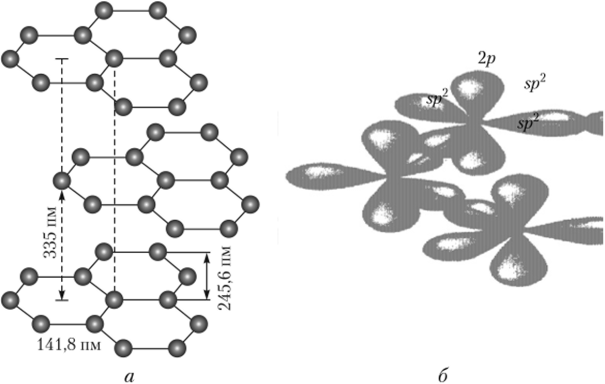
Рис. 18.1. Фрагмент слоистой структуры графита (а) и схема перекрывания электронных облаков (б) шести атомов углерода, образующих правильный шестиугольник Графит — распространенный в природе минерал. В промышленности его получают из кокса или из газообразных углеводородов. При температуре 2700 °C и давлении 11 — 12 ГПа графит превращается в алмаз.
Фуллерены представляют собой кристаллические вещества черного цвета с металлическим блеском, обладающие полупроводниковыми свойствами. По пластичности они близки к графиту. В отличие от других аллотропных модификаций углерода кристаллы фуллеренов состоят нс из атомов, а из молекул. Молекулы обычно имеют шарообразную форму или форму мяча для регби. В них всегда содержится четное число атомов углерода: 60, 70,72 и т. д., объединенных в пятии шестиугольники с общими ребрами (рис. 18.2). Внутри молекулы полые. Электронные орбитали атомов углерода в фуллеренах находятся в состоянии 5р2-гибридизации. Каждый атом, как и в графите, связан с тремя другими, но располагаются они не на плоскости, а на поверхности, близкой к сферической. В фуллеренах все связи между атомами углерода насыщены за счет их взаимодействия друг с другом, в то время как атомы углерода, расположенные на поверхности алмаза, по краям слоев графита и в концах цепей карбина насыщают свои связи, направленные наружу из объема, за счет взаимодействия с атомами других химических элементов, например водорода или кислорода. Первоначально фуллерены были получены испарением графита под действием лазерного импульса в атмосфере благородного газа гелия, позднее их обнаружили в природе, например, в составе минерала шунгита.
Алмаз — бесцветное прозрачное кристаллическое вещество с очень высоким преломлением света. Показатели пре;
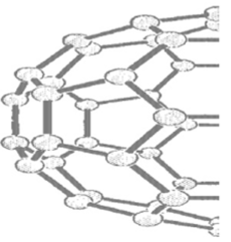
Рис. 18.2. Сферическая молекула фуллерена Cgo.
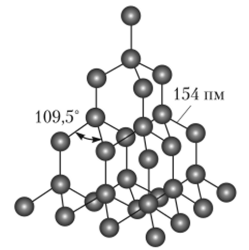
Рис. 18.3. Структура алмаза.
ломления для световых волн различных длин в алмазе сильно различаются, благодаря чему видимый свет разлагается в спектр. Алмаз — самый твердый, но хрупкий минерал.
Структура алмаза, показанная на рис. 18.3, отвечает-гибридизации орбиталей атомов углерода. Каждый атом углерода имеет четыре ст-связи и тетраэдрически окружен четырьмя такими же атомами углерода. Твердость и способность алмаза сильно преломлять свет — следствие его структуры.
При нормальных условиях алмаз термодинамически неустойчив и должен самопроизвольно превращаться в графит, но этого не происходит и он может существовать неопределенно долго из-за очень больших энергий активации реакции.
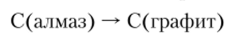
При высокой температуре в вакууме или в инертной атмосфере алмаз без плавления превращается в графит.
Массу алмаза принято измерять в каратах: 1 карат = 0,2 г. Крупные кристаллы алмаза, встречающиеся в природе, достигают 200 каратов. Синтетические алмазы получают в промышленности главным образом из графита.
Лонсдейлит найден в метеоритах и получен искусственно из графита при высоких давлениях и температуре около 900 °C. Он имеет кристаллическую структуру (рис. 18.4), состоящую, как и у алмаза, из атомов углерода с 5р3-гибридизацией электронных орбиталей. Отличие от алмаза заключается в строении кристаллической структуры.
Аморфный углерод (кокс, бурые и каменные угли, сажа, активный уголь) состоит из мельчайших кристаллов, имеющих структуру графита.
Химические свойства. Аллотропные формы углерода существенно различаются по реакционной способности. Об;
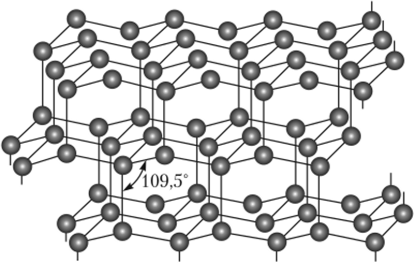
Рис. 18.4. Структура лонсдейлита.
щими химическими свойствами для всех них являются следующие:
- • углерод химически инертен при обычных условиях;
- • при высоких температурах он взаимодействует со многими простыми и сложными веществами, проявляя свойства сильного восстановителя.
Ниже описаны некоторые характерные особенности каждой из аллотропных форм углерода. Окисление озоном в присутствии воды превращает а-карбин в щавелевую кислоту, а p-карбин — в угольную. Алмаз химически очень устойчив. Фтором окисляется только при нагревании, но сразу с полным разрушением его трехмерной структуры и образованием тетрафторида углерода CF4. В присутствии кислорода алмаз сгорает при 870 °C. В отсутствие окислителей он не взаимодействует с кислотами и щелочами. Фуллерены реагируют с щелочными металлами с образованием фуллеридов, например K3CgoФуллерены взаимодействуют также с водородом, галогенами, фосфором. Наибольшей химической активностью обладают аморфные формы углерода, так как у них развитая поверхность, множество дефектов кристаллической структуры и большое число концевых химических связей углерода, насыщенных за счет атомов других элементов, а не углерода. Аморфный углерод воспламеняется на воздухе при температурах 300— 500 °C, при еще более высоких температурах он взаимодействует с парами серы с образованием сероуглерода CS2. При нагревании он образует ковалентные карбиды бора и кремния. В промышленности важны реакции восстановления аморфным углеродом металлов из их оксидов и его реакция с водяным паром:
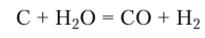
Самой распространенной формой углерода является графит, поэтому его химические свойства рассматриваются более подробно. Графит инертен при нормальных условиях. При 1200 °C начинает взаимодействовать с водородом с образованием метана СН4. При нагревании на воздухе воспламеняется и горит с образованием оксидов СО и С02. С молекулярным азотом графит не реагирует. С атомами азота, образующимися в электрическом разряде, взаимодействует с образованием дициана C2N2. При взаимодействии со смесью N2 и Н2 образуется циановодород I1CN. С большинством металлов графит дает карбиды. Характерной особенностью графита является образование соединений включения, которые возникают при проникновении атомов, ионов или молекул между раздвигающимися неразрушенными углеродными слоями. Соединения включения графит образует с щелочными металлами, галогенами, галогенидами, оксидами и сульфидами металлов. Графит устойчив по отношению к кислотам и растворам солей, реагирует с растворами щелочей.
Бинарные соединения.
Бинарные соединения углерода с sи р-элементами можно разделить на две большие группы (табл. 18.3). В первую группу входят молекулярные газообразные, жидкие или легколетучие соединения с более электроотрицательными, чем сам углерод, элементами. Вторую группу образуют карбиды. Карбиды — это соединения углерода с элементами, электроотрицательность которых меньше, чем электроотрицательность углерода. Начнем рассмотрение с первой группы соединений.
Таблица 183
Бинарные соединения углерода и их значения A298 (кДж/моль).
СН4(г). — 50,8. | ||||||
П2С2(к). — 56,1. | Ве-)С (к). — 88,3. | В4С (к). — 38,3. | С (алмаз) +2,8. | C2N2®. +309,2. | С02(г). — 394,4. | CF4®. — 635,1. |
Na2C2(i<). — 18,5. | MgC2(K). — 84,5. | А14С3(к). — 196,0. | SiC (ic). — 637. | Р2С6(ам). >0. | CS2(a<). +64,4. | ССд4(ж). — 68,6. |
Этиниды. | Мета; ниды. | Алмазо; подобные. | Аморфный. | Ковалентные молекулярные соединения. | ||
Карбиды. | ||||||
Углеводороды. Эти очень многочисленные соединения демонстрируют возможность образования прочных и разнообразных цепочечных линейных, разветвленных, циклических и других полимеров за счет связей С—С, С=С и С=С.
Простейший углеводород — метан (болотный или рудничный газ) СН4, в котором орбитали атома углерода имеют sp-гибридизацию (см. рис. 11.13, а). Его тетраэдрически построенная молекула из-за близости электроотрицательностей углерода (2,55) и водорода (2,2) обладает малополярными ковалентными ст-связями С—Н. Хотя все четыре атома водорода несут небольшие положительные заряды (-0,065 элементарного заряда), их расположение в вершинах тетраэдра приводит к отсутствию у СН4 электрического дипольного момента. Средняя энергия связей С—Н велика и составляет.
415 кДж/моль. Это и делает возможным прямой синтез СН4 из углерода и водорода:
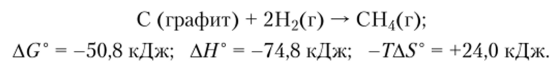
Но AG° этой реакции все же мало отличается от нуля, и при высоких температурах равновесие смещается влево изза того, что энтропия этой реакции — отрицательная величина. При низких же температурах реакция идет медленно.
Метан — газ без цвета, запаха и вкуса, мало растворимый в воде. Его молекулы взаимодействуют друг с другом только за счет слабых дисперсионных сил, и поэтому температуры кипения (-16ГС) и плавления (-184°С) у этого вещества низки.
В лабораториях получение метана осуществляют с помощью реакции декарбоксилирования, протекающей при сплавлении ацетата и гидроксида натрия:
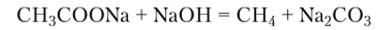
Промышленные источники метана — горючий природный газ, содержащий 80—99% СН4, и попутный нефтяной газ, в котором метана содержится 30—90%.
Метан — исходное сырье для получения многих продуктов. Так, например, получение из метана синтез-газа:
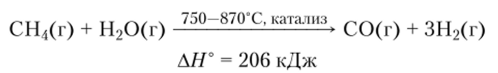
— это первая стадия двух важных технологических процессов: получения метанола СН3ОН и водорода, используемого для производства аммиака.
Метан широко используют в химической промышленности для синтеза этина, циановодорода, хлороформа, сероуглерода и других продуктов: 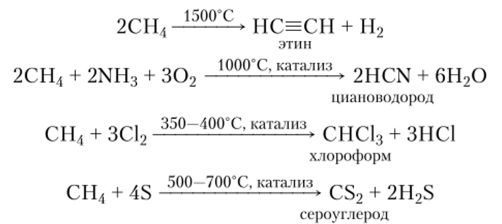
В свою очередь каждый из продуктов приведенных выше реакций служит родоначальником большого числа практически важных веществ.
Метан используют также в качестве бытового и промышленного топлива, так как он горит некоптящим пламенем и выделяет при этом большое количество теплоты:
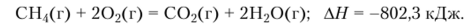
Смеси СЕЦ с воздухом очень взрывоопасны.
Галогениды. Простейшие галогениды углерода — аналогичные метану, но геометрическому строению тетрагалогениды CF4, ССЦ, СВг4 и СЦ. В этом ряду прочность связей углерода с галогеном быстро уменьшается, и термодинамически устойчивы только тетрафторид и тетрахлорид углерода. Так как электроотрицательности галогенов больше, чем у углерода, их атомы несут частичные отрицательные заряды: фтор -0,21, хлор -0,17 элементарного заряда.
Тетрафторид углерода CF4 — бесцветный, химически очень инертный газ с низкими температурами кипения (-128°С) и плавления (-184°С). Его получают фторированием углеродсодержащих соединений и используют в качестве фреона.
Тетрахлорид углерода ССЦ — негорючая бесцветная токсичная жидкость с большой плотностью и сладковатым запахом. Хотя принципиально возможен прямой синтез ССЦ, в промышленности для его получения используют реакцию замещения серы сероуглерода хлором:
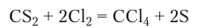
Тетрахлорид углерода должен реагировать с кислородом и водой, но кинетическая инертность этого соединения исключает возможность этих реакций. ССЦ находит широкое применение как хороший растворитель для смол, жиров, лаков.
Смешанные тетрагалогениды тина CF2C12, CF3CI и другие используют в качестве фреонов. Твердые при обычных условиях СВг4 и С14 применяют редко. Большое значение имеют хлори фторпроизводные разнообразных полимерных углеводородов. Эти пластмассы разнообразны и ценны, но свойствам. Их широко используют в бытовых и производственных целях.
Оксиды. Важнейшими из оксидов углерода являются монооксид СО и диоксид С02.
Монооксид углерода [оксид углерода (П) или угарный газ] имеет электронное строение, показанное на рис. 18.5. Моле;
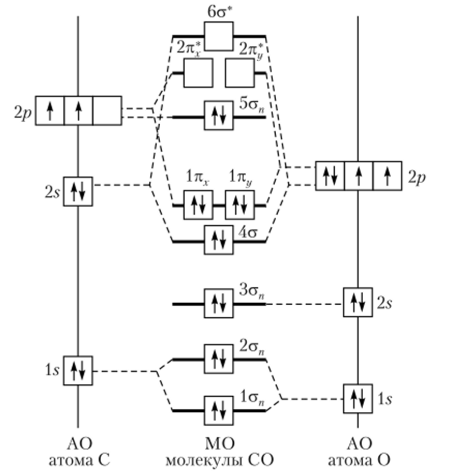
Рис. 185. Схема заполнения молекулярных орбиталей молекулы СО.
кула СО гетеронуклеарная, т. е. образована атомами двух разных химических элементов, поэтому энергетическая диаграмма расположения молекулярных орбиталей для гомоядерных молекул (см. рис. 11.19) к ней неприменима. В этом случае используют также другие обозначения молекулярных орбиталей: но порядку нумеруют отдельно аи отдельно л-орбитали, индексом п обозначают несвязывающие орбитали. При этих условиях запись электронной конфигурации молекулы СО имеет следующий вид:
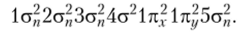
Связывающий характер имеют три орбитали (4а, 1лг и 1 пу), поэтому связь между атомами С и О является тройной и энергия ее очень велика: 1075 кДж/моль. Большое влияние на химические свойства СО оказывает самая высокая по энергии неподеленная электронная пара. Она занимает несвязывающую 5а"-орбиталь, вытянутую в сторону, противоположную атому кислорода, и придает СО свойства С-донорного лиганда.
Отражая эти структурные особенности, молекулу Monos' 5;
оксида углерода можно изобразить так: :С=0:.
Из-за того что электрический дипольный момент СО очень мал, диполь-дипольное взаимодействие молекул СО слабо, а температуры кипения (-192°С) и плавления (-205°С) этого вещества очень низки.
При обычных условиях монооксид углерода — газ без цвета, запаха и вкуса, плохо растворимый в воде. В небольших количествах он присутствует в атмосфере. Его содержание колеблется от 0,01 до 0,9 мг/м3. Природными источниками СО служат вулканы, болота, лесные пожары, фоторазложение морских водорослей. Его выделяют также микроорганизмы, растения и животные. Поступление СО из техногенных источников составляет примерно 5•108 т в год.
В лабораториях СО получают из муравьиной кислоты, воздействуя на нее водоотнимающими средствами:
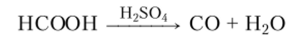
В промышленности СО получают при помощи реакций, которые называют реакциями неполного окисления углерода, потому что в них не достигается максимальная степень окисления этого элемента, равная +4:
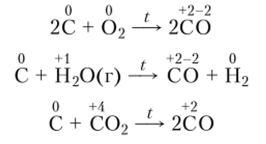
Другим промышленным источником СО служат углеводороды:
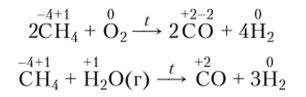
Монооксид углерода — несолеобразующий оксид. Хотя СО образуется при обезвоживании муравьиной кислоты и даст при взаимодействии с щелочами ее соли — формиаты:
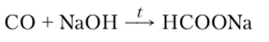
его нельзя считать ангидридом этой кислоты, поскольку природа химической связи в СО и НСООН различна.
Монооксид углерода — сильный восстановитель. При высоких температурах он восстанавливает оксиды металлов, окисляясь до С02. Например, в основе производства чугуна лежат реакции последовательного восстановления оксидов железа:
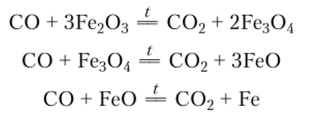
С некоторыми окислителями СО реагирует при небольшом нагревании. Так взаимодействует СО с хлором и серой:
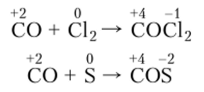
Образующиеся ядовитые дихлорид-оксид углерода (фосген) СОС12 и сульфид-оксид углерода COS служат полупродуктами для получения пестицидов, красителей и других органических соединений.
В присутствии катализаторов СО полностью окисляется до С02:
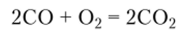
Эту реакцию используют для обезвреживания выхлопных газов автомобилей.
Для монооксида углерода характерны реакции присоединения. При повышенных температурах он взаимодействует с аммиаком, давая различные продукты в зависимости от природы катализатора. Например, в присутствии платины образуется мочевина:
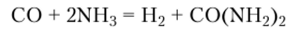
При взаимодействии СО с водородом, изменяя температуру, давление и катализатор, можно получить множество разнообразных продуктов: предельные углеводороды, спирты, альдегиды, кетоны, органические кислоты. Особенно важен процесс получения метанола:
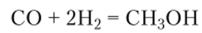
Монооксид углерода проявляет свойства лиганда. Это объясняется наличием несвязывающей электронной пары на 5а"-орбитали и двух вакантных разрыхляющих 2л*- и 2л*-орбиталей. Донорным атомом в молекуле СО служит атом углерода. За счет электронной пары (5а^) от атома углерода между молекулой СО и атомом металла образуется а-связь,.
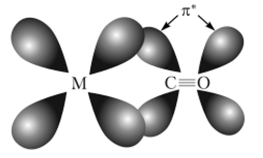
Рис. 18.6. Схема образования тс-связи в результате перекрывания d-орбитали атома металла и разрыхляющей я*-орбитали молекулы СО.
а при перекрывании заполненных электронами d-орбиталей атома металла и вакантных разрыхляющих л-орбиталей СО образуются л-связи (рис. 18.6).
Комплексные соединения монооксида углерода с металлами называют карбонилами. Известны карбонилы большинства d-элементов. Как правило, в координационной сфере содержится столько молекул СО, чтобы электронная оболочка металла достраивалась до конфигурации благородного газа, находящегося в конце того периода, к которому принадлежит металл. При этом молекула СО служит донором электронной пары, металл находится в нулевой степени окисления, и заряд координационной сферы равен нулю. Многие из карбонилов содержат в координационных сферах не только СО, но и другие лиганды. Большинство карбонилов металлов — это легколетучие, легкоплавкие кристаллические вещества. Пентакарбонилжелезо [Ее (СО)5] и тетракарбонилникель [Ni (CO)4] — бесцветные, легко испаряющиеся, очень ядовитые жидкости. Молекула [№(СО)4] имеет форму тетраэдра, [Fe (CO)5] — тригональной бипирамиды.
Карбонилы железа и никеля получают при взаимодействии металлов с СО при повышенных температурах и давлениях:
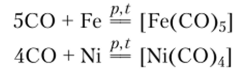
Многие карбонилы используют в промышленности. Некоторые из них служат активными катализаторами. Термическим разложением карбонилов получают особо чистые металлы, металлические порошки для порошковой металлургии.
Монооксид углерода очень ядовит. Его называют угарным газом, потому что он образует с железом гемоглобина крови прочное комплексное соединение и тем самым препятствует переносу кислорода.
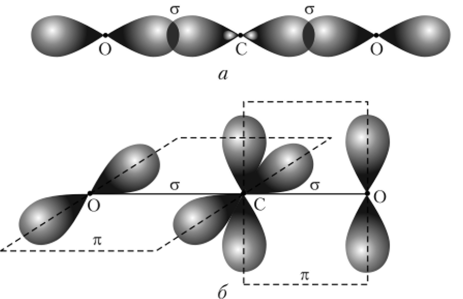
Рис. 18.7. Схема образования химических связей в молекуле С02:
а — образование a-связей; б — образование ти-связей.
Диоксид углерода [оксид углерода (1У) или углекислый газ] СО2 имеет линейные молекулы (рис. 18.7). Такая форма молекул объясняется тем, что в атоме углерода имеются две s/7-гибридные орбитали и две негибридизованные /7-орбитали. Все они перекрываются с /7-орбиталями двух атомов кислорода. При этом две гибридные орбитали дают с /7-орбиталями атомов кислорода две ст-связи, угол между которыми равен 180°. Негибридизованные /7-орбитали углерода дают с /7-орбиталями кислорода две тг-связи, расположенные в перпендикулярных друг другу плоскостях.
При обычных условиях диоксид углерода — бесцветный газ, со слабым кисловатым запахом и вкусом. При 20 °C и давлении 5,7 МПа он сжижается. Испарение жидкого СО2 приводит к охлаждению и образованию твердого диоксида углерода, известного под названием «сухой лед». Кристаллическая решетка С02 показана на рис. 11.25. При -78°С твердый С02 сублимирует (испаряется без плавления).
Электрический дипольный момент линейной молекулы С02 равен нулю, потому что дипольные моменты связей С=0 направлены навстречу друг другу и взаимно компенсируются О—О. Вещества, состоящие из неполярных молекул, как правило, плохо растворяются в полярных растворителях, к числу которых относится вода. Растворимость СО2 в воде подтверждает это правило: в 1 л воды при 20 °C растворяется 0,9 л С02.
Диоксид углерода содержится в атмосфере и гидросфере. Он образуется при окислении органических веществ, выделяется при дыхании животных. Велика также роль техногенных источников С02.
В лаборатории С02 получают, действуя хлороводородной или серной кислотой на карбонаты кальция или натрия:
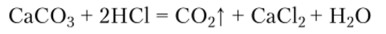
В промышленности С02 получают при сжигании углерода и его соединений:
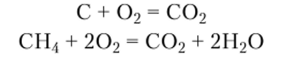
Он образуется также при спиртовом брожении и в качестве побочного продукта при обжиге известняка:
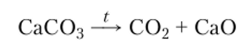
Диоксид углерода — кислотный оксид. Он взаимодействует с основными оксидами и сильными основаниями:
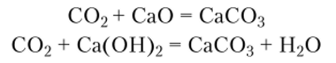
Однако его кислотообразующие свойства выражены слабо. Равновесие.
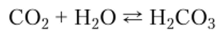
сильно смещено влево. Только одна молекула С02 из шестисот превращается в водных растворах в угольную кислоту. Основная же масса растворенного в воде С02 остается в молекулярном состоянии.
Диоксид углерода — слабый окислитель. Углерод в молекулах С02 проявляет наибольшую степень окисления +4. Вследствие этого диоксид углерода проявляет окислительные свойства, но является слабым окислителем. Он реагирует только с очень сильными восстановителями, например в его атмосфере может гореть магний:
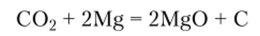
При пропускании С02 над раскаленным углем происходит обратимая реакция комнропорционирования:
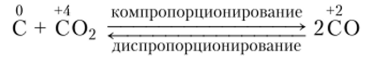
При температурах выше 1000 °C равновесие смещено вправо, а при температурах ниже 400 °C — влево. При обычных условиях диспропорционирование СО не наблюдается из-за чрезвычайно низкой скорости этой реакции.
Сульфид. Дисульфид углерода (сероуглерод) CS2 — бесцветная жидкость с приятным запахом, разлагается под действием света. Молекулы CS2 линейны. Дисульфид углерода легко воспламеняется и горит:
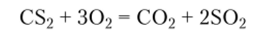
Взаимодействие CS2 с сульфидами щелочных металлов приводит к образованию кристаллических тиокарбонатов, например тиокарбоната калия:
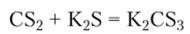
При действии на тиокарбонаты кислот образуется неустойчивая тиоугольная кислота, которая разлагается подобно Н2С03:
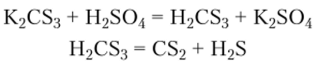
Соединения с азотом. Неорганические соединения, имеющие связи С—N, C=N и C=N, немногочисленны.
Циан (дициан) C2N2 имеет линейную структуру.
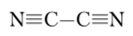
Это бесцветный ядовитый газ с резким запахом, при температуре -21°С превращающийся в бесцветную жидкость. Он термодинамически неустойчив. Его получают термическим разложением цианида серебра:
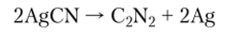
Дициан очень реакционноспособен и по некоторым химическим свойствам напоминает двухатомные галогены. Он легко вступает в реакции с образованием аналогов соединений галогенов:
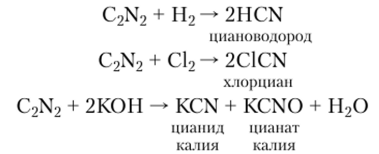
Дициан горит на воздухе:
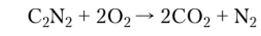
Циановодород HCN — бесцветная жидкость с низкой температурой кипения (26°С) и высокой летучестью, которая смешивается с водой в любых отношениях. В водных растворах HCN — слабая циаповодородная (синильная) кислота.
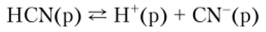
с константой диссоциации 5 • 10 10. Нейтрализация HCN сильными основаниями приводит к получению хорошо растворимых в воде цианидов:
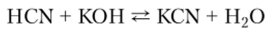
Цианиды аммония, щелочных и щелочноземельных металлов, диссоциирующие в растворах с отщеплением цианид-иона CN-, входят в число сильнейших ядов. Механизм их действия — очень быстрое ингибирование цитохромоксидазы (фермент, переносящий электроны на молекулу 02) и прекращение клеточного дыхания. Водные растворы цианидов щелочных и щелочноземельных металлов имеют сильнощелочную реакцию из-за гидролиза по аниону.
Цианид-ион — очень активный С-донорный лиганд, изоэлектронный молекулам СО и N2. Наличие отрицательного заряда придает его многочисленным комплексным соединениям с катионами-элементов анионный характер, например:
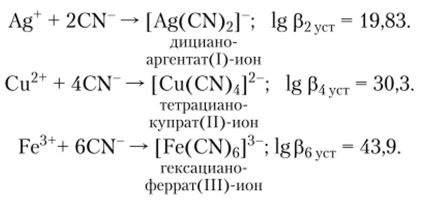
Прочность таких комплексных анионов, как гексацианоферрат (И)-ион [Fe (CN)6|1- и гексацианоферрат (Ш)-ион [Fe (CN)6] J>_, настолько высока, что содержащие их растворы не ядовиты, так как равновесные концентрации цианид-ионов CN- ничтожно малы.
Цианамид кальция CaCN2 — белое кристаллическое вещество, содержит цианамид-ион CN|, который является электронным аналогом диоксида углерода и имеет линейную структуру: ~N=C=N". Цианамид кальция получают при прокаливании карбида кальция в токе азота при 1100°С:
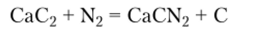
Его используют как азотное удобрение и дефолиант.
Карбиды. Эти соединения делятся на четыре группы (см. табл. 18.3): этиниды (ацетилениды), содержащие анионы.
Cf, метаниды, содержащие анионы С4-, алмазоподобные карбиды бора и кремния и аморфный карбид фосфора. Ацетилениды и метаниды — солеобразные кристаллы с преобладанием ионного характера связи разлагаются водой с образованием соответственно ацетилена и метана:
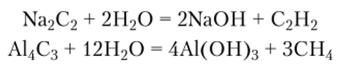
Алмазоподобные карбиды — кристаллы с трехмерными кристаллическими решетками, образуемыми ковалентными связями, не разлагаются водой, большинством кислот и щелочей.
Карбид фосфора PoCq — светло-желтое аморфное вещество, устойчивое к действию воды, кислот и щелочей, но загорающееся на воздухе даже при слабом нагревании.
Угольная кислота, карбонаты. Химические свойства этих веществ и существующие в природе равновесия между ними в огромной степени определяют условия жизни и даже саму возможность существования живых существ на нашей планете.
Угольная кислота. По первой ступени диссоциации.
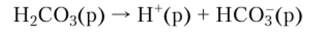
угольная кислота приблизительно равносильна муравьиной НСООН и превосходит, но силе уксусную СН3СООН, константы диссоциации которых равны соответственно 1,77−10 4 и 1,75−10 Истинная константа диссоциации угольной кислоты по первой ступени.
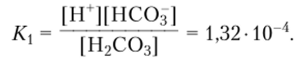
Кажущаяся константа первой ступени диссоциации, учитывающая обе формы С02, растворенного в воде, много меньше:
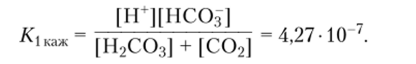
Вторая ступень диссоциации угольной кислоты 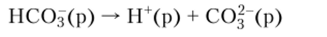 имеет очень небольшую константу равновесия:
имеет очень небольшую константу равновесия: 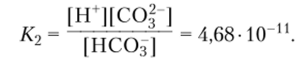
Карбонаты. Угольная кислота, будучи двухосновной, образует два ряда солей: карбонаты с анионом СО|" и гидрокарбонаты с анионом НС03. Карбонат-ионы СО|~ имеют плоское треугольное строение:
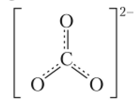
Орбитали атома углерода проявляют в них л/г-гибридизацию, а тг-связь, образованная негибридизованными p-электронами атома углерода и грех атомов кислорода, делокализована.
Карбонаты — кристаллические вещества. Хорошо растворимы карбонаты щелочных металлов (см. табл. 15.5), аммония и таллия (1). Карбонаты всех других металлов малорастворимы. Все гидрокарбонаты достаточно хорошо растворимы.
Растворы хорошо растворимых карбонатов всегда имеют pH > 7 вследствие гидролиза по аниону:
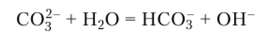
Гидролиз гидрокарбонатов по уравнению.
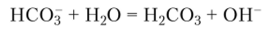
происходит слабее, и водные растворы гидрокарбонатов имеют меньшие значения pH, чем растворы карбонатов равной концентрации.
Получить гидрокарбонат можно действием избытка растворенного в воде диоксида углерода на осадок карбоната, например:
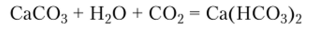
Гидрокарбонаты термически неустойчивы. Уже при нагревании чуть выше 100 °C гидрокарбонаты превращаются в карбонаты с выделением С02 и H2Q.
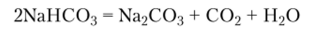
Температуры разложения карбонатов значительно выше. Карбонаты щелочных металлов разлагаются только после плавления. Карбонаты щелочноземельных и (/-металлов менее устойчивы и разлагаются при различных, иногда довольно высоких температурах с образованием оксидов:
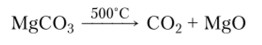
Поскольку диоксид углерода и вода участвуют в процессах образования минералов, карбонаты широко распространены в природе. Наряду с обычными карбонатами, такими, как кальцит СаС03 и магнезит MgC03, известны также двойные карбонаты, например доломит MgC03— СаС03 и основные карбонаты, например малахит CuC03Cu (0H)2.