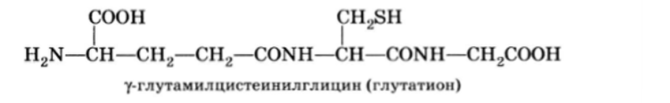Методы идентификации аминокислот

Если исследуемое вещество амфотерно и доказано присутствие в нем аминной и карбоксильной групп, как правило, встает лишь вопрос об их взаимном расположении. Для наиболее важных природных и синтетических а-аминокислот разработаны методы бумажной хроматографии, позволяющие с большой степенью надежности идентифицировать исследуемую аминокислоту. а-Аминокислоты дают характерное окрашивание… Читать ещё >
Методы идентификации аминокислот (реферат, курсовая, диплом, контрольная)
Если исследуемое вещество амфотерно и доказано присутствие в нем аминной и карбоксильной групп, как правило, встает лишь вопрос об их взаимном расположении. Для наиболее важных природных и синтетических а-аминокислот разработаны методы бумажной хроматографии, позволяющие с большой степенью надежности идентифицировать исследуемую аминокислоту. а-Аминокислоты дают характерное окрашивание с нингидрином и красное окрашивание с водным раствором FeCl3, исчезающее при подкислении соляной кислотой.
Методы ИКи УФ-спектроскопии могут лишь доказать наличие обеих функциональных групп (см. гл. 15 и 17). При съемке спектров ПМР аминокислот обычно используют D20 в качестве растворителя или снимают спектр не самих аминокислот, а их производных (эфиров или ацильных производных). На рис. 83 приведен спектр ПМР р-аланина. В спектре отчетливо видны триплеты метиленовых групп; в более слабом поле — триплет СН2-группы, ближайшей к карбоксилу. Протоны группы NH2 и протон карбоксила в D20 претерпевают изотопный обмен и не видны отдельно.
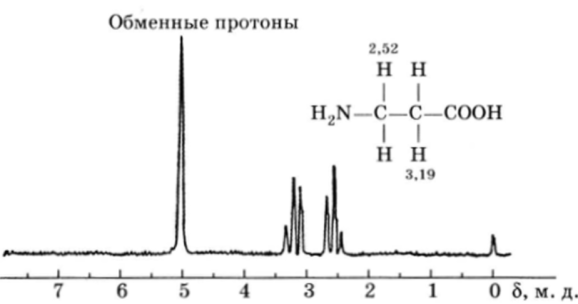
Рис. 83. ПМР-спектр р-аланина (J = 9,0 Гц).
Белки. Классификация. Общие свойства
Белки входят в состав всех живых организмов, но особо важную роль они играют в животных организмах, которые состоят главным образом из тех или иных форм белков. Мышцы, покровные ткани, внутренние органы, хрящи, кровь — все это белковые вещества.
Растения синтезируют белки (и их составные части — а-аминокислоты) из С02 и Н20 за счет фотосинтеза, усваивая остальные элементы белков (N, Р, S, Fe, Mg) из растворимых солей, находящихся в почве. В последние годы доказано, что растения могут усваивать и непосредственно азот атмосферы. Животные организмы в основном получают готовые аминокислоты с пищей и на их базе строят белки своего организма. Ряд аминокислот (заменимые аминокислоты) может синтезироваться непосредственно животными организмами.
Белки представляют собой биополимеры «-аминокислот. Если при гидролизе белковые вещества распадаются в конечном итоге до а-аминокислот, то мы имеем дело с так называемыми простыми белками, или протеинами. Но существуют и сложные белки, или протеиды, в состав которых входят остатки соединений, принадлежащих к иным классам органических и неорганических веществ (простетические группы).
Белки имеют большую молекулярную массу (104—107), многие белки растворимы в воде, но образуют, как правило, коллоидные растворы, из которых выпадают при увеличении концентрации неорганических солей, добавлении солей тяжелых металлов, органических растворителей или при нагревании (денатурация).
Для выделения и очистки белков используются специфические методы химии белка: диализ (отделение неорганических солей и низкомолекулярных органических соединений от белков благодаря тому, что белки не проходят через полупроницаемые мембраны из коллодия, целлофана и т. д.), электрофорез, хроматографирование на ионнообменных смолах и молекулярных ситах, лиофильная вакуумная сушка (испарение замерзшей воды в высоком вакууме) и т. д.
Молекулярную массу белков определяют методами высокомолекулярной химии.
Наиболее характерными качественными реакциями на белки являются:
- 1) биуретовая реакция — появление фиолетового окрашивания при обработке солями меди в щелочной среде (ее дают все белки);
- 2) ксантопротеиновая реакция — появление при действии концентрированной азотной кислоты желтого окрашивания, переходящего при действии аммиака в оранжевое (ее дают не все белки);
- 3) реакция Миллона — кипячение раствора белка с раствором нитрата ртути в смеси азотной и азотистой кислот приводит к выпадению красно-коричневого осадка (реакция на тирозин);
- 4) нингидринная реакция — появление синего окрашивания при кипячении с водным раствором нингидрина (на все белки).
По ряду характерных свойств простые белки (протеины) можно разделить на несколько подгрупп.
Альбумины. Они растворимы в воде, свертываются при мость в 80%-м спирте. Представителем этих белков может служить глиадин, составляющий главную часть клейковины.
Клейковина пшеницы — это смесь различных белков, в которой преобладает уже упомянутый выше глиадин. Другие белки, входящие в состав клейковины, в спирте не растворяются.
Склеропротеины. Склеропротеины — это нерастворимые белки, из которых состоят наружные покровы тел животных, они содержатся также в скелете и в соединительной ткани. К ним относятся кератин, коллагены, эластин, фиброин.
Кератин является главной составной частью волос, рогов, копыт, ногтей, перьев и верхнего слоя кожи. Скорлупа куриного яйца состоит из извести и кератина. Если растворить известь скорлупы яйца в кислоте, то остается мягкая пленка, состоящая из кератина; из кератина состоит и та кожица, которая следует за скорлупой яйца. Кератин богат серой.
Коллагены чрезвычайно распространены в животных организмах. Из коллагенов состоит соединительная ткань; они содержатся в хрящах. Кости позвоночных животных состоят из неорганических веществ (фосфата и карбоната кальция), жира и коллагенов.
Эластин входит в состав сухожилий и других эластичных соединительных тканей.
Нити сырого шелка состоят из белкового вещества — фиброина, покрытого серицином — белковым веществом, играющим роль шелкового клея. При кипячении с водой шелк освобождается от серицина, который при этом переходит в раствор.
К сложным белкам — протеидам относятся следующие.
Фосфопротеиды. В состав фосфопротеидов входит фосфорная кислота. Они, в противоположность нротаминам, обладающим основными свойствами, имеют кислотный характер.
Главным представителем фосфопротеидов является казеин молока. Он обладает настолько явно выраженным кислотным характером, что разлагает углекислые соли с выделением оксида углерода (IV). Казеин растворяется в слабых растворах щелочей, образуя с ними соли. Так, в молоке казеин содержится в виде кальциевой соли. Соли казеина называются казеинатами.
Из других фосфопротеидов следует отметить вителлину который входит в состав желтка куриного яйца.
Нуклеопротеиды. Содержатся они в клеточных ядрах. При осторожном гидролизе они расщепляются на белки и нуклеиновые кислоты.
Нуклеиновые кислоты являются весьма сложными веществами, расщепляющимися при гидролизе на фосфорную кислоту, углеводы и азотсодержащие органические вещества групп пиримидина и пурина (см. гл. 25).
Хромопротеиды. Под этим названием известны протеиды, которые представляют собой сочетание белков с окрашенными веществами. Из хромопротеидов наиболее изучен гемоглобин — красящее вещество красных кровяных шариков. Значение гемоглобина в жизни человека и животных очень велико. Он играет роль переносчика кислорода от легких к тканям. Кроме того, гемоглобин вместе с плазмой крови осуществляет регуляцию pH крови и перенос оксида углерода (1У) в организме. Характерной особенностью гемоглобина является его способность соединяться с оксидом углерода (Н), после чего он теряет способность соединяться с кислородом. Этим объясняется ядовитое действие оксида углерода (И).
Г липопротеиды. Некоторые белки этой группы встречаются в слизистых выделениях животных организмов и обусловливают свойство этих выделений вытягиваться в нити даже при сравнительно большом разбавлении. Эти белки образуются в подчелюстной железе (подчелюстная железа — одна из слюнных желез), печени, железах желудка и кишечника. Другие гликопротеиды содержатся в хрящах, яичном белке, стекловидном теле глаза и т. д.
Исследованные представители гликопротеидов являются сочетанием белков с олигоили полисахаридами.
Липопротеиды. При гидролизе липопротеиды распадаются на белок и растворимые в эфире жиры, лецитины и другие фосфатиды.
Ряд пептидов играет важную самостоятельную роль в существовании живых организмов.
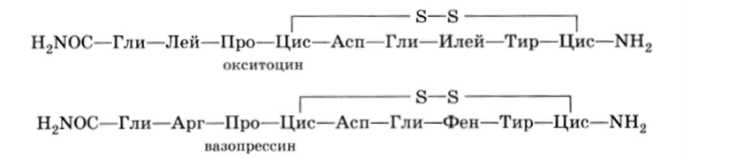
В 1955 г. Дю Виньо получил Нобелевскую премию за синтез циклических пептидных гормонов: окситоцина, регулирующего сокращение гладкой мускулатуры, и вазопрессина, регулирующего водный обмен:
Глутатион входит в активные центры ряда окислительно-восстановительных ферментов и содержится в тканях в свободном состоянии: