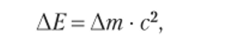1. Закон сохранения массы веществ (М. В. Ломоносов, 1748 г., А. Л. Лавуазье, 1789 г.): масса веществу вступивших в химическую реакцию, равна массе продуктов реакции.
Атомно-молекулярное учение этот закон объясняет следующим образом: в результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка, т. е. химическое превращение — это процесс разрыва одних связей между атомами и образование других, в результате чего из молекул исходных веществ получаются молекулы продуктов реакции. Поскольку число атомов до и после реакции остается неизменным, то их общая масса также изменяться не должна. Под массой в то время понимали величину, характеризующую количество материи.
В начале XX в. формулировка закона сохранения массы подверглась пересмотру в связи с появлением теории относительности (А. Эйнштейн, 1905 г.), согласно которой масса тела зависит от его скорости и, следовательно, характеризует не только количество материи, по и ее движение. Полученная телом энергия АЕ связана с увеличением его массы Дт соотношением.
где с — скорость света в вакууме (3 • 108 м/с).
Так как 1 кДж энергии соответствует изменению массы на ~Ю" И г, а энергетические эффекты химических реакций находятся в пределах 10—1000 кДж на единицу количества вещества, то величина Дт в химических реакциях практически не может быть измерена и ею можно пренебречь. Это соотношение имеет значение для ядерных реакций, где ДЕ в -10° раз больше, чем в химических реакциях.
Исходя из закона сохранения массы, можно составлять уравнения химических реакций и по ним производить расчеты. Этот закон является основой количественного химического анализа.