Работа 15.11.6. Определение усвояемой фосфорной кислоты в суперфосфате

Растворение остатка (приготовление цитратной вытяжки). Фильтр с нерастворившимся остатком суперфосфата осторожно вынимают из воронки и переносят в другую мерную колбу вместимостью 250 мл. Прибавляют 100 мл реактива Петермана и встряхивают до тех пор, пока фильтр не распадется на мелкие волокна. Доводят объем жидкости до метки, закрывают колбу пробкой, оставляют стоять минимум на 15 ч при… Читать ещё >
Работа 15.11.6. Определение усвояемой фосфорной кислоты в суперфосфате (реферат, курсовая, диплом, контрольная)
Агрохимики различают в суперфосфате четыре вида «фосфорной кислоты» (точнее, Р205): свободную, водорастворимую, усвояемую и общую.
Свободная фосфорная кислота обычно присутствует в суперфосфате. Количество ее определяют, титруя водную вытяжку из удобрения щелочью.
Водорастворимый Р205 складывается из свободной фосфорной кислоты и ее растворимых в воде солей. Определяют водорастворимый Р205 в водной вытяжке из суперфосфата путем осаждения иона РО^- магнезиальной смесью.
Усвояемый Р205 представляет собой сумму водорастворимого и так называемого цитратно-растворимого оксида фосфора Р205.
Общий Р205 — это общее содержание оксида фосфора Р205 в суперфосфате. Для определения его растворяют навеску удобрения в царской водке, отфильтровывают осадок оксида кремния Si02, связывают Fe3+ и А13+ лимонной кислотой, после чего осаждают ион РО|_ магнезиальной смесью.
Чаще всего определяют в суперфосфате усвояемый Р205. При этом навеску сначала обрабатывают водой, т. е. переводят в раствор водорастворимые вещества — фосфорную кислоту Н3Р04 и дигидрофосфат кальция Са (Н2Р04)2. Затем, отфильтровав нерастворимый осадок, обрабатывают его аммиачным раствором цитрата аммония (реактивом Петермана), т. е. извлекают цитратнорастворимое соединение — гидрофосфат кальция СаНР04.
Смешав равные объемы водного и цитратного растворов, осаждают ион РО^~ магнезиальной смесью.
Осадок отфильтровывают, промывают и прокаливают. Гравиметрическую форму Mg2P207 пересчитывают на Р205 и выражают в процентах. Реактив Петермана и магнезиальную смесь готовят заблаговременно.
Приготовление реактива Петермана. 50,0 г химически чистой лимонной кислоты растворяют приблизительно в 70 мл аммиака (р = 0,92 г/см3). Дают раствору остыть и разбавляют водой до плотности 1,09 г/см3. Затем на каждые 100 мл полученного раствора цитрата аммония прибавляют еще по 5 мл раствора аммиака с массовой долей 25%. Отстоявшийся раствор фильтруют. Реактив Петермана должен иметь плотность 1,082—1,083 г/см3.
Приготовление магнезиальной смеси. 55 г химически чистого хлорида магния MgCl2-6H20 и 70 г хлорида аммония NH4C1 растворяют в 650 мл дистиллированной воды. К полученной смеси прибавляют 350 мл раствора аммиака (р = 0,96 г/см3).
Ход определения. 1. Взятие навески и приготовление водной вытяжки. Из тонкоизмельченной пробы суперфосфата берут точную навеску около 2,5 г, переносят ее в фарфоровую ступку, прибавляют 25 мл воды и тщательно растирают пестиком. Жидкость из ступки декантируют на фильтр; фильтрат собирают в мерную колбу вместимостью 250 мл. Остаток обрабатывают в ступке тем же способом еще 3 раза, всякий раз сливая жидкость на фильтр. Затем содержимое ступки количественно переносят на тот же фильтр и промывают водой, пока в колбе не соберется приблизительно 200 мл фильтрата. Если фильтрат помутнеет, добавляют несколько капель азотной или хлороводородной кислоты. Наконец, объем раствора в колбе доводят водой до метки и перемешивают.
2. Растворение остатка (приготовление цитратной вытяжки). Фильтр с нерастворившимся остатком суперфосфата осторожно вынимают из воронки и переносят в другую мерную колбу вместимостью 250 мл. Прибавляют 100 мл реактива Петермана и встряхивают до тех пор, пока фильтр не распадется на мелкие волокна. Доводят объем жидкости до метки, закрывают колбу пробкой, оставляют стоять минимум на 15 ч при комнатной температуре, затем помещают на теплую водяную баню (40 °С) на 1 ч.
Приготовив таким образом водную и цитратную вытяжки, переносят мерной пипеткой по 50 мл каждой в коническую колбу. Прибавляют по каплям 25 мл магнезиальной смеси и 30—40 мин энергично перемешивают (вместо этого можно оставить колбу стоять на 8—12 ч).
- 3. Фильтрование и промывание. Осадок фосфата магния-аммония MgNH4P04, как обычно, фильтруют, промывают разбавленным раствором аммиака, высушивают, озоляют и прокаливают до постоянной массы.
- 4. Вычисления. Зная массу пирофосфата магния Mg2P207, вычисляют массовую долю (%) Р205 в суперфосфате по формуле
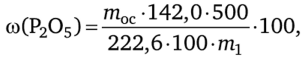
где moc— масса прокаленного осадка Mg2P207, г; 142,0 — молярная масса Р205; 500 — общий объем водоцитратной вытяжки из суперфосфата, мл; 222,6 — молярная масса Mg2P207; 100 — объем вытяжки, взятый для осаждения фосфат-иона, мл; тг — навеска суперфосфата, г.
Например, если навеска составляла 2,4622 г, а масса Mg2P207 оказалась равна 0,1298 г, то.

Аналогично определяют содержание усвояемой Р205 в преципитате.