Энтропия идеального газа

При г = 0 концентрация п (0) = п0, т. е. параметр п0 есть значение концентрации молекул у поверхности Земли. С увеличением z концентрация молекул убывает экспоненциально при Т = const. Для воображаемой модели изотермической атмосферы Земли графики функции (4.34), соответствующие различным значениям температуры, приведены на рис. 4.5. Площадь. Так как в силу равенства (4.32) выражение TV‘y~l… Читать ещё >
Энтропия идеального газа (реферат, курсовая, диплом, контрольная)
Используя определение энтропии (1.12), первое начало термодинамики (1.4) и формулу (1.5) для элементарной работы, получим выражение для приращения энтропии в некотором равновесном процессе.
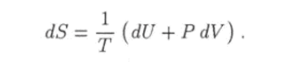
При помощи законов идеального газа (4.13) и (4.21) это выражение можно преобразовать к виду.
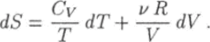
Нетрудно проверить, что функция S = 5(Т, V), имеющая такой дифференциал, есть.

здесь символ const обозначает слагаемые, не зависящие от Т и V} но они могут зависеть от числа частиц N или от числа молей и.
При адиабатическом процессе по определению энтропия должна оставаться постоянной. Чтобы убедиться в том, что функция (4.33) удовлетворяет этому условию, достаточно преобразовать ее к виду.
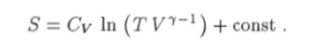
Так как в силу равенства (4.32) выражение TV‘y~l не изменяется со временем в адиабатическом процессе, энтропия при этом также будет оставаться постоянной.
Барометрическая формула
Рассмотрим идеальный газ, находящийся в состоянии термодинамического равновесия в однородном поле силы тяжести. Если газ состоит из одинаковых молекул, то потенциальная энергия U каждой из них будет.
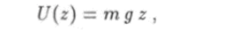
где тп — масса молекулы, д — ускорение свободного падения, г — высота, на которой находится молекула над поверхностью Земли. Для описания распределения молекул газа в пространстве можно применить закон Больцмана (3.29), который теперь будет иметь вид.
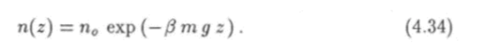
При г = 0 концентрация п (0) = п0, т. е. параметр п0 есть значение концентрации молекул у поверхности Земли. С увеличением z концентрация молекул убывает экспоненциально при Т = const.
Формулу (4.34) можно применять для описания распределения молекул воздуха над земной поверхностью, но только к сравнительно небольшим объемам атмосферы, где поле силы тяжести и температура воздуха однородны.
Для воображаемой модели изотермической атмосферы Земли графики функции (4.34), соответствующие различным значениям температуры, приведены на рис. 4.5. Площадь.
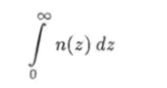
под каждой из этих кривых одна и та же, и равна числу молекул воздуха, приходящихся на квадратный метр земной поверхности.
При увеличении температуры концентрация п0 молекул у поверхности Земли уменьшается, а кривая зависимости п = n (z) становится более пологой, т. е. молекулы более равномерно распределяются в пространстве. На характер распределения молекул в пространстве и вид зависимости п = n (z) оказывают влияние две тенденции в поведении молекул газа: 1) под действием силы тяжести молекулы стремятся опуститься на земную поверхность, 2) в результате теплового движения молекулы стремятся расположиться равномерно в пространстве. При низких температурах преобладает первая тенденция и атмосфера уплотняется и становится тоньше. При высоких температурах доминирует вторая тенденция и концентрация молекул медленнее убывает с высотой.
Подставив выражение (4.34) в формулу (4.8), получим соотношение.
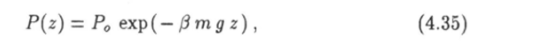
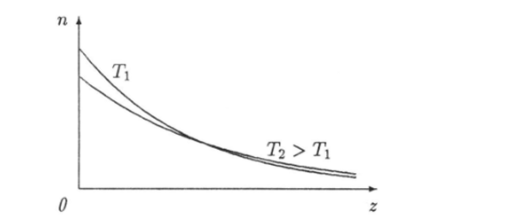
Рис. 4 5. Зависимость концентрации молекул в земной атмосфере от высоты.
где Р0 = п0кТ. Формула (4.35) описывает зависимость атмосферного давления от высоты и называется барометрической формулой.