Задачи по теме «Изобарный процесс»

Эта модель позволяет нам наблюдать изобары для разных значений давления. Мы можем менять значение давления и наблюдать, что происходит с графиком зависимости объема от температуры. Так же с помощью энергетической диаграммы мы может видеть какие из параметров (количество теплоты Q, полученной газом, произведенная газом работа. Указания: Ученик, используя модель, фиксирует две точки эксперимента… Читать ещё >
Задачи по теме «Изобарный процесс» (реферат, курсовая, диплом, контрольная)
Задачи составлены, используя диск «Открытая физика» модель «Изобарный процесс» .
Эта модель позволяет нам наблюдать изобары для разных значений давления. Мы можем менять значение давления и наблюдать, что происходит с графиком зависимости объема от температуры. Так же с помощью энергетической диаграммы мы может видеть какие из параметров (количество теплоты Q, полученной газом, произведенная газом работа.
A и изменение ДU его внутренней энергии) меняются, а какие остаются постоянными.
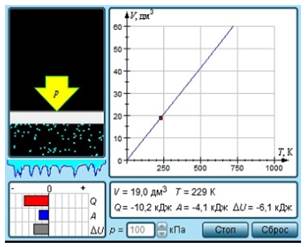
Задача 1.
В ходе изобарного процесса кривая изобары при увеличении давления располагается:
- 1) выше
- 2) ниже
- 3) график не меняется
Правильный ответ: 2.
Ученик задает одно значение давления из возможного диапазона и запускает модель. Затем увеличивает его и сравнивает, какие изменения произошли с графиком.
Задача 2
Используя модель, проверьте экспериментально справедливость закона Гей-Люссака. (Выдвинуть гипотезу и проверить ее с помощью модели).
Правильный ответ: Ученик должен снять несколько показаний с модели и убедиться в справедливости закона V/T = const.
Ученик выбирает несколько значений давления из диапазона, заданного моделью. Затем последовательно заносит эти числа в модель и, запустив ее, определяет температуру и объем. Подставляет полученные значения в закон Гей-Люссака.
Задача 3
Найдите полученное газом количество теплоты Q, произведенную газом работу A и изменение его внутренней энергии ДU для 1 моль идеального газа в ходе изобарного процесса при изменении объема от V1 до V2 и изменении температуры от Т1 до Т2. Значения V1, V2, Т1 и Т2 выбрать на модели самостоятельно. Проверить результаты компьютерного эксперимента расчетом.
Указания: Ученик, используя модель, фиксирует две точки эксперимента и снимает показания с модели. Затем, применяя формулы для расчета работы при изменении объема газа (A = pДV), изменения внутренней энергии (где i число степеней свободы для 1 моль идеального газа), первый закон термодинамики (Q = A + ДU), проверяет полученные значения.
Задача 2.
Идеальный газ, масса которого т и молярная масса м, расширяется изобарно при некотором давлении. Начальная температура газа Т, конечная Т Определить работу, совершаемую газом.
Решение:
1. Работа в изобарном процессе
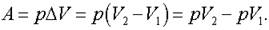
Из уравнения Менделеева-Клапейрона.
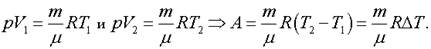
Оказалось, что работу в изобарном процессе можно выразить не только через изменение объема по формуле, но и через изменение температуры:
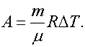
Полученный результат следует иметь в виду, так как он часто используется при решении более сложных задач.
Ответ:
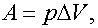
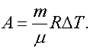
2. Гелий (Не) нагревается при постоянном давлении. При этом ему сообщено Q = 20 кДж теплоты. Определить изменение внутренней энергии газа и совершенную им работу.
Решение:
Так как по условию задачи р = const, то совершаемая газом работа.
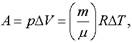
где т — масса газа, м — его молярная масса,.
T — изменение температуры.
Гелий — одноатомный газ, поэтому его внутренняя энергия.
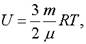
а ее изменение.
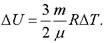
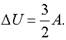
Сравнивая формулы для работы, А и изменения внутренней энергии? U, получаем, что Запишем первый закон термодинамики для этого процесса:
Следовательно, работа.
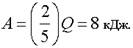
Изменение внутренней энергии.
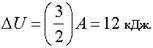
Ответ:
3. Температура некоторой массы т идеального газа с молярной массой м меняется по закону, где, а = const, > 0. Найти работу, совершенную газом при увеличении объема от V1 до V.
Поглощается или выделяется теплота при таком процессе?
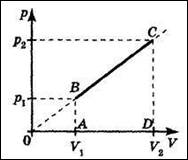
Решение:
Процесс не является ни изобарным, ни изохорным, ни тем более изотермическим. Запишем для любого состояния в этом процессе уравнение Менделеева—Клапейрона:
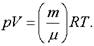
Так как, то после подстановки получим зависимость давления от объема в виде.
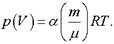
представлен на рисунке.
Совершенная газом работа График этой зависимости.
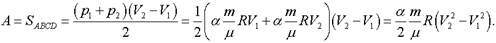
Для ответа на второй вопрос задачи воспользуемся первым законом термодинамики: Так как газ расширяется, то его работа, А > 0. Изменение внутренней энергии идеального газа пропорционально изменению температуры: ?U ~ ?T. Так как и объем возрастает, то возрастает и температура, поэтому? U > 0. Тогда и Q > 0, что соответствует поглощению газом теплоты.
4. При адиабатном сжатии 1 моля одноатомного газа внешними силами была совершена работа А. Во сколько раз увеличилась среднеквадратичная скорость молекул этого газа, если начальная температура газа равна Т1?
Решение:
Первый закон термодинамики для адиабатного процесса записывается в виде.
0 = ?U + А',.
где ?U — изменение внутренней энергии газа, А' — работа газа в этом процессе.
Так как газ сжимают, то А'<0, в то же время внешние силы совершаютположительную работу А, причем А'=-А. Следовательно,.
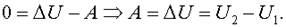
Внутренняя энергия 1 моля идеального одноатомного газа поэтому.
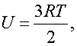
Отсюда выражаем конечную температуру газа.
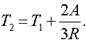
Средняя кинетическая энергия молекул.
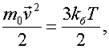
где Т — температура.
Тогда среднеквадратичная скорость.
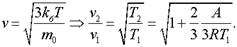
Ответ:

5. Какое количество теплоты получит 1 моль идеального одноатомного газа при изобарном нагревании от некоторой начальной температуры и последующем адиабатном расширении, если при адиабатном расширении газ совершает работу А, а в конечном состоянии температура равна начальной?
Решение:
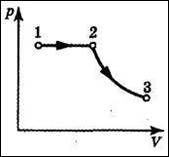
Построим график зависимости давления от объема в осях р, V (рисунок):
- 1—2 — изобарное нагревание, сопровождаемое увеличением объема;
- 2—3 — адиабатное расширение. Работа в адиабатном процессе

Следовательно,.
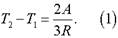
Количество теплоты, полученное газом в изобарном процессе:
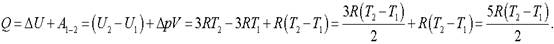
Подставляя из формулы (1) разность температур находим, что.
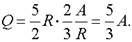
Ответ:
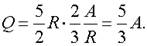
6. Масса т идеального газа, находящегося при температуре Т, охлаждается изохорно так, что давление падает в п раз. Затем газ расширяется при постоянном давлении. В конечном состоянии его температура равна первоначальной.
Молярная масса газа м. Определить совершенную газом работу.
Решение:
График указанного процесса приведен на рисунке.
Здесь 1—2 — изохора, 2—3 — изобара. Искомая работа где А1 — работа на участке 1—2, а А2−3 2 — работа на участке 2—3. На участке 1—2 V — const, поэтому, А = 0. На участке 2—3 р = const и 1−2.
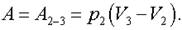
Выражения подобного вида преобразовывают так, чтобы выделить произведение давления на объем в состоянии, в котором задана температура:
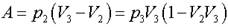
здесь учтено, что р2 = р3.
Из уравнения Менделеева-Клайперона для состояния 3 находим, что.
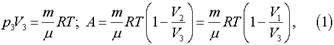
так как из состояния 1 в состояние 3 можно переходить по изотерме 1—3 (в этом случае говорят, что точки 1 и 3 расположены на одной изотерме). По закону Бойля—Мариотта.
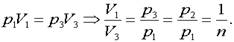
После постановки в формулу (1) получим.
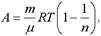
Ответ:
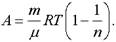
Задача 3.
В цилиндре с площадью основания 1 дм² под поршнем находится газ. При изобарном нагревании поршень переместился на 20 см. Какую работу совершил газ, если наружное давление равно 100 кПа?.
Решение Работа газа в термодинамике определяется формулой.
где — изменение объема.
В нашем случае, поэтому.
Ответ:
Задача 4.
На сколько градусов надо нагреть 3,2 кг одноатомного газа, чтобы при его изобарном нагревании была совершена работа 8,31 кДж? Определить, также, изменение внутренней энергии газа. Молярная масса газа М = 32 г/моль.
Решение Работа газа в изобарном процессе определяется формулой.
.
где — количество вещества, поэтому.
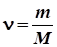
;
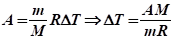
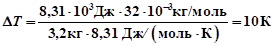
.
Изменение внутренней энергии одноатомного газа определяет формула:
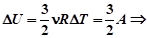

.
Ответ:; .
Задача 5.
При увеличении абсолютной температуры в изобарном процессе в 1,4 раза объем увеличился на 40 см³. Найти первоначальный объем.
Решение.
Процесс изобарный, поэтому уравнение Клапейрона имеет следующий вид:
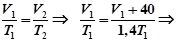
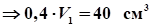

.
Задачи для самостоятельного решения Задача 1.
Найти давление 3 моль азота в баллоне объемом 28 л, если среднеквадратичная скорость его молекул равна 400 м/с. Молярная масса азота 28 г/моль.
E. Ответ: P = 1,6105 Па.
Задача 2.
Определить среднюю кинетическую энергию молекулы одноатомного идеального газа и концентрацию молекул при температуре 290 К и давлении 0,8 МПа.
E. Ответ: Eср =.
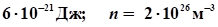
Задача 3.
Найти плотность углекислого газа, который при температуре 300К имеет давление 100 кПа. Молярная масса углекислого газа М=44 г/моль.
E. Ответ:
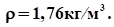
Задача 4.
Найти массу воздуха в помещении объемом 100 м³ при температуре 17С и давлении 100 кПа. Молярная масса воздуха = 29 г/моль.
Дано:
E. Ответ:
Задача 5.
Какова была начальная температура воздуха, если при нагревании при постоянном давлении на 3К его объем увеличился на 1% от первоначального?
Ответ:
Задача 6.
При изотермическом процессе объем газа увеличился в два раза. На сколько паскалей изменилось давление газа, если начальное давление было 1000 Па?
Ответ: .
Задача 7.
При увеличении давления в 1,5 раза объем газа уменьшился на 2 м³. Найти начальный и конечный объемы газа, считая процесс изотермическим.
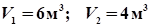
E. Ответ: .
Задача 8.
При сжатии газа его объем уменьшился с 8 до 5 л, а давление повысилось на 60 кПа. Найти первоначальное давление газа, считая процесс изотермическим.
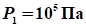
Ответ: .
Задача 9.
При увеличении абсолютной температуры идеального газа в два раза давление газа увеличилось на 25%. Во сколько раз при этом изменился объем?
Ответ: Увеличился в 1,6 раза.
Задача 10.
При изобарном нагревании 10 молей идеального газа его объем увеличился на 0,01 м³, температура возросла на 10 К. Чему равно давление газа?
Задача 11.
Баллон содержит г кислорода и г аргона. Давление смеси МПа, температура К. Принимая данные газы за идеальные, определить V баллона. Ответ: V=26.2 л.