Материальные и тепловые расчеты процесса 2-х ступенчатой конверсии метана в производстве аммиака

Двухступенчатая система конверсии аммиака Двухступенчатая система позволяет повысить степень превращения метана. Так как реакция метана с водой — эндотермическая, то повышение температуры повышает скорость реакции. Температура, необходимая для полного превращения в процессе — 1300 К. Материал из которого сделаны части реактора не позволяют использовать его при таких высоких температурах. Поэтому… Читать ещё >
Материальные и тепловые расчеты процесса 2-х ступенчатой конверсии метана в производстве аммиака (реферат, курсовая, диплом, контрольная)
Задание.
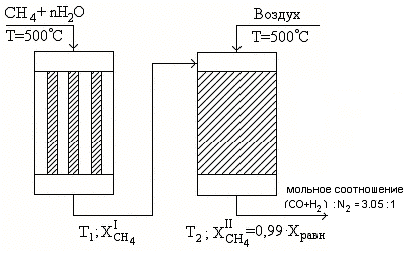
Температура Т1 — 850 °C Температура Т2 — 1050 °C.
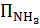
Производительность = 1500 т/сутки Концентрация азота в природном газе.
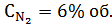
Потеря АВС с продувочным газом.
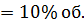
Коэффициент избытка H2O — 4.
1. Материальный баланс Реакции, протекающие при конверсии метана водяным паром:
СН4 + Н2О -> СО + ЗН2; (1).
СО + Н2О -> co2 + н2; (2).
СН4 + Н2О -> СО + 4H2; (3).
Реакции с кислородом воздуха:
CH4 + 0,5О2 -> СО + 2Н2; (4).
СН4 + 2О2 -> СО2 + 2Н2О; (5).
Реакция водяного газа:
2Н2 + О2 -> 2H2O (6).
С учётом производительности производства аммиака рассчитаем количество азота и водорода, необходимое для его получения:
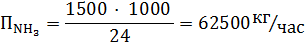
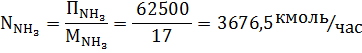
Реакция образования аммиака из водорода и азота следующая:
3H2 + N2 = 2NH3.
Рассчитаем количество АВС, необходимое для получения данного количества аммиака:
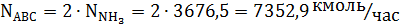
При продувке часть АВС теряется, рассчитаем начальное количество АВС:
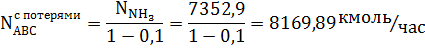
Рассчитаем количество азота и водорода.
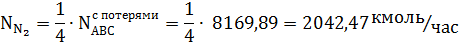
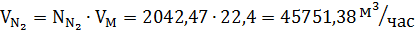
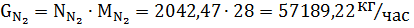
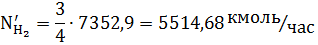
Так как часть водорода образуется при конверсии углекислого газа, пересчитаем количество водорода в АВС:
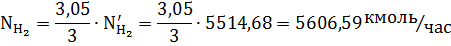
Рассчитываем равновесную степень превращения, с помощью программы на компьютере кафедры (T2=1050+273=1323K, P=30 атм):
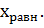
Рассчитаем Исходые данные для расчёта:
CCH4= 0,14 мольн. доли, СH2O =0,67 мольн. доли, СN2 = 0,19 мольн. доли.
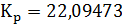
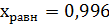
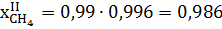
Азот в реакции не вступает в превращения, приходит из воздуха и природного газа.
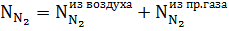
Водород образуется по реакции метана и расходуется на реакцию выгорания кислорода:
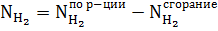
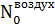
Пусть — исходное количество воздуха, а — исходное количество природного газа, то исходя из уравнений (3) и (6) получаем систему:
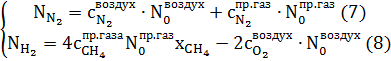
Решая систему учтем, что воздух сухой, состоит только из кислорода и азота, в соотношении 0,21/0,79 об. доли, соответственно.
Получим:
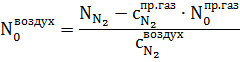
кмоль/час.
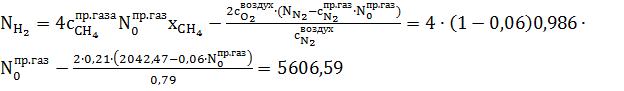
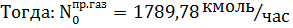
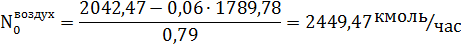
Количество метана и азота в природном газе:
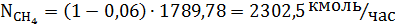
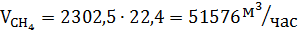
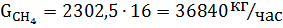
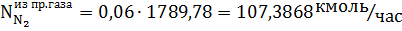
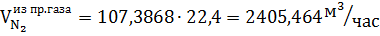
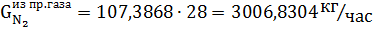
Исходное количество воды:
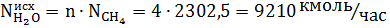
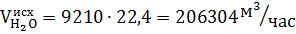
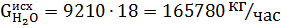
Количество кислорода и азота в воздухе:
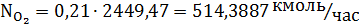
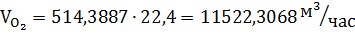
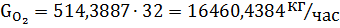
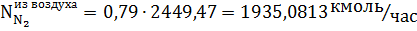
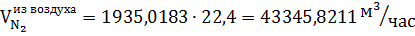
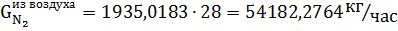
Вода в процессе расходуется и образуется:
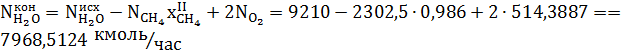
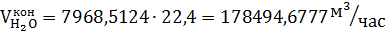
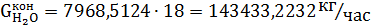
Метан, остающийся после реакции:
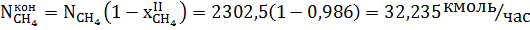
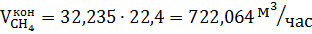
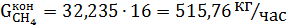
Так же образуется окись углерода в количестве:
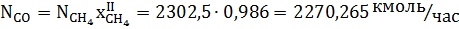
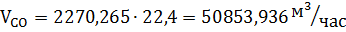
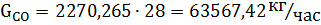
Количество водорода после конверсии метана:
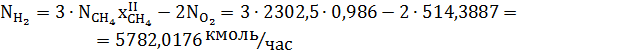 Расход. | кмоль/час. | кг/час. | Приход. | кмоль/час. | 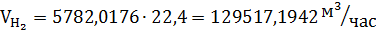 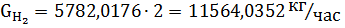 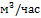 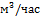 кг/час. | ||
Пр. газ. | 1789,78. | 40 091,072. | 29 710,351. | ABC. | 7824,4876. | 175 268,522. | 234 734,628. |
CH4 | 2302,5. | H2 | 5782,0176. | 129 517,1942. | 11 564,0352. | ||
N2 | 107,3868. | 2405,4643. | 3006,8304. | N2 | 2042,47. | 45 751,38. | 57 189,22. |
H2O. | H2O. | 7968,5124. | 178 494,677. | 143 433,2232. | |||
Воздух. | 2449,47. | 54 868,128. | 71 034,63. | CH4 | 32,235. | 722,064. | 515,76. |
O2 | 514,3887. | 11 522,3068. | 16 460,4384. | CO. | 2270,265. | 50 853,936. | 63 567,42. |
N2. | 1935,0813. | 43 345,8211. | 54 182,2764. | ||||
Итого. | 377 014,5. | Итого. | 511 004,3. |
2. Тепловой баланс Уравнение теплового баланса:
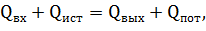
где.
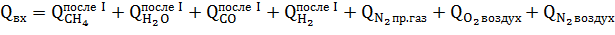
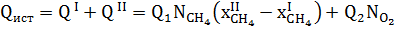
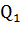
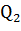
= 206,4 кДж/моль Н2; = -242,3 кДж/моль H2O — тепловые эффекты реакций соответственно.
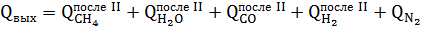
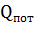
примем 5% от приходящей теплоты.
Количество теплоты, принесённое каждым отдельным компонентом найдём как:
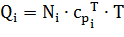
На входе во 2 реактор при T = 1123 К и для воздуха при T = 773К:
Вещество. | сp, кДж/(кмоль· К). |
CH4 | 64,8988. |
H2O. | 39,1490. |
CO. | 31,8313. |
H2 | 30,1202. |
N2 (пр. газ). | 31,5095. |
О2 (воздух). | 31,647. |
N2 (воздух). | 30,015. |
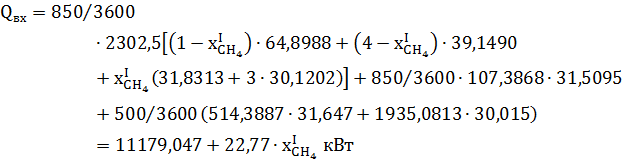
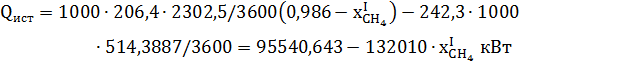
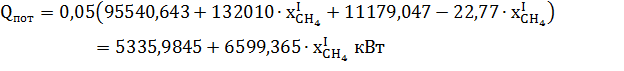
Для веществ на выходе из 2 го реактора при T = 1323К теплоёмкости из:
Вещество. | сp, кДж/(кмоль· К). |
CH4 | 73,4964. |
H2O. | 41,2754. |
CO. | 32,6733. |
H2 | 30,7384. |
N2 | 32,3635. |
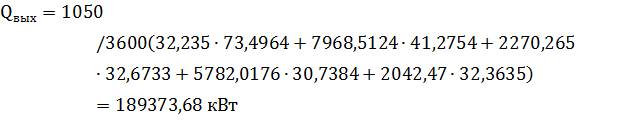
Найдём.
 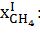 Приход. | кВт. | %. | Расход. | кВт. | %. |
Теплота входящая. | 11 193,459. | 48,8373. | Теплота выходящая. | 189 373,68. | 95,21. |
Теплота реакций. | 11 727,494. | 51,1627. | Потери. | 9525,9213. | 4,79. |
Итого. | 22 920,953. | Итого. | 198 899,6013. |
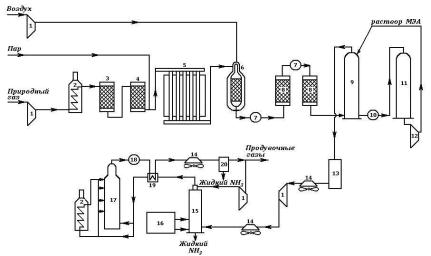
3. Функциональная схема производства аммиака.
1. Очистка природного газа от серосодержащих соединений, гидрированием и адсорбцией образующегося сероводорода:
H2S + ZnO = ZnS +Н2O.
1. Конверсия метана с водяным паром.
СН4 + Н2О = СО + ЗН2;
СО + Н2O = СО2 + Н2.
2. Конверсия оксида углерода с водяным паром (так как в предыдущем процессе оксид углерода СО не полностью превращается в СO2):
СО + Н2O = СO2 + Н2.
Достигается максимально возможного извлечения водорода из исходного сырья.
- 3. Получение азота N2 — второго исходного компонента для синтеза аммиака, который получают из воздуха путем «выжигания» из него кислорода:
- 3O2 + 2СН4 = 2СО + 4Н2O или O2 + 2Н2 = 2Н2O
Это не только простой способ, но и энергосберегающий, так как сжигание части природного газа все равно необходимо для обеспечения теплотой всего процесса.
4. Абсорбция диоксида углерода — удаление СО. Его поглощают раствором моноэтаноламина:
СO2 + 2RNH2 + Н2O = (RNH3)2CO3.
5. Очистка газа после конверсии от оксида углерода СО. Его удаляют, превращая в безвредный метан:
СО + 3Н2 = СН4 + Н2О.
- 6. Синтез аммиака:
- 3H2+N2=2NH3.
Двухступенчатая система конверсии аммиака Двухступенчатая система позволяет повысить степень превращения метана. Так как реакция метана с водой — эндотермическая, то повышение температуры повышает скорость реакции. Температура, необходимая для полного превращения в процессе — 1300 К [1]. Материал из которого сделаны части реактора не позволяют использовать его при таких высоких температурах. Поэтому необходима вторая ступень конверсии, которая проходит в адиабатическом реакторе, со стенками высотемпературного материала — бетоном. Это позволяет повысить температуру внутри реактора и добиться почти полной степени превращения метана.
Еще одна причина, это использование шахтного конвертора, как дополнительную систему для выделения азота. Так же теплота сгорания воздуха, из которого выделяется азот, расходуется для получения водорода из метана.
Можно сделать вывод, что двухступенчатая система позволяет добиться почти полного превращения метана, снизить тепловые расходы и избежать конструирования отдельной системы для получения элементарного азота.
Каталитические химические реакторы, используемые в синтезе аммиака Однослойный реактор с неподвижным слоем зернистого поглотителя для очистки природного газа от серосодержащих соединений. На кобальто-молибденовом катализаторе происходит гидрирование серосодержащих соединений до сероводорода, далее он поглощается в однослойном абсорбере с неподвижным слоем ZnS.
Трубчатый реактор для конверсии природного газа и воды, состоит из труб, в которых находится катализатор.
Шахтный конвектор метана (адиабатический реактор), позволяющий повышать температуру газовой смеси. Стенки сделаны из бетона для повышения температуры внутри реактора и почти полной степени превращения метана.
Радиальный конвертор оксида углерода. Катализатор располагают в корзинах, образованных центральной трубой и наружной обечайкой. Сырье вводят и продукты отводят по кольцевому каналу между корпусом реактора и катализаторной корзиной.
Синтез аммиака должен проходить при отводе тепла, для достижения оптимальной температуры процесса, это обеспечивается в многослойном реакторе с промежуточным теплообменом (а) или в трубчатом реакторе с охлаждением (б).
Структурная схема производства аммиака.
- 1 — колонна (реактор) синтеза NH3
- 2, 3, 13 — теплообменники
- 4 — воздушный холодильник
- 5 — сепаратор
- 6 — сборник аммиака
- 7 — циркуляционный компрессор
- 8 — конденсационная колонна
- 9 — испаритель
- 10 — реактор метанирования СО
- 11 — абсорбер
- 12 — реактор коверсии СО с медьсодержащим катализатором
- 14 — реактор с железохромовым катализатором
- 15 — шахтный конвертор
- 16 — трубчатая печь
- 17 — компрессор
- 18 — реактор очистки природного газа от серосодержащих соединений
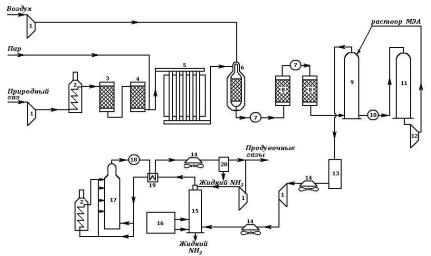
- 1-компрессоры;
- 2-подогреватели;
- 3-реактор гидрирования сероорганических соединений;
- 4-адсорбер H2S;
- 5-трубчатая печь (первичный риформинг);
- 6-шахтный конвертор (вторичный риформинг);
- 7-паровые котлы;
- 8-конверторы СО;
- 9-абсорбер СО2;
- 10-кипятильник;
- 11 — регенератор раствора моноэтаноламина;
- 12-насос;
- 13-аппарат для гидрирования остаточных СО и СО2;
- 14-воздушные холодильники;
- 15-конденсационная колонна;
- 16-испаритель жидкого NH3 (для охлаждения газа и выделения NH3);
- 17-колонна синтеза NН3;
- 18-водоподогреватель;
- 19-теплообменник;
- 20-сепаратор
Конверсия оксида углерода Конверсия оксида углерода водяным паром одна из важнейших технологических стадий в производстве аммиака. Это каталитически процесс с обратимой экзотермической реакцией:
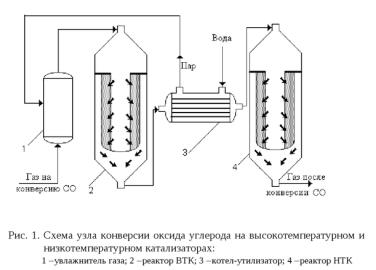
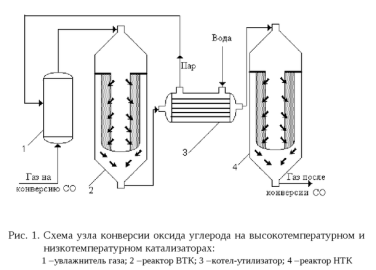
СО + Н2O = СO2 + Н2 +42,2 кДж Практическая реализация оптимального температурного режима предусматривает осуществление конверсии оксида углерода в два этапа, на двух слоях катализаторов — высокотемпературном (ВКТ) и низкотемпературном (НКТ) — с промежуточным охлаждением между ними (рис 1.).

На первом этапе конверсию СО проводят на ВКТ, активном в области температур 600−700К. Реакцию проводят при избытке водяного пара, что увеличивает равновесную степень и скорость превращения оксида углерода. После ВКТ парогазовая смесь, содержащая 4−5 об.% оксида углерода поступает на второй этап конверсии, которая осуществляется на НТК при температурах 480−530К. Перед подачей в реактор низкотемпературной конверсии СО парогазовую смесь необходимо охладить. Охлаждение происходит путем пропускания нагретого потока через котел-утилизатор с получением технологического пара, после чего с температурой 493К парогазовая смесь поступает на низкотемпературную конверсию. На НТК осуществляется дальнейшее превращение оксида углерода. Остаточное содержание СО после НТК должно быть не более 0,15−0,5 об.%.
Равновесие реакции:
СО + Н2O = СO2 + Н2
Определяется уравнением.
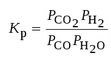
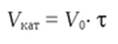

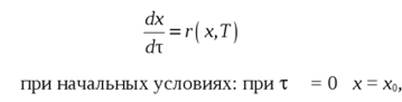

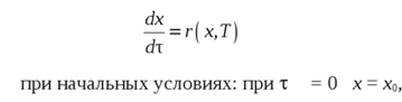


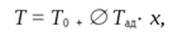

конверсия метан тепловой аммиак Список использованной литературы.
- 1. Бесков В. С. Общая химическая технология: Учебник для вузов. — М.: ИКЦ «Академкнига», 2005. — 452 с.
- 2. Атрощенко В. И. Технология связанного азота. — Киев: «Вища школа», 1985. — 327 с.
- 3. Равдель А. А., Пономарева А. М. Краткий справочник физико-химических величин. — СПб: «Иван Федоров», 2003. -240 с.
- 4. Кутепов А. М., Бондарева Т. И., Беренгартен М. Г. Общая химическая технология: Учебник для вузов. — М.: ИКЦ «Академкнига», 2003. — 528 с.