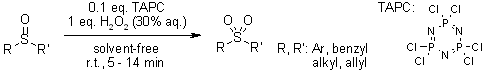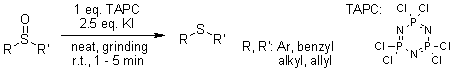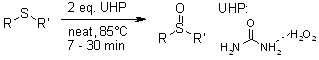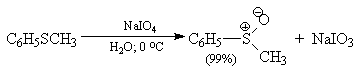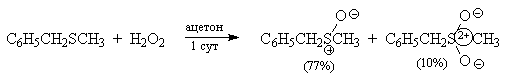Сульфоксиды получают в основном окислением соответствующих сульфидов. Окислителями могут выступать: гидропероксид в кислой среде, оксиды азота, гипохлориты и некоторые другие окислители.
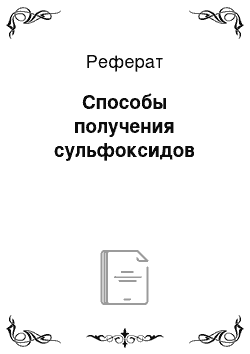
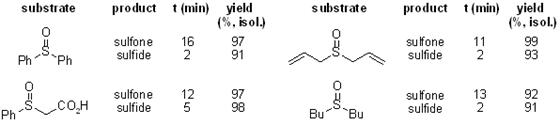
ТАРС (1,3,5-триазо2,4,6-трифосфо 2,2,4,4,6,6гексахлорид) Тарс обеспечивает высокую селективность реакции и ее высокую скорость[28].
UHP пероксид мочевины [29].
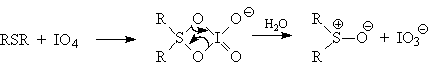
Среди огромного количества разнообразных окислителей наилучшие результаты для превращения сульфидов в сульфоксиды достигаются при использовании метапериодата натрия (NaIO4), мета-хлорпербензойной кислоты и третбутилгипохлорита. Среди них наиболее широко применяется 0,5 М водный раствор метапериодата натрия. Этот реагент обеспечивает очень высокую селективность окисления сульфидов до сульфоксидов практически без примеси сульфона и других побочных продуктов, если окисление проводится при 0 oС в бинарной системе вода — органический растворитель (метанол, диоксан, ацетонитрил) Механизм окисления сульфидов периодатом, по-видимому, аналогичен механизму расщепления 1,2-гликолей и включает циклический интермедиат:
Способ окисления сульфидов до сульфоксидов 30%-м водным пероксидом водорода в уксусной кислоте или ацетоне при 20 °C постепенно утрачивает свое значение в лабораторной практике, так как наряду с сульфоксидом, как правило, образуется некоторое количество сульфона:
[30].