Первая в мире электростанция, использующая для выработки электричества явление осмоса, открылась 24 ноября 2009 года в Норвегии. Солёная морская и пресная вода на электростанции разделены мембраной; так как концентрация солей в морской воде выше, между солёной и пресной водой развивается явление осмоса, в результате чего давление солёной воды самопроизвольно возрастает. Так как давление солёной воды подвергшейся осмосу больше, чем атмосферное давление, возникает мощный поток воды, который и приводит в действие гидротурбину, вырабатывающую энергию.
Осмотическое давление неэлектролитов
Закон Вант-Гоффа
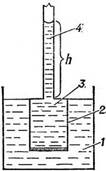
Схема осмометра: 1— вода; 2 — целлофановый мешочек (полупроницаемый); 3 — раствор; 4 — стеклянная трубка; h — высота столбика жидкости (мера осмотического давления).
Осмотическое давление — давление на раствор, отделенный от чистого растворителя мембраной, проницаемой только для молекул растворителя (полупроницаемая мембрана), при котором прекращается осмос. Измерение осмотического давления производят при помощи осмометров. Схема простейшего осмометра показана на рисунке.
В качестве полупроницаемых мембран применяют пленки из целлофана, коллодия и др.
Осмотическое давление разбавленных растворов неэлектролитов при постоянной температуре пропорционально молярной концентрации раствора, а при постоянной концентрации — абсолютной температуре. Растворы, обладающие равными осмотическим давлением, называют изотоническими. Раствор с большим осмотическим давлением называют гипертоническим, а с меньшим — гипотоническим.
Для разбавленных растворов неэлектролитов зависимость осмотического давления от концентрации и температуры раствора выражается уравнением Вант-Гоффа:
р = сВ RT,.
где р — осмотическое давление раствора, кПа; сВ — его молярная концентрация, моль/л; R — универсальная газовая постоянная, 8,314 Дж/(моль· К); Т — абсолютная температура раствора.

