Характеристика комплексных соединений никеля

Никель характеризуется высокой коррозионной стойкостью — устойчив на воздухе, в воде, в щелочах, в ряде кислот. Химическая стойкость обусловлена его склонностью к пассивированию — образованию на его поверхности плотной оксидной пленки, обладающей защитным действием. Никель активно растворяется в азотной кислоте. Известно ограниченное число соединений одновалентного никеля, при этом большинство… Читать ещё >
Характеристика комплексных соединений никеля (реферат, курсовая, диплом, контрольная)
Атомы никеля имеют внешнюю электронную конфигурацию 3d84s2. Наиболее устойчивым для никеля является состояние окисления Ni (II).
Соединение одновалентного никеля.
Известно ограниченное число соединений одновалентного никеля, при этом большинство из них неустойчивы, легко выветриваются на воздухе; соединения окрашены в желтый, красный, зеленый, и синий цвета, получают восстановлением соединений никеля (II). Примеры соединений никеля (I):
- — окись Ni2O — оранжево — желтая,
- — гидроокись NiOH — - синяя,
- — цианид NiCN — оранжевый,
- — сульфид Ni2S — желтый,
- — селенид Ni2Se — желтый.
Комплексы:
- — K2[NiCl3] - красный,
- — Na2[Ni (CN)3] - красный,
- — K3[Ni (CN)3] - красный,
- — K2[Ni (NO)(CN)3] - красный,
- — [Ni (NO)SC2H5] - красный.
Никель образует соединения со степенью окисления +2 и +3. При этом никель со степенью окисления +3 только в виде комплексных солей. Для соединений никеля +2 известно большое количество обычных и комплексных соединений. Оксид никеля Ni2O3 является сильным окислителем.
Никель характеризуется высокой коррозионной стойкостью — устойчив на воздухе, в воде, в щелочах, в ряде кислот. Химическая стойкость обусловлена его склонностью к пассивированию — образованию на его поверхности плотной оксидной пленки, обладающей защитным действием. Никель активно растворяется в азотной кислоте.
С оксидом углерода CO никель легко образует летучий и весьма ядовитый карбонил Ni (CO)4.
Тонкодисперсный порошок никеля пирофорный (самовоспламеняется на воздухе).
Никель горит только в виде порошка. Образует два оксида NiO и Ni2O3 и соответственно два гидроксида Ni (OH)2и Ni (OH)3. Важнейшие растворимые соли никеля — ацетат, хлорид, нитрат и сульфат. Растворы окрашены обычно в зеленый цвет, а безводные соли — желтые или коричнево-желтые. К нерастворимым солям относятся оксалат и фосфат (зеленые), три сульфида NiS (черный), Ni2S3 (желтовато-бронзовый) и Ni3S4 (черный). Никель также образует многочисленные координационные и комплексные соединения. Например, диметилглиоксимат никеля Ni (C4H6N2O2)2, дающий четкую красную окраску в кислой среде, широко используется в качественном анализе для обнаружения никеля.
Водные растворы солей никеля (II) содержат ион гексаакваникеля (II) [Ni (H2O)6]2+. При добавлении к раствору, содержащему эти ионы, аммиачного раствора происходит осаждение гидроксида никеля (II), зеленого желатинообразного вещества. Этот осадок растворяется при добавлении избыточного количества аммиака вследствие образования ионов гексамминникеля (II) [Ni (NH3)6]2+.
Протекает следующая реакция:
NiSO4+ 2NH4OH= Ni (OH)2+ (NH4)SO4.
Ni (OH)2+ 6NH4OH= [Ni (NH3)6]2+ + 2OH- +6H2O.
Никель образует комплексы с тетраэдрической и с плоской квадратной структурой. Например, комплекс тетрахлороникелат (II) [NiCl4]2- имеет тетраэдрическую структуру, а комплекс тетрацианоникелат (II) [Ni (CN)4]2-имеет плоскую квадратную структуру.
В качественном и количественном анализе для обнаружения ионов никеля (II) используется щелочной раствор бутандиондиоксима, известного также под названием диметилглиоксима. При его взаимодействии с ионами никеля (II) образуется красное координационное соединение бис (бутандиондиоксимато)никель (II). Это — хелатное соединение и бутандиондиоксимато-лиганд является бидентатным.
Для никеля наиболее характерны цианидные комплексы. Их основными представителями являются K4[Ni2(CN)6] и K4[Ni (CN)4]. Лучше изучен цианид состава K4[Ni2(CN)6], который в водной щелочной среде довольно устойчив, но в кислой среде из раствора осаждается оранжевый NiCN. В водном растворе K4[Ni2(CN)6] способен присоединять оксид углерода (II), при этом образуется неоднородное комплексное соединение K4[Ni2(CN)6(CO)2], имеющее желтый цвет. В щелочных растворах оно, также как и K4[Ni2(CN)6], довольно устойчиво, но в кислых распадается на K2[Ni (CN)4] и Ni (CO)4.
Так, катион Ni2+ с аммиаком образует гексаамминовый комплекс [Ni (NH3)6]2+ и диакватетраамминовый комплекс [Ni (NH3)4(Н2О)2]2+. Эти комплексы с анионами образуют синие или фиолетовые соединения.
При действии фтора F2 на смесь NiCl2 и КСl возникают комплексные соединения, содержащие никель в высоких степенях окисления: +3 — (K3[NiF6]) и +4 — (K2[NiF6]).
Порошок никеля реагирует с оксидом углерода (II) СО, причем образуется легко летучий тетракарбонил Ni (CO)4, который находит большое практическое применение при нанесении никелевых покрытий, приготовлении высокочистого дисперсного никеля и т. д.
Действие монооксида углерода под давлением на порошок никеля:
.
Химические свойства.
Разлагается при нагревании:
.
Реагирует с концентрированными кислотами:
.
.
Во влажных условиях медленно окисляется:
.
Окисляется кислородом при нагревании:
.
Карбонил никеля [Ni (CO)4] — очень ядовит. Предельно допустимая концентрация его паров в воздухе производственных помещений 0.0005 мг/мі.
Олигомеризация.
Реакции этилена, приводящие к образованию димеров, олигомеров и полимеров этилена представляют существенный интерес для химической промышленности. Эти реакции могут приводить к образованию линейных, разветвленных или циклических соединений.
Комплексы никеля являются самыми распространенными катализаторами олигомеризации олефинов и проявляют наибольшую активность и селективность по отношению к олефинам. Никелевые катализаторы можно разделить на две группы: соединения никеля (П) в сочетании с алкильными или гидридными производными металлов основной группы (катализаторы Циглера-Натта) и металлоорганические комплексы, которые служат предшественниками каталитических комплексов.
Ниже показан путь протекания реакции внедрения этилена, включающий стадию появления свободного координационного места в результате акта внедрения этилена.
Рис. 1.
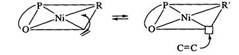
Рост цепи протекает в трансположении относительно атома кислорода комплекса, в то время как свободные координационные места для входящей молекулы мономера после внедрения этилена возникают в трансположения по отношению к атому фосфора.
Все комплексы, активные в реакции линейного присоединения по связи С-С, состоят из хелата и органического лиганда. Органическая часть только стабилизирует комплекс, тогда как хелатный лиганд регулирует каталитическую активность и селективность.
Рис. 2.
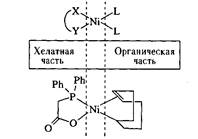
Применение.
Сплавы.
Никель является основой большинства суперсплавов — жаропрочных материалов, применяемых в аэрокосмической промышленности для деталей силовых установок.
- * монель-металл (65 — 67% Ni + 30 — 32% Cu + 1% Mn), жаростойкий до 500 °C, очень коррозионно-устойчив;
- * белое золото (например 585 пробы содержит 58,5% золота и сплав (лигатуру) из серебра и никеля (или палладия));
- * нихром, сплав сопротивления (60% Ni + 40% Cr);
- * пермаллой (76% Ni + 17%Fe + 5% Cu + 2% Cr), обладает высокой магнитной восприимчивостью при очень малых потерях на гистерезис;
- * инвар (65% Fe + 35% Ni), почти не удлиняется при нагревании;
- * Кроме того, к сплавам никеля относятся никелевые и хромоникелевые стали, нейзильбер и различные сплавы сопротивления типа константана, никелина и манганина.
Никелирование.
Никелирование — создание никелевого покрытия на поверхности другого металла с целью предохранения его от коррозии. Проводится гальваническим способом с использованием электролитов, содержащих сульфат никеля (II), хлорид натрия, гидроксид бора, поверхностно-активные и глянцующие вещества, и растворимых никелевых анодов. Толщина получаемого никелевого слоя составляет 12 — 36 мкм. Устойчивость блеска поверхности может быть обеспечена последующим хромированием (толщина слоя хрома 0,3 мкм).
Бестоковое никелирование проводится в растворе смеси хлорида никеля (II) и гипофосфита натрия в присутствии цитрата натрия:
никелевый этилен монооксид димер
NiCl2 + NaH2PO2 + H2O = Ni + NaH2PO3 + 2HCl.
Процесс проводят при рН 4—6 и 95 °C.
Производство аккумуляторов.
Производство железо-никелевых, никель-кадмиевых, никель-цинковых, никель-водородных аккумуляторов.
Радиационные технологии.
Нуклид 63Ni, излучающий в±частицы, имеет период полураспада 100,1 года и применяется в крайтронах.
Медицина.
Применяется при изготовлении брекет-систем (никелид титана).
Протезирование.
Монетное дело.
Никель широко применяется при производстве монет во многих странах. В США монета достоинством в 5 центов носит разговорное название «никель».