Эквивалент, закон эквивалентов.
Определение эквивалента кислоты, основания, соли, простых газободибних веществ, окислителя, восстановителя

Эквивалент, как частица, может быть охарактеризован молярной массой (молярным объемом) и определенным количеством вещества nэ. Молярная масса эквивалента (МЭ) — это масса одного моль эквивалента. Она равна произведению молярной массы вещества на фактор эквивалентности: Из закона эквивалентов следует, что массы (или объемы) реагирующих и образующихся веществ пропорциональны молярным массам… Читать ещё >
Эквивалент, закон эквивалентов. Определение эквивалента кислоты, основания, соли, простых газободибних веществ, окислителя, восстановителя (реферат, курсовая, диплом, контрольная)
Эквивалент — это реальная или условная частица, которая в кислотно-основных реакциях присоединяет (или отдает) один ион Н+ или ОН-, в окислительно-восстановительных реакциях принимает (или отдает) один электрон, реагирует с одним атомом водорода или с одним эквивалентом другого вещества. Например, рассмотрим следующую реакцию:
H3PO4 + 2KOH =K2HPO4 + 2H2O.
В ходе этой реакции только два атома водорода замещаются на атомы калия, иначе, в реакцию вступают два иона Н+ (кислота проявляет основность 2). Тогда по определению эквивалентом H3PO4 будет являться условная частица ½H3PO4, т.к. если одна молекула H3PO4 предоставляет два иона Н+, то один ион Н+ дает половина молекулы H3PO4. С другой стороны, на реакцию с одной молекулой ортофосфорной кислотой щелочь отдает два иона ОН-, следовательно, один ион ОНпотребуется на взаимодействие с ½ молекулы кислоты. Эквивалентом кислоты является условная частица ½Н3РО4, а эквивалентом щелочи частица КОН. Число, показывающее, какая часть молекулы или другой частицы вещества соответствует эквиваленту, называется фактором эквивалентности (fЭ). Фактор эквивалентности — это безразмерная величина, которая меньше, либо равна 1. Формулы расчета фактора эквивалентности приведены в таблице. Таким образом, сочетая фактор эквивалентности и формульную единицу вещества, можно составить формулу эквивалента какой-либо частицы, где фактор эквивалентности записывается как химический коэффициент перед формулой частицы.
Следует учитывать, что эквивалент одного и того же вещества может меняться в зависимости от того, в какую реакцию оно вступает. Эквивалент элемента также может быть различным в зависимости от вида соединения, в состав которого он входит. Эквивалентом может являться как сама молекула или какая-либо другая формульная единица вещества, так и ее часть.
Таблица 1 Расчет фактора эквивалентности
Частица. | Фактор эквивалентности. | Примеры. |
Элемент. | 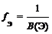 . где В (Э) — валентность элемента. | |
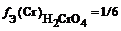 Простое вещество. | 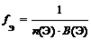 . где n (Э) — число атомов элемента (индекс в химической формуле), В (Э) — валентность элемента. | fЭ (H2) = 1/(2?1) = ½; fЭ (O2) = 1/(2?2) = ¼; fЭ (Cl2) = 1/(2?1) = ½; fЭ (O3) = 1/(3?2) = 1/6. |
Оксид. | 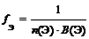 . где n (Э) — число атомов элемента (индекс в химической формуле оксида), В (Э) — валентность элемента. | fЭ (Cr2O3) = 1/(2?3) = 1/6; fЭ (CrO) = 1/(1?2) = ½; fЭ (H2O) = 1/(2?1) = ½; fЭ (P2O5) = 1/(2?5) = 1/10. |
Кислота. | 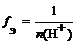 . где n (H+) — число отданных в ходе реакции ионов водорода (основность кислоты). | fЭ (H2SO4) = 1/1 = 1 (основность равна 1). или. fЭ (H2SO4) = ½. (основность равна 2). |
Основание. | 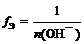 . где n (ОH-) — число отданных в ходе реакции гидроксид-ионов (кислотность основания). | fЭ (Cu (OH)2) = 1/1 = 1 (кислотность равна 1) или. fЭ (Cu (OH)2) = ½. (кислотность равна 2). |
Соль. | 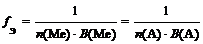 . где n (Ме) — число атомов металла (индекс в химической формуле соли), В (Ме) — валентность металла; n (А) — число кислотных остатков, В (А) — валентность кислотного остатка. | fЭ (Cr2(SO4)3) = 1/(2?3) = 1/6 (расчет по металлу) или. fЭ (Cr2(SO4)3) = 1/(3?2) = 1/6 (расчет по кислотному остатку). |
Частица в окислительно-восстановительных реакциях. | 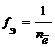 . где — число электронов, участвующих в процессе окисления или восстановления. | Fe2+ + 2 Fe0. fЭ (Fe2+) =½; MnO4- + 8H+ + 5 Mn2+ + 4H2O. fЭ (MnO4-) = 1/5. |
Ион. | 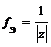 . где z — заряд иона. | fЭ (SO42-) = ½. |
Пример. Определите фактор эквивалентности и эквивалент у солей: а) ZnCl2, б) КНСО3, в) (MgOH)2SO4. Решение: Для расчетов воспользуемся формулами, приведенными в таблице.
а) ZnCl2 (средняя соль):
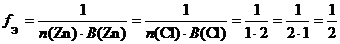
.
fЭ (ZnCl2) = ½, поэтому эквивалентом ZnCl2 является частица ½ZnCl2.
б) КНСО3 (кислая соль):
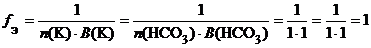
.
fЭ (КНСО3) = 1, поэтому эквивалентом КНСО3 является частица КНСО3.
в) (MgOH)2SO4 (основная соль):
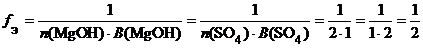
.
fЭ ((MgOH)2SO4) = ½, поэтому эквивалентом (MgOH)2SO4 является частица ½(MgOH)2SO4.
Эквивалент, как частица, может быть охарактеризован молярной массой (молярным объемом) и определенным количеством вещества nэ. Молярная масса эквивалента (МЭ) — это масса одного моль эквивалента. Она равна произведению молярной массы вещества на фактор эквивалентности:
МЭ = МЧfЭ.
Молярная масса эквивалента имеет размерность «г/моль».
Молярная масса эквивалента сложного вещества равна сумме молярных масс эквивалентов образующих его составных частей, например:
МЭ (оксида) = МЭ (элемента) + МЭ (О) = МЭ (элемента) + 8.
МЭ (кислоты) = МЭ (Н) + МЭ (кислотного остатка) = 1 + МЭ (кислотного остатка) МЭ (основания) = МЭ (Ме) + МЭ (ОН) = МЭ (Ме) + 17.
МЭ (соли) = МЭ (Ме) + МЭ (кислотного остатка).
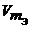
Газообразные вещества помимо молярной массы эквивалента имеют молярный объем эквивалента (или VЭ) — объем, занимаемый молярной массой эквивалента или объем одного моль эквивалента. Размерность «л/моль». При н.у. получаем:
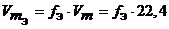
Закон эквивалентов был открыт в 1792 г. И. Рихтером. Современная формулировка закона: вещества реагируют и образуются согласно их эквивалентам. Все вещества в уравнении реакции связаны законом эквивалентов, поэтому:
nэ (реагента1) = … = nэ (реагентаn) = nэ (продукта1) = … = nэ (продуктаn).
Из закона эквивалентов следует, что массы (или объемы) реагирующих и образующихся веществ пропорциональны молярным массам (молярным объемам) их эквивалентов. Для любых двух веществ, связанных законом эквивалентов, можно записать:
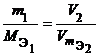
где m1 и m2 — массы реагентов и (или) продуктов реакции, г;
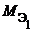
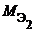
— молярные массы эквивалентов реагентов и (или) продуктов реакции, г/моль;
V1, V2 — объемы реагентов и (или) продуктов реакции, л;
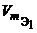
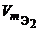
— молярные объемы эквивалентов реагентов, л/моль.