Расчет показателей качества воды для установки обратного осмоса

Фактическая концентрация углекислоты определяется из уравнения диссоциации по первой ступени: Н2СО3 НСО3— + Н+ по закону действующих масс в формуле (1), откуда. Для нашего случая м=47,149Ч10−3; гI=0,897; гII=0,648. Равновесная концентрация углекислоты определяется равновесием следующих химических реакций: В данном случае могут быть использованы следующие выражения для расчета средних значений… Читать ещё >
Расчет показателей качества воды для установки обратного осмоса (реферат, курсовая, диплом, контрольная)
Исходная вода
Исходной обычно служит природная вода, примерный химический состав примесей которой приведен в табл. 4. В качестве примера взята вода поступающая на химводоочистку расходом 300 м3/ч.
вода осмос осветление катионитный Таблица 4. Химический состав примесей воды
Показатель. | Жесткость, мг-экв/л. | Концентрация ионов, мг/л. | Що,. мг-экв/л. | Ок, мгО/л. | |||||||
Жо | ЖСа | Na++K+ | SO42- | Cl- | NO3- | SiO22- | ГДП. | ||||
Численное значение. | 6,48. | 5,1. | 6,9. | 93,2. | 25,5. | ; | ; | ; | 4,34. | 8,5. | |
Проверка анализа исходной воды выполняется по уравнению электронейтральности:
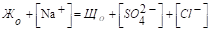
.
- 6,48 + 6,9/23=4,43 + 93,2/48 +7,1/35,5
- 6,78?6,48.
Ошибка химического анализа должна быть не более 2% и в данном случае составляет:

=4,4% > 2%.
Так как сумма катионов больше суммы анионов, то корректируем.
Жо + [Na+] = Що + [ + [Cl-].
6,48 + 6,9/23 = 4,34 + 107,52/48 + 7,1/35,5
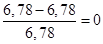
Ош==0%<2%.
ЖCa2+=[Сa2+].
Жо=[Сa2+]+[Mg2+]= ЖCa2++ ЖMg2+ => [Mg2+]= ЖMg2+ = Жо— ЖCa2+=1,38 мг (экв)/л.
[HCO3- ]=Що= Жк=4,34 мг (экв)/л Жо=Жк+Жнк => Жнк= Жо— Жк=2,14 мг (экв)/л Для дальнейших расчетов данные табл. 4 следует переписать с пересчетом концентраций ионов в мг-экв/л и моль/л (см. табл. 5).
Расчет характеристики «стабильность» воды производится сравнением равновесной и фактической концентрации углекислоты в воде. Поскольку значения рН исходной воды не задано, принимаем рН=7. Для определения активностей ионов в воде найдем ионную силу (м) и коэффициенты активности гI и гII.
=0,5(Сi zi2)=0,5([Ca2+](Z Ca2+)2+ [Mg2+](Z Mg2+)2+[Na+](Z Na+)2+[SO42-](Z SO2-)2+[Cl-](Z Cl-)2 +[HCO3-](Z HCO-)2)=0,5(2,55Ч22+0,69Ч22+0,3Ч12+0,97Ч22+0,2Ч12+4,34Ч12)=10,84Ч10-3
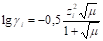
.
где, Сi — концентрации ионов, моль/л; z — заряд i-го иона.
Для нашего случая м=47,149Ч10-3; гI=0,897; гII=0,648. Равновесная концентрация углекислоты определяется равновесием следующих химических реакций:
Н2СО3 НСО3— + Н+,.
НСО3— СО32- + Н+,.
СО32- + Ca2+ CaСО3 v (тв).

.
pH=7; ан+=10-7
Равновесная концентрация углекислоты равна:

моль/л где КI и КII — константы диссоциации углекислоты по I и II ступеням; - произведение растворимости СaCO3; , — концентрации ионов кальция и бикарбонатов, моль/л.
Фактическая концентрация углекислоты определяется из уравнения диссоциации по первой ступени: Н2СО3 НСО3— + Н+ по закону действующих масс в формуле (1), откуда.
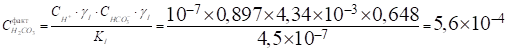
моль/л (1).
Таблица 5. Пересчет концентраций ионных примесей воды по табл.4
Показатель. | Концентрация ионов, мг-экв/л. | |||||||
Ca2+ | Mg2+ | Na++K+ | SO42- | Cl- | HCO3- | SiO22- | ||
Концентрации:
|
|
|
|
|
|
|
| |
Для нашего случая: = 5,565моль/л;
= моль/л.
Таким образом, исходная вода — агрессивная, т.к. < .
Расчет удельной электропроводности исходной воды может быть выполнен по методике, приведенной в книге Чебанова С. Н., Ларина Б. М. «Водоподготовка и водный режим тепловых электростанций», гл. 20, с. 321 — 322.
В данном случае могут быть использованы следующие выражения для расчета средних значений эквивалентных электропроводностей:
Ом-1· см-1·экв-1;
Ом-1· см1·экв-1;
Ом-1· см-1·экв-1;
где М=УKt=УAn=4,42 — минерализация воды, мг-экв/л;
Кt = 1+0,024(t-18 °С)=1+0,024•(25?18)=1,168 — температурный коэффициент электропроводности при температуре раствора t єС.
Тогда удельная электропроводность (ч, мкСм/см) определяется так:
Где и — концентрации хлоридов и сульфатов, мг-экв/л.
В рассматриваемом примере имеем:
; Ом-1· см-1·экв-1; Ом-1· см-1·экв-1;
Ом-1· см-1·экв-1.
Удельная электропроводность воды:
мкСм/см.