Результаты исследования и их обсуждение

После 6 часов повышения ВБД почти у всех животных регистрировалась синусная брадикардия. ЧСС снизилась с 409±17 до 349±10 уд/мин (r=0,81, р<0,05). Длительность интервалов P-Q, QRS, Q-T не менялась. Но было отмечено, что интервал S-T был выше изолинии у большинства животных (60%). Регистрация ЭКГ через 12 часов после воспроизведения ВБД выявила аналогичные изменения как у животных через 6 часов… Читать ещё >
Результаты исследования и их обсуждение (реферат, курсовая, диплом, контрольная)
1. Влияние внутрибрюшной гипертензии на жизненно важные органы и системы экспериментальных животных.
Для изучения патофизиологических и морфологических изменений, происходящих при высоком уровне ВБД (25 мм рт. ст.), нами была проведена серия опытов на малых лабораторных животных.
После 6 часов повышения ВБД почти у всех животных регистрировалась синусная брадикардия. ЧСС снизилась с 409±17 до 349±10 уд/мин (r=0,81, р<0,05). Длительность интервалов P-Q, QRS, Q-T не менялась. Но было отмечено, что интервал S-T был выше изолинии у большинства животных (60%). Регистрация ЭКГ через 12 часов после воспроизведения ВБД выявила аналогичные изменения как у животных через 6 часов, но они носили более выраженный характер. Наблюдалось дальнейшее усиление брадикардии. Так, ЧСС снизилась по сравнению с исходной на 21% и составляла 325±12 уд/мин (r=0,94, р<0,001). У части животных регистрировалась синусовая аритмия. У животных через 24 часа на ЭКГ заметна тенденция к урежению частоты сердечных сокращений до 263±12 уд/мин (r=0,81, р<0,05), возникновению сначала синусовой аритмии, а затем и появлению эктопических очагов возбуждения (экстрасистолия), изменение высоты зубцов, элевация сегмента S-T, изменение конфигурации зубца Т во II-м и III-м отведениях, сходное с т.н. «спиной кошки».
Полученные данные свидетельствуют, что при повышении ВБД до высоких цифр частота сердечных сокращений уряжается. Это может свидетельствовать о возникновении гипертензии, в связи с возросшим сосудистым сопротивлением и вследствие сдавления сосудистого русла под влиянием повышенного ВБД. Появление аритмии, изменения высоты зубцов и конфигурации зубца Т говорят об ишемии миокарда, преимущественно его задней стенки, нарушениях процессов реполяризации и функции проводимости. Надо отметить, что эти сдвиги нарастали с увеличением срока воздействия повышенного ВБД.
При анализе изменений функции дыхания было установлено, что у крыс при моделировании ВБГ в течении 6 часов ЧД снизилась с 193±15 до 165±10 дыхательных движений/мин (r=0,82, р<0,05), через 12 часов ЧД снизилась до 138±12 в мин, а к концу опыта — 114±11 в мин. При этом к концу опыта отмечалось достоверное снижение амплитуды глубины дыхания.
Повышение ВБД вызывало замедление свертывания крови, снижение вязкости и плотности сгустка, которые были выражены через сутки эксперимента. Вместе с тем, вязкость крови имела тенденцию к повышению. Сдвиги можно объяснить развивающийся гипоксией, которая вызывала существенные изменения в организме, обусловившие гипокоагуляционные сдвиги крови, что приводит к геморрагическим нарушениям, с развитием тромбогеморрагического синдрома.
Изучение содержания электролитов в органах и тканях показало, что в ранние сроки после повышения ВБД наибольшие изменения регистрируются в тех органах и тканях, которые непосредственно подвергаются воздействию повышенного давления. Это кишечник, печень и почки. Причем, при этом снижается как уровень натрия, так и калия, что свидетельствует о нарушении проницаемости мембран клеток в этих тканях. Наряду с этим, наблюдалась потеря натрия сердечной мышц. О том, что имеющиеся сдвиги существенны, свидетельствовали статистически значимые изменения K+/Na+ коэффициента во всех исследуемых нами органах и тканях.
При морфологическом исследовании органов животных, подвергшихся воздействию ВБГ через 6, 12 и 24 часа в них были выявлены структурные изменения.
Изменения в сердечной мышце, нарастающие к концу опыта и выражались в расстройстве микроциркуляции, признаках ишемии, такие как: потеря поперечной исчерченности, отек интерстиция миокарда, некроз кардиомиоцитов, полнокровие микроциркуляторного русла, диапедезные кровоизлияния. Следует отметить, что данные морфологические изменения были отмечены во всех группах моделирования ВБГ, однако наибольшая их выраженность наблюдалась в IV группе.
В легких при моделировании ВБГ нами были обнаружены патоморфологические изменения и в тканях легкого: в виде скопления жидкости в просветах альвеол и диффузные альвеолярные повреждения, отмечалось полнокровие капилляров межальвеолярных перегородок, венозное полнокровие и интраальвеолярные кровоизлияния. Выявленные изменения нарастали у экспериментальных животных к концу опыта.
В печени при повышении ВБД нами были обнаружены дистрофические изменения паренхимы, признаки расстройства кровообращения в виде венозного застоя, вплоть до кровоизлияний и дистрофические изменения гепатоцитов.
При исследовании тонкой кишки через 6 и 12 часов после повышения ВБГ изменения были не существенны. Через 24 часа наблюдались расстройства регионарного кровообращения в виде полнокровия, кровоизлияний и отека стенки кишка. Вероятно, в основе этих изменений лежит прямое, механическое влияние ВБД на стенки полых органов и портокавальную систему. Это вызвано ухудшением перфузии в результате компрессии магистральных сосудов. Кроме того, компрессия приводит к нарушению микроциркуляции и тромбообразованию, сопровождается ухудшением лимфооттока, приводит к ишемии кишечной стенки с развитием клеточного ацидоза, транссудации жидкости, возникновению отека стенки кишки и выходу форменных элементов крови за пределы сосудистого русла.
В почках наблюдались изменения в виде паренхиматозной дистрофии, отложение солей в просвете канальцев и полнокровие сосудов.
Таким образом, патоморфологические изменения, возникающие в органах при максимальном по длительности и уровню повышении ВБД, подтверждает причинно следственную связь синдрома внутрибрюшной гипертензии с сопровождающимися расстройствами кровообращения, возникновением гипоксии, с формированием полиорганной недостаточности. Следовательно, при острой хирургической патологии живота повышение ВБД является фактором, напрямую связанным с развитием полиорганной недостаточности.
При проведении сравнительного анализа патоморфологических изменений внутренних органов выявленных на вскрытии пациентов с острой интраабдоминальной патологией было установлено, что характер патологических изменений обнаруженных в печени, легких, почках, миокарде и тонкой кишке лабораторных животных, был идентичен изменениям у умерших пациентов.
Таким образом, анализ результатов экспериментальных исследований убедительно доказал, что ВБД негативно влияет на функцию жизненно важных органов и систем организма, способствует развитию тяжелых осложнений и ухудшает прогноз основного заболевания. Сохранение повышенного уровня ВБД в течении 12−24 часов приводит к развитию полиорганной недостаточности и СВБГ, что требует принятия неотложных мер по профилактике и лечению ВБГ у больных экстренными хирургическими заболеваниями и травмами живота.
2. Результаты клинических исследований
У больных экстренными хирургическими заболеваниями и травмами живота в дооперационном периоде повышение внутрибрюшного давления было отмечено в 438 (81,56%) наблюдениях. Внутрибрюшная гипертензия зарегистрирована у 402 (74,86%) пациентов. При этом уровень ВБГ I степени — установлен у 82 (15,27%) больных, II степени — у 143 (26,63%), III степени — у 119 (22,53%) и IV — у 56 (10,43%) больных. Синдром внутрибрюшной гипертензии развился у 83 (15,46%) пациентов.
Распределение больных по степени ВБГ внутри групп представлена на рисунке 1.

Рис. 1 Распределение больных исследуемых групп по степени ВБГ в дооперационном периоде
Анализируя полученные данные, было установлено, что в I группе больных ВБГ отмечалась в 98 (76,92%) наблюдениях. В I «А» подгруппе в 50 (51,02%) наблюдениях, в I «Б» подгруппе в 48 (48,98%) наблюдениях. СВБГ был установлен в 8 (8,16%) и 7 (7,14%) наблюдениях соответственно.
Во II группе больных ВБГ была отмечена у 123 (95,35%) пациентов. При этом у 57 (46,34%) больных была зарегистрирована ВБГ III-IV степени, а СВБГ развился у 14 (11,38%) пациентов из II «А» подгруппы и у 15 (12,2%) пациентов II «Б» подгруппы.
В III группе больных ВБГ регистрировалась в 100% случаев, у 56 (51,85%) больных была установлена I — II степень ВБГ, а у 52 (48,15%) III — IV степень ВБГ. В 12,04% случаев развился СВБГ у больных III «А» подгруппы и в 9,26% случаев у больных III «Б» подгруппы.
У пострадавших IV группы при поступлении ВБГ отмечалась в 43 (51,19%) наблюдениях, которая характеризовалась в 34 (79,07%) случаях ВБГ II — III степени, при этом IV степень ВБГ зарегистрирована не была. СВБГ развивался у 7 (16,28%) пострадавших IV «А» подгруппы и у 7 (16,28%)% пострадавших IV «Б» подгруппы.
В V группе пациентов ВБГ отмечена в 42 (57,53%) наблюдениях, при этом в 34 (80,95%) случаев была установлена ВБГ I — II степени. СВБГ развился у 3 (7,14%) пациентов, как V «А», так и V «Б» подгрупп.
Изучение клинической картины у пациентов с экстренными хирургическими заболеваниями и травмами живота, с повышенным ВБД показало, что клинические симптомы, наблюдающиеся при развитии ВБГ неспецифичны и зависят от выраженности воспалительного процесса в брюшной полости, признаков пареза кишки и количества жидкости в брюшной полости. Анализируя частоту развития признаков перитонеального синдрома, включающего напряжение мышц передней брюшной стенки и симптомов воспаления брюшины, нами было установлено, что частота его проявления в исследуемых группах статистически не значима. Признаки пареза кишечника встречались несколько чаще у больных с IV степенью ВБГ, чем у больных других групп.
Анализ результатов лабораторных исследований не выявил существенных отличий в уровне общего белка, креатинина, мочевины, общего билирубина, электролитов и глюкозы крови. Таким образом, было установлено, что эти «традиционные» лабораторные показатели не являются значимыми в комплексе дифференциальной диагностики степени ВБГ и являются в первую очередь показателями, отражающими степень метаболических нарушений.
Повышение ВБД? 15 мм. рт. ст. приводило к ухудшению спланхнического кровообращения и характеризовалось снижением АПД ниже 85 мм рт. ст., при этом отмечалось снижение pHi ниже 7,32 в сочетании с увеличением Рg-а СО2 (CO2-gap) более 13 мм рт. ст., что свидетельствовало о наличие интрамурального ацидоза и гипоксии слизистой кишечника, тем самым отражало состояние тканевой ишемии, обусловленной выраженной гипоперфузией ЖКТ, нарушением кровообращения в спланхническом бассейне.
Установлено, что рост ВБД замедляет кровоток по нижней полой вене и уменьшает венозный возврат, ограничивает диастолическое заполнение желудочков, способствует повышению ЦВД. При дальнейшем прогрессировании ВБГ отмечалось снижение ударного объема и сердечного выброса, несмотря на компенсаторную тахикардию. Увеличение ОПСС было прямо пропорционально величине ВБГ и было связано с прямым механическим воздействием на сосуды брюшной полости. Среднее артериальное давление (САД) у больных ВБГ снижалось по мере увеличения ВБД. У всех больных с ВБГ выявляли снижение оксигенации крови, нарастающей по мере увеличения уровня ВБД.
При оценке результатов инструментальных методов исследования больных с ВБГ в дооперационном периоде установлена положительная корреляционная связь между уровнем ВБД и количеством жидкости в брюшной полости. Наличие в брюшной полости около 500 мл жидкости в 72% наблюдениях соответствовало ВБГ I степени, 500−1000 мл в 87% наблюдениях соответствовало ВБГ II степени, а 1000 мл и более в 98% наблюдений соответствовало ВБГ III-IV степени.
По мнению большинства авторов, самым достоверным способом диагностики ВБГ является измерение ВБД через мочевой пузырь. Нами был проведен поиск оптимального способа измерения ВБД по следующим критериям: продолжительность процедуры, точность и воспроизводимость метода средним медицинским персоналом, стоимость выполнения процедуры, развитие осложнений (табл. 3).
Таблица 3 Сравнительная оценка способов измерения ВБД.
Критерии оценки. | Измерение внутрибрюшного давления. | ||||
в мочевом пузыре по I. Kron (1989). | в мочевом пузыре по M. Cheatham (1998). | в мочевом пузыре, с помощью закрытой системы Advaiser. | в желудке по. G. Collee (1993). | ||
Число пациентов. | |||||
Продолжительность процедуры, мин. | 4,2±1,2. [2,5−6]. | 2,8±0,9. [2−5]. | 2,1±0,5. [1−4]. | 9,5±2,5. [4−14,5]. | |
Воспроизводимость метода средним медицинским персоналом. | Хорошая. | Хорошая. | Хорошая. | Удовлетвор. | |
Точность. | Низкая. | Высокая. | Высокая. | Высокая. | |
Стоимость выполнения 1 процедуры, руб. | |||||
Осложнения, %. | ; | ; | ; | ; | |
Как видно из представленных в таблице 3 данных, предпочтительным методом измерения внутрибрюшного давления может быть признано измерение давления в мочевом пузыре по M. Cheatham (1998). Этот метод безопасен, непродолжителен по времени, точен и экономически выгоден.
3. Анализ результатов мониторинга ВБД и АПД у больных экстренными хирургическими заболеваниями и травмами живота
Во всех исследуемых группах пациентов нами был проведён анализ результатов мониторирования внутрибрюшного и абдоминального перфузионного давлений (рис. 2 — 9).
В предоперационном периоде, несмотря на предоперационную подготовку у всех больных I группы отмечали ВБГ II степени и снижение уровня АПД до критического (ниже 65 мм рт. ст.). В дальнейшем в первые сутки послеоперационного периода у пациентов I «А» подгруппы отмечалась статистически достоверное снижение ВБД до 12,5±3,1 мм рт. ст. (r=0,83, p<0,05). Отмечалась улучшение показателей АПД — до 78,5±4,2 мм рт. ст. (r=0,82, p<0,05), что было связано с улучшением состояния микроциркуляции ЖКТ у пациентов этой подгруппы и сопровождалось уменьшением лёгочной гипертензии и диастолической нагрузки, а также увеличением ударного объема сердца и артериального давления (рис. 2).

Рис. 2 Динамика ВБД и АПД во I «А» подгруппе
Вместе с тем, у пациентов I «Б» подгруппы отмечалась сохранение ВБГ II степени с максимальным нарастание уровня ВБД на 3−4 сутки (20,5±4,5 мм рт. ст.) (рис 3.). При этом уровень АПД оставался низким, достигая минимальных значений (64,5±5,5 мм рт. ст.) к 3 послеоперационному дню. Отмечалось неустойчивость показателей центральной гемодинамики, низкий уровень артериального давления и ударного объема сердца, регистрировались признаки лёгочной гипертензии и диастолической перегрузки, что сопровождалось нарастанием тяжести состояния по шкалам APACHE II и SOFA. В дальнейшем на фоне проводимого лечения к 6−7 суткам в 43 (61,43%) наблюдениях отмечался постепенный регресс внутрибрюшной гипертензии и улучшение показателей АПД, а у 27 (38,57%) пациентов регистрировалось дальнейшее нарастание значений ВБД и снижением АПД ниже критического уровня.
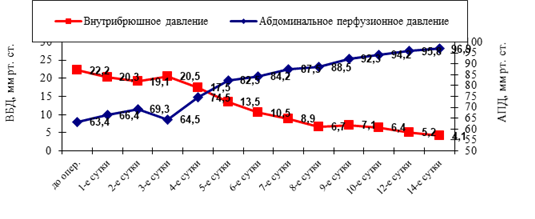
Рис. 3 Динамика ВБД и АПД в I «Б» подгруппе
В дальнейшем, при отсутствии снижения ВБД это приводило к повышению ОПСС, развитию диастолической дисфункции миокарда, к нарушениям в спланхническом кровообращении и гипоксии ЖКТ, развитию хирургической инфекции, что в 21 (30%) случае потребовало выполнения релапаротомии, одной из задач которой являлось снижение уровня ВБД. СВБГ у этих больных был диагностирован в 15 (21,43%) случаях. Декомпрессионная лапаротомия завершалась по одному из вариантов: ушивание только кожи в зоне лапаротомного разреза или временным замещением дефекта передней брюшной стенки синтетической заплатой. Во всех случаях оперативное лечение дополнялось проведением декомпрессии кишечника: при дыхательной недостаточности, неустойчивой гемодинамики и низком уровне АПД выполнялось одномоментная декомпрессия тонкой кишки с последующим дренированием начальных отделов тощей кишки, в других случаях осуществлялось назогастроинтестинальное дренирование. Критерием выбора способа закрытия лапаротомной раны являлся уровень ВБД и АПД. Первый вариант применяли при ВБД? 15 мм рт. ст. и АПД? 75 мм рт. ст. Второй вариант использовали при ВБД > 15 мм рт. ст. и АПД? 70 мм рт. ст.
К 7 — 8-м суткам после операции показатели ВБД и АПД находились в пределах нормы в обеих подгруппах, что подтверждалось отсутствием ВБГ и сводило вероятность трофических нарушений к минимуму. Клинически это сопровождалось регрессом воспалительного процесса в брюшной полости, восстановлением перистальтики кишечника и диуреза, уменьшении количества отделяемого по зонду, улучшением параметров центральной гемодинамики.
При анализе данных мониторинга ВБД и АПД у больных II группы установлено, что у этих пациентов в результате проведения стандартной комплексной консервативной терапии отмечалось снижение уровня внутрибрюшного давления ниже 15 мм рт. ст. Однако дальнейшее прогрессирования воспаления в тканях поджелудочной железы и забрюшинного пространства консервативными методами приостановить не удавалось, что к 4 — 7-м суткам приводило к ухудшению клинической симптоматики и лабораторных показателей и сопровождалось повышением ВБД до 25,8±2,1 мм рт. ст. и снижением АПД ниже 65 мм рт. ст., что явилось показанием к оперативному вмешательству (рис. 4 и 5).

Рис. 4 Динамика ВБД и АПД во II «А» подгруппе
У больных II «А» подгруппы были выполнены «открытые» дренирующие операции. В раннем послеоперационном периоде было отмечено постепенное снижение уровня внутрибрюшного давления ниже 15 мм рт. ст. в течение суток, с улучшением показателей перфузии органов брюшной полости. Использование открытых дренирующих операций при панкреонекрозе, с проведением программных ревизий и санаций, позволило замедлить прогрессирование панкреонекроза и дальнейшее повышение ВБД. В последующем уровень ВБД и АПД соответствовал характеру морфологических изменений в патологической зоне, верифицированных с помощью УЗИ и КТ.
Во II «Б» подгруппе выполнение «закрытых» дренирующих операций приводило к временной стабилизации состояния больных и снижению внутрибрюшного давления до 17,2±4,7 мм рт. ст. (см. рис. 5). Однако в 38 (63,33%) наблюдениях принятыми мерами приостановить дальнейшее прогрессирование деструкции поджелудочной железы не удалось, что привело к повышению ВБД до 29,9±6,9 мм рт. ст., со снижением АПД до 62,3±3,5 мм рт. ст. При этом отмечалась неустойчивость показателей центральной гемодинамики, потребовавшая проведение инотропной поддержки, ухудшение тяжести состояния по шкалам APACHE II и SOFA.

Рис. 5 Динамика ВБД и АПД во II «Б» подгруппе
Наличие отрицательной динамики свидетельствовало о развитии гнойно-септических осложнений и потребовало выполнения «открытого» оперативного вмешательства. В раннем послеоперационном периоде было отмечено постепенное снижение уровня ВБД ниже 18 мм рт. ст. и увеличения АПД выше 70 мм рт. ст. в течение суток. В дальнейшем уровень ВБД и АПД соответствовал характеру морфологических изменений в патологической зоне, верифицированных с помощью УЗИ и КТ. В 13 (21,67%) случаях было установлено развитие СВБГ.
Наблюдаемая динамика изменений значений ВБД и АПБ в III группе больных представлена на рисунках 6 и 7. Использование приемов декомпрессионного завершения оперативного лечения перитонита у пациентов III «А» подгруппы уже с первых суток привело к статистически достоверному снижению ВБД до 13,5± 6,1 мм рт. ст., в сравнении с III «Б» подгруппой (r=0,84, p<0,05). Отмечался рост показателей АПД — до 76,2±8,3 мм рт. ст. (r=0,81, p<0,05), что характеризовало восстановление микроциркуляции. Увеличение ВБД на 4 — 5-е сутки до 15,6±1,5 мм рт. ст., было связано с окончательным закрытием лапаротомной раны. В дальнейшем послеоперационном периоде было отмечено постепенное снижение уровня ВБД и улучшение показателей АПД, к 10−12-м суткам после операции показатели ВБД и АПД находились в пределах нормы. Клинически это сопровождалось улучшением балльной оценки по шкалам тяжести состояния, регрессом воспалительного процесса в брюшной полости, купирование признаков SIRS, восстановлением перистальтики кишечника, улучшением параметров центральной гемодинамики и спланхнического кровообращения.
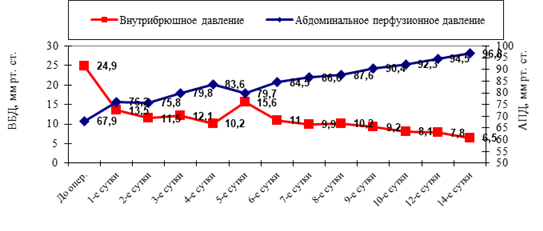
Рис. 6 Динамика ВБД и АПД в III «А» подгруппе
В первые дни послеоперационного периода у пациентов III «Б» подгруппы отмечалась ВБГ второй степени, с постепенным нарастанием уровня ВБД к 4−5 суткам (27,1±4,5 мм рт. ст.), что соответствовало ВБГ III степени (рис. 7).
Уровень АПД у больных данной подгруппы оставался низким, достигая минимальных значений (61,3±9,1 мм рт. ст.) на 5-е сутки. Нарастание уровня ВБД у них характеризовалось клиническим ухудшением состояния и прогрессированием воспалительного процесса в брюшной полости, развитием абдоминального сепсиса и в 24 (45,15%) наблюдениях привело к СВБГ. На этом фоне было отмечено достоверное падение артериального давления и ударного объема сердца, увеличение лёгочной гипертензии и диастолической перегрузки, а также выраженное расширение периферических сосудов, снижение темпа диуреза.

Рис. 7 Динамика ВБД и АПД в III «Б» подгруппе
У 20 (38,46%) больных была выполнена релапаротомия, с наложением декомпрессионной лапаростомы. Анализ полученных результатов показал, что лапаростомия, с различными вариантами дозированной декомпрессии, приводит к снижению ВБД в ближайшие 9,5±2,1 часов и предупреждает дальнейшее прогрессирование перитонита и органной дисфункции.
В дальнейшем на фоне проводимого лечения к 12−14 суткам у пациентов III «Б» подгруппы отмечалось постепенное снижение ВБГ и улучшение показателей АПД, центральной гемодинамики и спланхнического кровообращения. Данные клинико-инструментальных исследований и результаты балльной оценки по шкалам оценки тяжести состояния также свидетельствовали о купировании воспалительного процесса.
Наблюдаемая динамика ВБД и АПД в IV группе представлена на рисунках 8 и 9. В IV «А» подгруппе в первые сутки отмечалась статистически достоверное снижение ВБД до 7,2±3,7 мм рт. ст. (r=0,81, p<0,05) и повышение показателей АПД — до 85,4±4,6 мм рт. ст. (r=0,83, p<0,05). Такая динамика показателей свидетельствовала о значительном улучшении состояния спланхнического кровообращения, функции внешнего дыхания и увеличении ударного объема сердца и артериального давления (рис 8.).
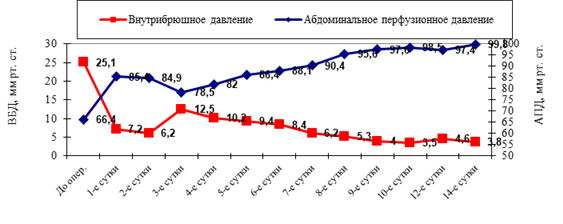
Рис. 8 Динамика ВБД и АПД в IV «А» подгруппе
Увеличение ВБД у пострадавших на 3-й сутки до 12,5±3,5 мм рт. ст., было связано с очередным этапом оперативного лечения и окончательным закрытием лапаротомной раны. К седьмым суткам после операции показатели ВБД и АПД находились в пределах нормы, что подтверждалось отсутствие ВБГ и сводило вероятность трофических нарушений к минимуму. Данные клинико-инструментальных исследований и результаты балльной оценки по шкалам оценки тяжести состояния также свидетельствовали о купировании воспалительного процесса в брюшной полости.
В первые дни послеоперационного периода у пациентов IV «Б» подгруппе отмечалась ВБГ II степени (см. рис. 9). В дальнейшем наблюдалось прогрессивное нарастание уровня ВБД к 4−5 суткам (26,9±3,7 мм рт. ст.). При этом уровень АПД также снижался, достигая минимальных значений (60,3±9,1 мм рт. ст.) также к 5-м суткам послеоперационного периода.
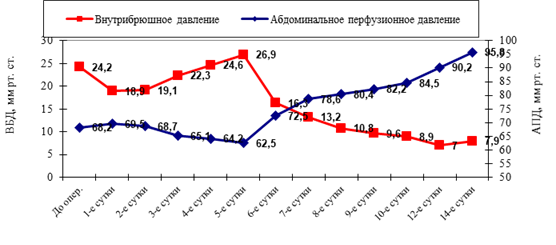
Рис. 9 Динамика ВБД и АПД в IV «Б» подгруппе
Увеличение ВБД коррелировало с увеличением количества баллов по шкале SOFA, что свидетельствовало об ухудшении тяжести состояния и развитии органной дисфункции. Отмечалось нарастание признаков SIRS, неустойчивость показателей центральной гемодинамики.
Повышение и сохранение ВБД до 25 мм рт. ст. и выше, снижением АПД ниже критических значений у пострадавших IV «Б» подгруппы, с ушитой наглухо лапаротомной раной, свидетельствовало о развитии в 15 (28,85%) наблюдениях СВБГ. Сочетание гипотонии, с невозможностью обеспечения адекватной респираторной поддержки у 11 (25,58%) пострадавших IV «Б» подгруппы потребовало выполнения экстренной декомпрессионной лапаротомии. Использование различных вариантов декомпрессии способствовало снижению ВБГ в ближайшие 10±2,2 часов. В дальнейшем на фоне проводимого лечения к 9−10 суткам отмечался постепенный регресс ВБГ и улучшение показателей АПД.
Результаты мониторинга ВБД и АПБ в V группе представлены на рисунках 10 и 11.
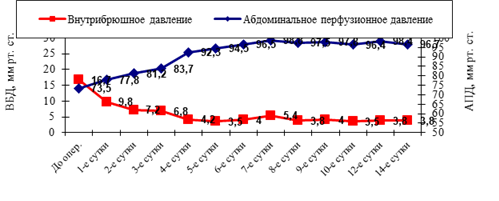
Рис. 10 Динамика ВБД и АПД в V «А» подгруппе
Анализ динамики ВБД и АПД у больных V «А» подгруппе показал, что использование способов ненатяжной герниопластики, с применением полипропиленового сетчатого эндопротеза «Линтекс-Эсфил», способствует статистически достоверному снижению уровня ВБД в первые сутки послеоперационного периода с 16,7±3,8 мм рт. ст. до 9,8±2,5 мм рт. ст. (r=0,83, p<0,05) и не приводит к его повышению в дальнейшем. Уровень АПД у больных этой подгруппы характеризовался постепенным нарастанием, что свидетельствовало о восстановлении спланхнического кровообращения.

Рис. 11 Динамика ВБД и АПД в V «Б» подгруппе
У пациентов V «Б» подгруппы, после выполнения герниопластики местными тканями, в первые сутки послеоперационного периода в 30 (81,08%) случаях отмечалась ВБГ II степени и АПД ниже 80 мм рт. ст. В дальнейшем у этих больных было отмечено нарастание ВБД до 26,8 ±5,5 мм рт. ст. к 5-м суткам после операции, что сопровождалось снижением АПД до 60±4,8 мм рт. ст. Клиническая картина характеризовалась развитием признаков дыхательной и сердечно-сосудистой недостаточности, что потребовало повторных оперативных вмешательств. СВБГ в этой подгруппе был диагностирован в 5 (13,51%) наблюдениях.
При расчете корреляционной зависимости в подгруппах «А» и «В» установлено, что между уровнем ВБД и АБД в динамике имеется сильная отрицательная связь (подгруппа «А» r =(-0,99), подгруппа «В» r =(-0,97) p<0,001). Этот факт отражал динамику состояния больного: с уменьшением ВБД увеличивается АПД, что отражает нормализацию спланхнического кровообращения.
В результате исследования динамики ВБД у больных исследуемых подгрупп установлена положительная корреляционная связь между уровнем ВБД и способом закрытия лапаротомной раны (r=0,82, р<0,05). Увеличение показателей ВБД коррелировало с ухудшением состояния больных по шкалам APACHE II и SOFA. Повышение и сохранение ВБД до 25 мм рт. ст. и выше у 72 (27,02%) больных (контрольная подгруппа) с ушитой наглухо лапаротомной раной свидетельствовало о развитии СВБГ. Сочетание гипотонии, с невозможностью обеспечения адекватной респираторной поддержки у 56 пациентов привило к состоянию, когда единственным выходом из него была незамедлительная декомпрессия брюшной полости — выполнение декомпрессионной релапаротомии. Использование предложенных вариантов декомпрессии способствовало снижению ВБД в ближайшие 7±4,5 часов до 13,2±3,8 мм рт. ст. что предупреждало прогрессирование ВБГ и органной дисфункции. Следует указать, что степень органной дисфункции определяет и сроки закрытия лапаростомы. При наличии дыхательной, сердечной недостаточности и ВБД более 15 мм рт. ст., возникающей в результате сведения лапаротомной раны (после устранения перитонита), следует воздержаться от традиционного ушивания брюшной полости и использовать описанные ранее варианты декомпрессионного закрытия лапаротомной раны.
Релапаротомия, направленная на устранение дефекта передней брюшной стенки проводилась во все сроки после восстановления стула, нормализации общего состояния пациентов до удовлетворительного и нормализации уровня ВБД и АПД. Так, не прибегая к повторной госпитализации дефект передней брюшной стенки, был восстановлен в 37,5% наблюдениях. При повторной госпитализации у 48,6% больных, у оставшихся 13,9% пациентов в связи с наличием тяжелой, инвалидизирующей сопутствующей патологией восстановление дефекта брюшной стенки не проводилось, и было рекомендовано ношение абдоминального бандажа.
Установлено, что уровень ВБГ статистически достоверно указывает на прогрессирование воспалительно-деструктивного процесса в брюшной полости, подтвержденного данными лабораторных тестов и оценкой тяжести состояния по шкалам APACHE II и SOFA (см. табл. 4).
Таблица 4 Изменение уровня ВБГ при развитии гнойно-септических осложнений.
Уровень ВБГ. | Уровень лейкоцитов, 109/л. | ЛИИ, усл. ед. | SOFA, баллы. | APACHE II, баллы. | Признаки. | ||||
SIRS,. (2 и более). | Перитонит. | Динамическая кишечная непроходимость. | Гнойно-септические осложнения. | ||||||
I степень,. n=82. | 12,1±2,3. [8,2−14,5]. | 3,1±1,2. [1,9−4,5]. | 2,9±0,6. [1−4]. | 7,8±2,3. [2−14]. | 8 (9,8%). | ; | 56 (69,3%). | 11 (13,4%). | |
II степень,. n=143. | 14,9±1,4. [9,5−16]. | 6,3±1,4. [2,5−7,9]. | 6,2±1,8. [2−6]. | 16±1,7. [6−22]. | 46 (32,2%). | 62 (43,4%). | 77 (53,9%). | 69 (48,3%). | |
III степень,. n=121. | 16,7±1,8. [9,5−21]. | 8,6±1,2. [3,9−11]. | 8,4±1,2. [5−10]. | 19±1,4. [9−28]. | 103 (85,1%). | 121 (100%). | 121 (100%). | 108 (89,3%). | |
IV степень,. n=56. | 20,1±0,8. [15−22,5]. | 10,6±0,8. [6−14,5]. | 10,4± 1,6 [7−12]. | 24±1,2. [12−32]. | 56 (100%). | 56 (100%). | 56 (100%). | 56 (100%). | |
Примечание: — достоверность различий между группами ВБГ I и II степени, ВБГ I и III степени, ВБГ I и IV степени (р<0,05).
Как видно из представленных данных, ВБГ I степени не связана с развитием гнойно-септических осложнений и определяется выраженностью пареза кишки.
Регистрация ВБГ II степени достоверно свидетельствовала о прогрессировании воспалительного процесса и была связана с нарастанием уровня эндогенной интоксикации, прогрессированием признаков перитонита и развитием пареза кишечника.
Анализ данных измерения ВБД у больных с ВБГ III и IV степени достоверно свидетельствовал о наличии абдоминального сепсиса.
4. Анализ результатов влияние ВБГ на состояние спланхнического кровообращения у больных экстренными хирургическими заболеваниями и травмами живота Определение состояния спланхнического кровообращения и степени гипоксии слизистой ЖКТ по данным желудочной тонометрии свидетельствовало, что у больных исследуемых подгрупп в первые сутки после оперативного вмешательства внутрислизистое pH (pHi) было ниже нормальных величин на 2−3% (7,21−7,22 мм рт. ст.) (см. табл. 5). Разница между внутрислизистым и артериальным Рg-а CO2 (CO2-gap) составляла 16,8−18,1 мм рт. ст. Снижение pHi ниже 7,32 в сочетании с увеличением CO2-gap более 13 мм рт.ст. свидетельствовало о наличие интрамурального ацидоза и гипоксии слизистой, отражая состояние тканевой ишемии, обусловленной выраженной гипоперфузией ЖКТ, нарушением кровообращения в спланхническом бассейне.
Сниженная концентрация pHi в желудке и повышенный показатель Рg-а СО2 (CO2-gap) в контрольных подгруппах сохранялись до 3−4-х суток и совпадали с выраженными клинико-рентгенологическими признаками динамической кишечной непроходимости, что указывало на сохраняющуюся гипоксию и ишемию слизистой ЖКТ.
Таблица 5 Изменения показателей желудочной тонометрии в исследуемых группах больных, (М±у).
Показатель. | Подгруппы больных. | Сроки исследования (сутки после операции). | ||||
1-е. | 3-и. | 5-е. | 7-е. | |||
pHi. | Основная. | 7,22±0,01. | 7,34±0,01. | 7,42±0,01. | 7,42±0,03. | |
Контрольная. | 7,21±0,01. | 7,25±0,03. | 7,35±0,02. | 7,39±0,02. | ||
Рg-а СО2. (CO2-gap). | Основная. | 16,8±2,9. | 12,3±2,3. | 8,2±1,4. | 5,4±1,2. | |
Контрольная. | 18,1±2,1. | 15,2±2,2. | 10,5±1,1. | 7,3±1,3. | ||
РgСО2. | Основная. | 56,7±2,2. | 49,3±2,2. | 43,6±1,7. | 38,1±1,8. | |
Контрольная. | 58,1±2,1. | 53,72±2,1. | 49,2±1,9. | 40,2±1,6. | ||
Примечания: * - р<0,05 по отношению к 1-м суткам. pHi — концентрация ионов водорода в слизистой оболочке желудка; Рg-а СО2 (C02-gap) — разность между регионарной и артериальной концентрацией углекислого газа; РgСО2 регионарная концентрация углекислого газа;
У больных основных подгрупп уже к 3-м суткам pHi повышалась до 7,34±0,01 (r=0,85, p<0,05), снижалась CO2-gap — 12,3±2,3 мм рт. ст. (r=0,81, p<0,05), что свидетельствовало об уменьшении регионарного ацидоза и улучшении тканевой перфузии (табл. 5). От 3-х к 7-м суткам данные тонометрии оставались в пределах нормы.
Известно, что одним из факторов развития энтеральной кишечной недостаточности при ВБГ являются деструктивные изменения в тканях кишечной стенки, а также выраженные изменения со стороны эпителия, обусловленные гипоксией в результате острых нарушений в системе микроциркуляции. Поэтому достоверное повышение pHi в слизистой желудка и снижение регионарной концентрации СО2 у больных основных подгрупп по сравнению с больными контрольных подгрупп, вероятно, связано с усилением процессов регенерации в слизистой оболочке ЖКТ и восстановления функциональной активности энтероцитов на фоне адекватного спаланхнического кровообращения.
Таким образом, результаты мониторинга уровня ВБД и АПД, а также данные желудочной тонометрии свидетельствуют о положительном влиянии декомпрессионных способов закрытия лапаротомной раны на восстановление функций ЖКТ и разрешение энтеральной кишечной недостаточности.
Бактериальная транслокация, обусловленная изменениями проницаемости кишечной стенки при энтеральной кишечной недостаточности у больных с ВБГ, рассматривается как основная причина развития SIRS, сепсиса и ПОН, это подтверждалось проведенными нами результатами микробиологических исследований экссудата брюшной полости и отделяемого по интестинальному зонду.
У 73 пациентов с ВБД более 15 мм рт. ст., через 24−48 часов с момента начала заболевания, при микробиологическом исследовании отделяемого из интестинального зонда были обнаружены патогенные микроорганизмы в концентрации 1×106 — 3×106 в 1 мл, при этом наиболее часто высеивались: Escherichia coli; Proteus spp; Streptococcus spp. и ассоциации грамотрицательных микроорганизмов. При микробиологическом исследовании экссудата брюшной полости, некротических тканей были определены следующие микроорганизмы: Escherichia coli, Pseudomonas spp., Klebsiella spp., Proteus spp., Citrobacter spp., Serratia spp., Enterococcus faecalis, Ochrobactrum anthropi, Acinetobacter spp., Staphylococcus aureus, Streptococcus spp., Bacteroides fragilis. Спектр выделенных культур был представлен в 40% случаев преимущественно ассоциациями грамотрицательных микроорганизмов. Принципиальным является то, что микробный состав содержимого тонкой кишки и отделяемого из брюшной полости не отличался, что подтверждает факт бактериальной транслокации.
4. Анализ результатов лечения больных экстренными хирургическими заболеваниями и травмами живота с развившейся ВБГ Для определения степени эффективности хирургического лечения больных экстренными хирургическими заболеваниями и травмами живота, осложненных развитием ВБГ с применением разработанного нами лечебно-диагностического алгоритма (рис. 12−13) был проведен анализ послеоперационных осложнений, летальности в основных и контрольных подгруппах (см. табл. 6).
Все случившиеся осложнения мы условно разделили на три группы: «системные» (острая сердечная недостаточность, ДВС, абдоминальный сепсис, РДСВ, полиорганная недостаточность и т. п.), гнойно-воспалительные (прогрессирование перитонита, образование абсцессов брюшной полости, формирование флегмон забрюшинной клетчатки, нагноение операционной раны и т. п.) и «локальные» (несостоятельность анастомозов, некроз колостомы, кровотечение из острых язв ЖКТ, кишечная непроходимость) осложнения.
Таблица 6 Результаты лечения больных исследуемых групп.
Группы больных. | Кол-во осложнений. | Кол-во умерших, n (%). | |||
«Системные», n (%). | Гнойно-воспалительные, n (%). | «Локальные», n (%). | |||
I «А», n=73. | 9 (12,33%). | 13 (17,81%). | 9 (12,33%). | 7 (9,59%). | |
I «Б», n=70. | 19 (27,14%). | 24 (34,29%). | 27 (38,57%). | 16 (22,86%). | |
II «А», n=66. | 15 (22,73%). | 26 (39,39%). | 17 (25,78%). | 11 (16,67%). | |
II «Б», n=60. | 28 (46,67%). | 48 (80%). | 25 (41,67%). | 21 (35%). | |
III «А», n=56. | 9 (16,07%). | 13 (23,21%). | 10 (17,86%). | 9 (16,07%). | |
III «Б», n=52. | 29 (55,77%). | 32 (61,54%). | 21 (40,38%). | 24 (46,15%). | |
IV «А», n=41. | 9 (21,95%). | 11 (26,83%). | 5 (12,2%). | 10 (24,39%). | |
IV «Б», n=43. | 19 (44,19). | 16 (37,21%). | 20 (46,51%). | 19 (44,19%). | |
V «А», n=36. | 1 (2,78%). | 4 (11,11%). | ; | 1 (2,78%). | |
V «Б», n=37. | 5 (13,51). | 10 (27,03%). | 6 (16,22%). | 5 (13,51%). | |
Примечание: при наличии у пациента нескольких осложнений каждое из них указано в соответствующей графе, достоверность различий между подгруппами «А» и «Б» (р<0,05).
У 24,63% пациентов основных подгрупп были установлены различные гнойно-воспалительные осложнения, в 15,81% наблюдениях отмечались «системные», а в 15% - «локальные» осложнения. В структуре осложнений больных контрольных подгрупп в 49% наблюдениях были верифицированы гнойно-воспалительные осложнений, в 37,74% - «системные», а в 37,36% - «локальные» осложнения.
Из таблицы 6 видно, что общая летальность у пациентов с интраабдоминальной патологией в контрольной подгруппе была существенно выше, чем в основной и составила 32,08% и 13,97% соответственно. Причиной смерти у 43 пациентов контрольных подгрупп в раннем послеоперационном периоде являлась острая дыхательная и сердечнососудистая недостаточность, на фоне прогрессирующей полиорганной недостаточности, а в 36 наблюдениях явились гнойно-воспалительные осложнения, развившиеся в позднем послеоперационном периоде, на фоне абдоминального сепсиса. В основных подгруппах в 81,58% наблюдениях причиной смерти явились различные гнойно-воспалительные осложнения в позднем послеоперационном периоде.
Каковы причинно-следственные связи между высокой ВБГ и возникшими осложнениями при СВБГ? Вполне очевидно, что возникновение эвентрации было связано непосредственно с высоким уровнем ВБД. Ишемия стенки кишечника и желудка на высоте ВБГ и снижении АПД являлась одной из причин развития несостоятельности межкишечных анастомозов, кишечных свищей и желудочных кровотечений из острых язв у больных СВБГ. На фоне ВБГ снижается перистальтика кишечника и функциональная активность сфинктерного аппарата и тем самым повышается риск аспирации. Компрессия грудной полости за счет краниального смещения диафрагмы приводила к образованию ателектазов, увеличению легочного шунтирования крови. Сочетание названных механизмов и микроаспирации желудочного содержимого в трахею является одним из механизмов развития нозокомиальных пневмоний при ВБГ. Замедление кровотока и склонность к тромбообразованию у больных с ВБГ приводит к увеличению числа случаев ТЭЛА.
Лапаростомия у пациентов с экстренной интраабдоминальной патологией была направлена на лечение и профилактику повышения ВБД, на создание условий для малотравматичного выполнения релапаротомии, на предупреждение развития эвентерации, на обеспечение контроля за характером отделяемого из брюшной полости, на дренирование отдельных областей брюшной полости и предохранение передней брюшной стенки от развития в ней инфекции, что имело важное значение для окончательного закрытия брюшной полости.
Следует отметить, что решение о декомпрессии брюшной полости принималось не только на основании результатов отдельных измерений внутрибрюшного давления, а с учетом всей клинической картины интраабдоминальной патологии и развивающейся полиорганной недостаточности (табл. 7).
Таблица 7 Частота развития осложнений со стороны различных органов и систем при внутрибрюшной гипертензии III, IV степени.
Проявления полиорганной недостаточности. | III — IV степень внутрибрюшной гипертензии. | |
Острая дыхательная недостаточность, %. | 97,2. | |
Сердечно-сосудистая недостаточность, %. | 82,5. | |
Энтеральная кишечная недостаточность, %. | 71,7. | |
Острая почечная недостаточность, %. | 48,6. | |
Энцефалопатия, %. | 33,9. | |
Геморрагический синдром, %. | 26,5. | |
Третья и четвертая степень внутрибрюшной гипертензии в 97,2% случаев сопровождалась развитием дыхательной недостаточности, в 82,5% была отмечена сердечно-сосудистая недостаточность. Энтеральная кишечная недостаточность развилась у 67,7% больных, острая почечная недостаточность у 48,6%, энцефалопатия — в 33,9% случаев и геморрагический синдром — у 26,5% больных. Прогрессирование дыхательной и сердечно-сосудистой недостаточности, нарушения гемокоагуляции, энтеральная и почечная дисфункция происходили в результате развития полиорганной недостаточности. При этом третья и четвертая степень внутрибрюшной гипертензии в 47,5% случаев сочеталась развитием недостаточности двух органов и систем, в 35,6% - трех, а в 16,9% - четырех и более органов и систем. При повышении ВБД до 15−25 мм рт. ст. признаки полиорганной недостаточности развивались не позднее 24−32 часов от начала заболевания, а при повышении выше 25 мм рт. ст. — через 8−12 часов.
Таким образом, повышенное внутрибрюшное давление являлось достоверным неблагоприятным прогностическим признаком развития послеоперационных осложнений и позволяет судить о степени тяжести состояния пациентов.
Таким образом, ведение больных экстренными хирургическими заболеваниями и травмами живота согласно разработанному лечебно-диагностическому алгоритму (рис. 12−13), с учетом показателей ВБД, АПД и использованием медикаментозных и хирургических методов коррекции ВБГ позволяет сократить предоперационное время в 1,4 раза, среднее количество койко-дней пребывания в стационаре в 1,5 раза, снизить показатели послеоперационных осложнений и послеоперационной летальности в 1,9 раза.
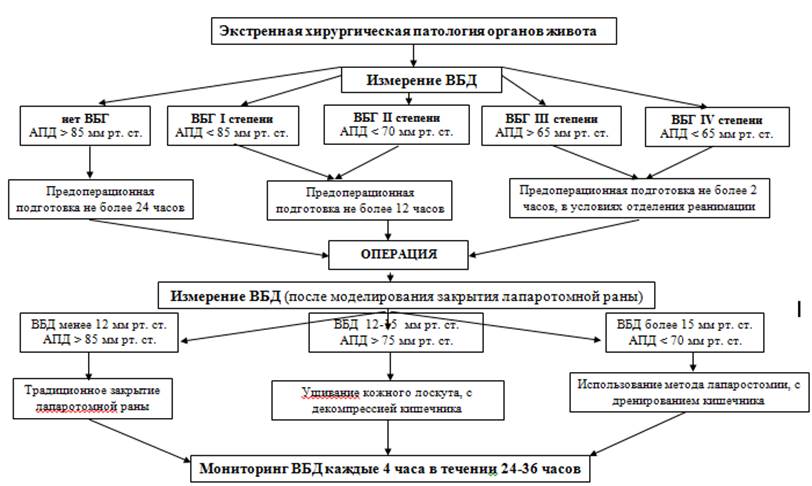
Рис. 12 Лечебно-диагностический алгоритм предоперационного периода
Рис. 13 Лечебно-диагностический алгоритм послеоперационного периода