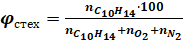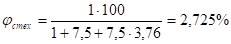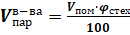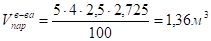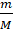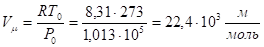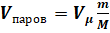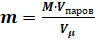Количество вещества, А (в кг), которое должно испариться в помещении
Количество вещества, А (в кг), которое должно испариться в помещении размерами aЧbЧh чтобы в нем создалась наиболее взрывоопасная паровоздушная смесь, находят из условия образования в помещении паровоздушной смеси стехиометрического состава. Для этого из уравнения материального баланса горения находит стехиометрическую концентрацию вещества А:
горение взрыв пламя газовоздушный Стехиометрическая смесь содержит 1 моль трет-амилового спирта () 7,5 моль кислорода и 7,5· 3,76 моль азота.
Концентрация горючего в такой смеси:
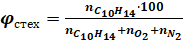
(30).
По рассчитанной концентрации вещества и известному объему помещения находим объем паров вещества А:
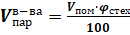
(31).
Зная объем паров, рассчитывает их массу, воспользовавшись понятием киломоля вещества.
1 моль вещества — количество вещества в граммах, масса которого численно равна молекулярной массе.
В связи с тем, что масса 1 моля вещества численно равна его молекулярной массе, то в 1 моле любого вещества содержится одинаковое количество молекул. Оно составляет NА = 6,02· 1023молекул/моль (число Авогадро). Поэтому в газообразном состоянии 1 моль любого вещества при нормальных условиях занимает один и тот же объем, равный 22,4 л. Таким образом, объем 1 моля любого газа при Т0 = 273 К и Р0 = 1,013· 105 Па составляет 22,4 л/моль или 22,4 10−3 м3/моль. Объем 1 киломоля в тысячу раз больше и равен.
22,4 м3 /кмоль. Объем 1 моля газа можно определить из уравнения состояния (Клапейрона — Менделеева):
где m - масса вещества, М — масса одного моля вещества, — число молей вещества, R — универсальная газовая постоянная (R = 8,31Дж/(моль· К).
Для 1 моля вещества (m/М = 1) объем газа при нормальных условиях составит:
.
Где Дж=Н· м, Па= Н/м2.
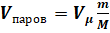
(33).

(34).
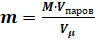
(35).