Процессы извлечения неопентилгликоля из водно-органических систем

Сравнение четырехкомпонентных систем неопентилгликоль — формиат натрия — метанол — вода и неопентилгликоль — формиат натрия — метанол — реакционная смесь Исследования показали, что метанол выступает как гомогенизатор для расслаивающихся смесей. С увеличением концентрации метанола в разрезах систем область расслаивания уменьшается и исчезает при концентрации метанола около 15%. При введении… Читать ещё >
Процессы извлечения неопентилгликоля из водно-органических систем (реферат, курсовая, диплом, контрольная)
Аннотация: Приведены результаты исследования растворимости поликомпонентных водно-органических систем, содержащих неопентилгликоль, формиат натрия и органические растворители. На основании полученных диаграмм растворимости определены температурно-концентрационные параметры процессов экстракции и кристаллизации неопентилгликоля и формиата натрия, теоретически обоснованы технологические схемы процессов и проведен укрупненный лабораторный эксперимент. неопентилгликоль растворимость поликомпонентный Ключевые слова: Неопентилгликоль, водно-органические системы, диаграммы растворимости, экстракция, кристаллизация Начало работы опубликовано под тем же названием в предыдущем выпуске журнала «Инженерный вестник Дона» № 4, 2014 г.
Четырехкомпонентные системы [27−32].
Изучение трехкомпонентных систем показало принципиальную возможность осуществления процесса кристаллизации неопентилгликоля. Однако физико-химические свойства этих систем таковы, что получаемый продукт содержит более 1 масс.% формиата натрия, что в конечном итоге сужает область его дальнейшего использования. Один из путей усовершенствования предлагаемого процесса — это введение в систему нового компонента, который бы высаливал формиат натрия из насыщенных растворов неопентилгликоля и позволял получать более чистый продукт. Из литературных данных известно, что для высаливания формиата натрия можно использовать метанол.
Выбор температуры исследования — 30 °C связан с физико-химическими свойствами компонентов систем. При температурах ниже 30 °C происходит образование кристаллогидратов формиата натрия (ниже 15 °C — тригидрат, от 15 до 26 °C — дигидрат), что приводит к резкому повышению вязкости растворов и затрудняет процесс кристаллизации неопентилгликоля. Изотермы растворимости при 30 и 50 °C практически совпадают, а повышение температуры может привести к усложнению аппаратурного оформления процесса.
Система неопентилгликоль — формиат натрия — метанол — вода.
Четырехкомпонентная система неопентилгликоль — формиат натрия — метанол — вода изучена с целью оптимизации процесса кристаллизации неопентилгликоля, а так же для выявления степени высаливающего эффекта метанола в отношении формиата натрия.
Данные по растворимости твердых веществ в воде и метаноле при 30 °C приведены в таблице 3.
Таблица 3.
Растворимость формиата натрия и неопентилгликоля в воде и метаноле (мас.%) при 30 °C.
Вещество. | Растворитель. | ||
Вода. | Метанол. | ||
Неопентилгликоль. | 87.80. | 82.60. | |
Формиат натрия. | 50.70. | 3.40. | |
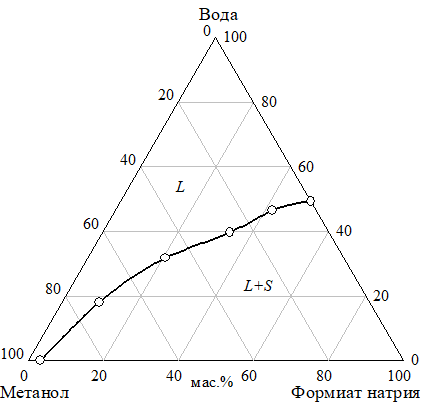
Эвтонический раствор оконтуривающей системы неопентилгликоль — формиат натрия — метанол при 30 °C содержит менее 1 масс.% формиата натрия и 15.5 масс.% метанола (рис. 13а), а в системе неопентилгликоль — формиат натрия — вода концентрация формиата натрия в эвтонике — 2.1 масс.% (рис. 8а). Растворимость неопентилгликоля в воде и метаноле изменяется не значительно, а у формиата натрия при введении в систему метанола резко уменьшается (рис. 14, 15; табл. 3).
Анализ оконтуривающих систем показал целесообразность использования метанола в качестве высаливателя для формиата натрия. Для оптимизации процесса высаливания изучен ряд разрезов (с 50%, 25% и 10% водными растворами метанола) четырехкомпонентной системы неопентилгликоль — формиат натрия — метанол — вода.
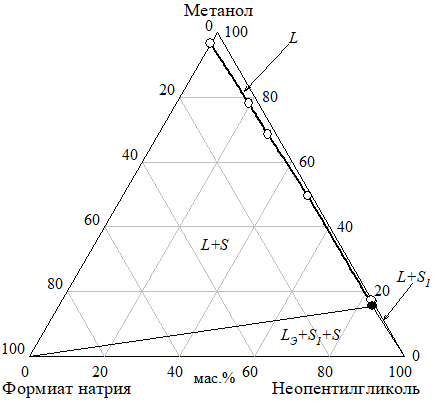
- а)
- б)
Рис. 13 Изотермы растворимости (а) и показателя преломления (б) системы неопентилгликоль — формиат натрия — метанол при 30°C
- а)
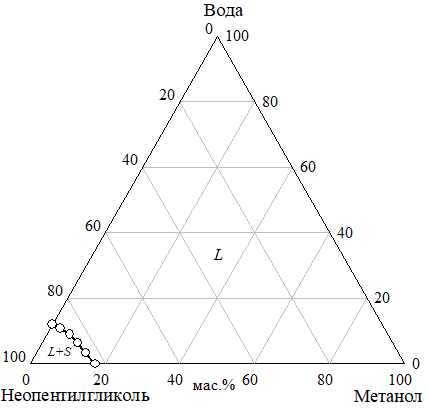
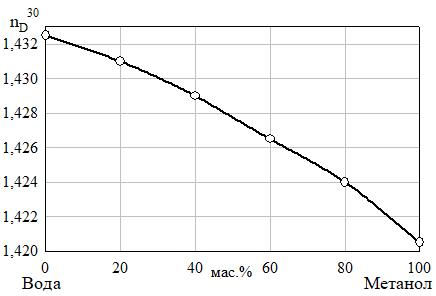
- б)
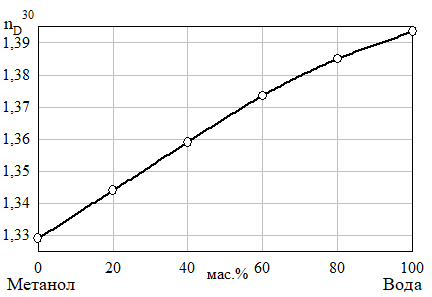
Рис. 14 Изотермы растворимости (а) и показателя преломления (б) системы неопентилгликоль — метанол — вода при 30°C
а).
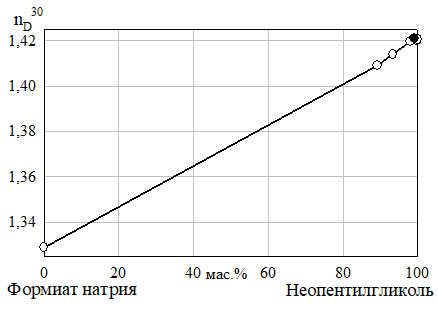
б) Рис. 15 Изотермы растворимости (а) и показателя преломления (б) системы формиат натрия — метанол — вода при 30°C
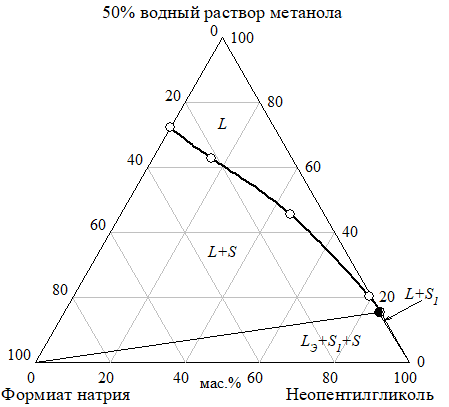
В разрезе с 10% водным раствором метанола сохраняется область монотектического равновесия. Область кристаллизации неопентилгликоля более выражена, чем в других разрезах. В разрезах с 50% и 25% водными растворами метанола области расслаивания не обнаружено (рис. 16−18). Составы эвтонических растворов изученных разрезов приведены в таблице 4.
- а)
- б)
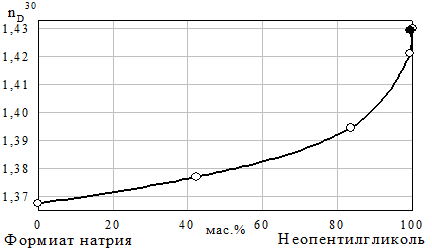
Рис. 16 Изотермы растворимости (а) и показателя преломления (б) разреза неопентилгликоль — формиат натрия — 50% водный раствор метанола при 30°C
- а)
- б)
Рис. 17 Изотермы растворимости (а) и показателя преломления (б) разреза неопентилгликоль — формиат натрия — 25% водный раствор метанола при 30°C
а).
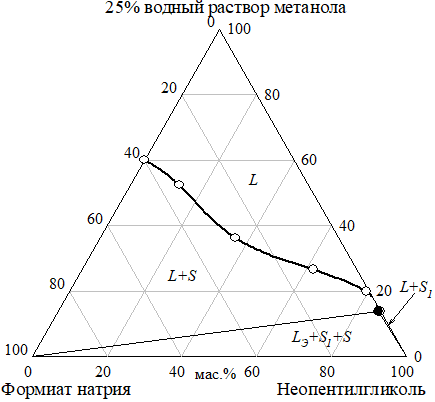
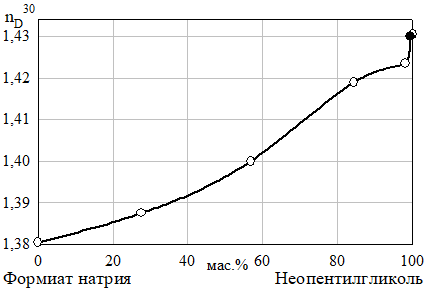
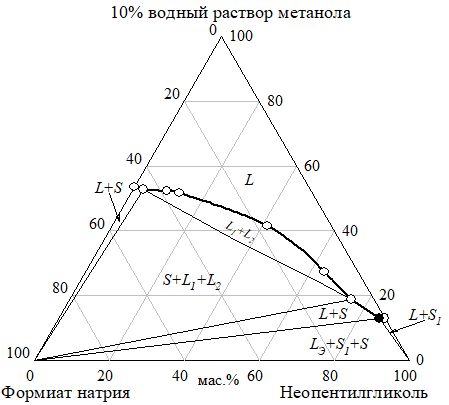
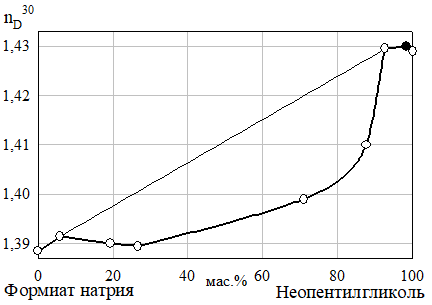
б) Рис. 18 Изотермы растворимости (а) и показателя преломления (б) разреза неопентилгликоль — формиат натрия — 10% водный раствор метанола при 30°C
Таблица 4
Составы эвтонических растворов разрезов четырехкомпонентной системы.
Разрезы. | Состав эвтонических растворов, мас.%. | ||||
Неопентилгликоль. | Формиат натрия. | Метанол. | Вода. | ||
50% водный раствор метанола — неопентилгликоль — формиат натрия. | 84.20. | 0.50. | 7.65. | 7.65. | |
25% водный раствор метанола — неопентилгликоль — формиат натрия. | 85.60. | 0.50. | 3.47. | 10.43. | |
10% водный раствор метанола — неопентилгликоль — формиат натрия. | 85.70. | 1.50. | 1.28. | 11.52. | |
Установлено, что растворимость формиата натрия в водно-спиртовых растворах неопентилгликоля понижается с увеличением концентрации последнего. Полученные экспериментальные данные подтвердили, что метанол может быть использован для высаливания формиата натрия из насыщенных растворов неопентилгликоля.
Система неопентилгликоль — формиат натрия — метанол — реакционная смесь Четырехкомпонентная система неопентилгликоль — формиат натрия — метанол — реакционная смесь фактически является разрезом условно пяти компонентной системы неопентилгликоль — формиат натрия — метанол — вода — сумма технологических примесей. В реакционной смеси количественное содержание примесей неизвестно, поэтому диаграмма растворимости изученного нами разреза построена в тетраэдре состава, вершины которого неопентилгликоль, формиат натрия, метанол, реакционная смесь.
Изучены трехкомпонентные оконтуривающие системы: неопентилгликоль — метанол — реакционная смесь (рис. 19) и формиат натрия — метанол — реакционная смесь (рис. 20). Установлено, что технологические примеси способствуют процессу высаливания формиата натрия. Изучено два разреза четырехкомпонентной системы (рис. 21, 22). Составы эвтонических растворов разрезов приведены в таблице 5.
Установлено, что растворимость формиата натрия понижается с увеличением концентрации неопентилгликоля в растворах реакционной смеси со спиртом.
Таблица 5.
Составы эвтонических растворов разрезов четырехкомпонентной системы.
Разрезы. | Состав эвтонических растворов, мас.%. | ||||
Неопентилгликоль. | Формиат натрия. | Метанол. | Реакционная смесь. | ||
25% раствор метанола в реакционной смеси — неопентилгликоль — формиат натрия. | 76.00. | 0.50. | 5.88. | 17.62. | |
10% раствор метанола в реакционной смеси — неопентилгликоль — формиат натрия. | 80.50. | 0.50. | 1.90. | 17.10. | |
Сравнение четырехкомпонентных систем неопентилгликоль — формиат натрия — метанол — вода и неопентилгликоль — формиат натрия — метанол — реакционная смесь Исследования показали, что метанол выступает как гомогенизатор для расслаивающихся смесей. С увеличением концентрации метанола в разрезах систем область расслаивания уменьшается и исчезает при концентрации метанола около 15%. При введении в реакционную смесь метанола суммарный высаливающий эффект в отношении формиата натрия усиливается. В разрезах с 10% раствором метанола происходит уменьшение области монотектического равновесия за счет расширения поля кристаллизации формиата натрия (рис. 23). Дальнейшее повышение концентрации метанола приводит к увеличению области кристаллизации формиата натрия, причем в системе с реакционной смесью этот эффект проявляется более ярко (рис. 24).
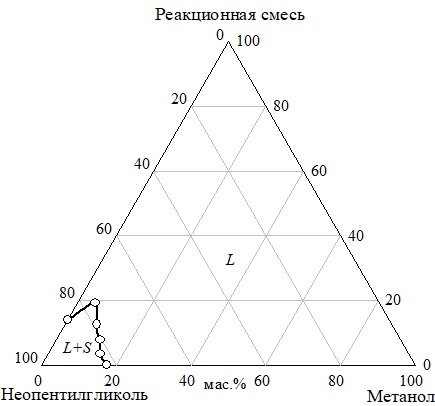
- а)
- б)
Рис. 19 Изотермы растворимости (а) и показателя преломления (б) системы неопентилгликоль — метанол — реакционная смесь при 30°C
- а)
- б)
Рис. 20 Изотермы растворимости (а) и показателя преломления (б) системы формиат натрия — реакционная смесь — метанол при 30°C
а) б.
Рис. 21 Изотермы растворимости (а) и показателя преломления (б) системы неопентилгликоль — формиат натрия — 25% раствор метанола в реакционной смеси при 30°C
- а)
- б)
Рис. 22 Изотермы растворимости (а) и показателя преломления (б) системы неопентилгликоль — формиат натрия — 10% раствор метанола в реакционной смеси при 30°C
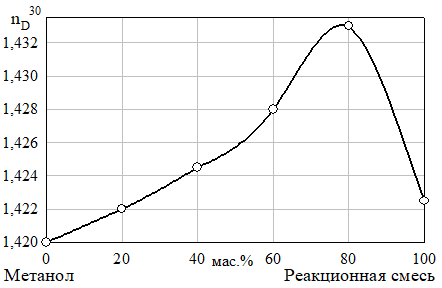
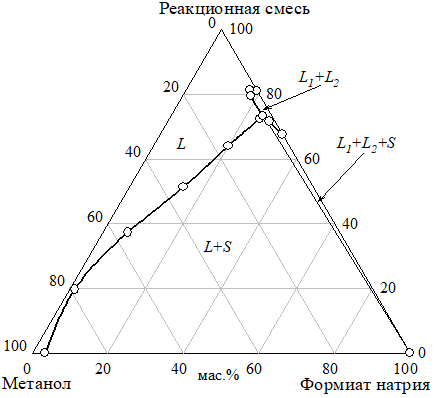
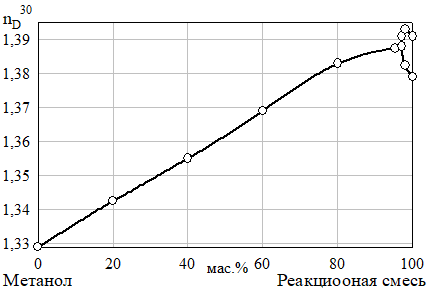
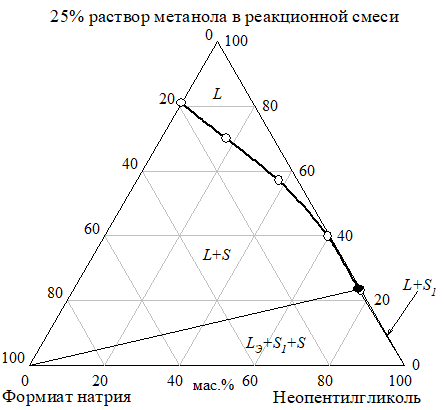
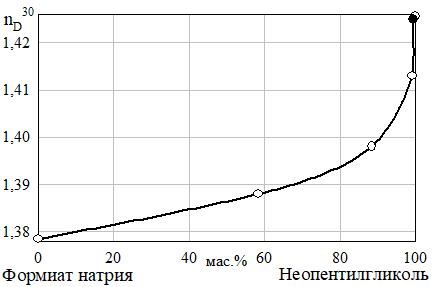
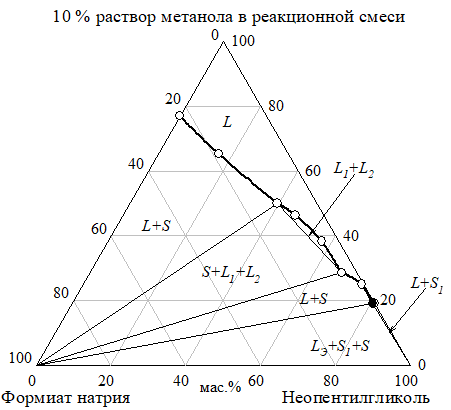
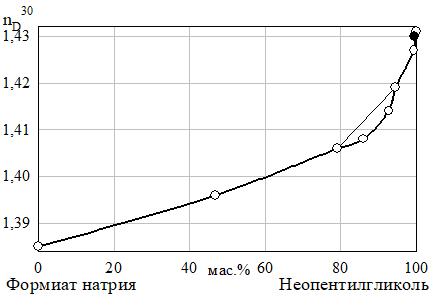
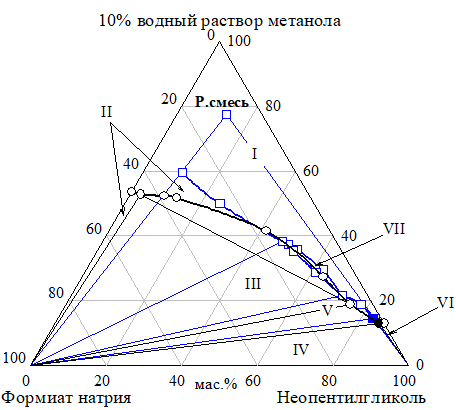
Рис. 23 Проекция разреза неопентилгликоль — формиат натрия — реакционная смесь на грань тетраэдра неопентилгликоль — формиат натрия — 10% водный раствор метанола при 30 °C (Фазовые области: I — L, II, V — L+S, III — S+L1+L2, IV — LЭ+S+S1, VI — L+S1, VII — L1+L2)
Зависимость содержания формиата натрия от концентрации метанола в эвтонических растворах представлена на рис. 25. Она позволяет установить минимальную концентрацию метанола для максимального высаливания формиата натрия. Для системы с реакционной смесью оптимальная концентрация метанола в эвтоническом растворе составляет 2−4 масс.%, при этом содержание формиата натрия менее 0,5 масс.%.
Кристаллизация неопентилгликоля.
Система неопентилгликоль — формиат натрия — вода Графическое изображение процесса кристаллизации неопентилгликоля приведено на рисунке 26, состав исходной и промежуточных смесей — в таблице 6. Соотношение и состав фаз определены по диаграммам растворимости.
При упаривании исходного раствора состава точки P при температуре 50 °C, его состав изменяется по лучу испарения до предельной ноды — точка В. Эта смесь распадается на две жидкие фазы, которые разделяют. Соотношение фаз: верхняя, точка С — 49,6%, нижняя, точка М — 50,4%.
Верхнюю фазу охлаждают до 20 °C, при этом в осадок выпадает твердая фаза состава точки D. Состав раствора меняется по линии, соединяющей эвтоники 50° и 20 °C. Состав конечного раствора соответствует эвтоническому раствору при 20 °C точка E. Соотношение выпавшей твердой фазы и эвтонического раствора равно 41,20: 58,80 соответственно. При упаривании эвтонического раствора получаем 8,96 масс.ч. неопентилгликоля и 0,045 масс.ч. формиата натрия. Таким образом, теоретический выход неопентилгликоля в данном процессе составляет 59,73%.
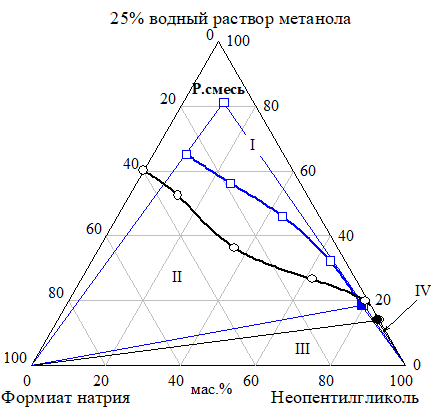
Рис. 24 Проекция разреза неопентилгликоль — формиат натрия — реакционная смесь на грань тетраэдра неопентилгликоль — формиат натрия — 25% водный раствор метанола при 30 °C (Фазовые области: I — L, II — L+S, III — LЭ+S+S1, IV — L+S1)
Рис. 25 Зависимость содержания формиата натрия от концентрации метанола в эвтонических растворах: 1 — система неопентилгликоль — формиат натрия — метанол — вода, 2 — система неопентилгликоль — формиат натрия — метанол — реакционная смесь
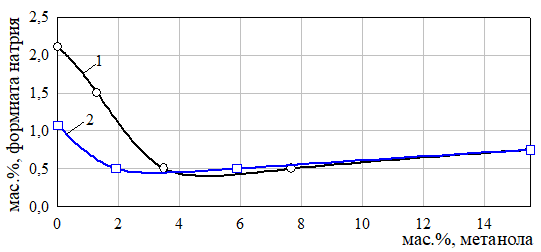
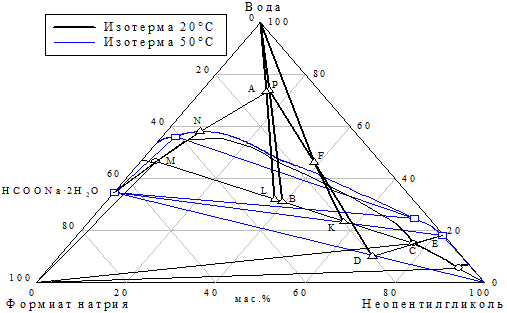
Рис. 26 Политерма растворимости системы неопентилгликоль — формиат натрия — вода
Таблица 6
Состав смесей процесса кристаллизации неопентилгликоля.
Точка на диаграмме. | Состав, мас.%. | |||
Неопентилгликоль. | Формиат натрия. | Вода /Вода + примеси. | ||
P. | 14.55. | 10.44. | 75.01. | |
В. | 39.68. | 29.82. | 30.50. | |
С. | 76.67. | 8.33. | 15.00. | |
М. | 3.42. | 50.08. | 46.50. | |
D. | 69.60. | 30.40. | ; | |
E. | 81.39. | 0.41. | 18.20. | |
F. | 38.87. | 15.02. | 43.11. | |
К. | 56.91. | 19.79. | 23.30. | |
N. | 7.50. | 34.50. | 58.00. | |
А. | 14.60. | 12.13. | 73.27. | |
L. | 37.14. | 30.86. | 32.00. | |
Выпавшую на последней стадии смесь неопентилгликоля и формиата натрия можно возвращать обратно в процесс — растворять в исходном растворе (синтезате), что приведет к снижению количества упариваемой воды и увеличению выхода неопентилгликоля. Необходимо добавить такое количество смеси неопентилгликоля и формиата натрия, чтобы полученный раствор стал практически насыщенным — фигуративная точка состава раствора F находится немного выше бинодали при 50 °C (рис. 26). Этот раствор упаривается при 50 °C до точки К (расположена на предельной ноде). Полученная смесь расслаивается, соотношение верхней и нижней фаз составляет 73.08: 26.92 соответственно. Далее процесс идет аналогично вышеописанному. Теоретический выход неопентилгликоля по данному циклу составляет 54.1%. Расчет показал, что количество получаемой смеси неопентилгликоля и дигидрата формиата натрия недостаточно для получения раствора точки F: необходимо 43.7 маcс.ч., а получили 21.16 мас.ч. Тем не менее, возврат выделившейся смеси неопентилгликоля и формиата натрия в процесс повышает выход неопентилгликоля и снижает количество выпариваемой воды. Справедливо предположить, что процесс будет выходить на оптимальный режим в течение нескольких циклов. Оптимальные условия осуществления процесса будут достигнуты тогда, когда количество возвращаемой в процесс смеси неопентилгликоля и формиата натрия будет равно количеству этой смеси, выделившейся при следующем цикле.
Нижнюю фазу состава точки М охлаждают до 20 °C. В результате в осадок выпадает дигидрат формиата натрия, а состав жидкой фазы изменяется по лучу MN до точки N. Соотношение выпавшего осадка соли и маточного раствора равно 49.1: 50.9 соответственно. Возможно возвращение этого раствора на первую стадию. При смешивании растворов соответствующих точкам Р и N получаем раствор состава точки А, который упариваем при 50 °C до точки L, лежащей на предельной ноде. Соотношение верхней и нижней фазы равно 46.15% (точка С) и 53.85% (точка М). Охлаждение верхней фазы до 20 °C приведет к кристаллизации смеси неопентилгликоля и дигидрата формиата натрия, а состав маточного раствора соответствует эвтоническому — точка E. Из нижней фазы состава точки М, охлажденной до 20 °C получаем дигидрата формиата натрия. Расчеты показали, что возврат в цикл маточного раствора после кристаллизации формиата натрия приводит к некоторому снижению выхода неопентилгликоля.
Система неопентилгликоль — формиат натрия — вода — метанол Графическое изображение процесса кристаллизации неопентилгликоля приведено на рисунке 27, состав исходной и промежуточных смесей — в таблице 7. При упаривании исходного раствора точки P его состав изменяется по лучу испарения до предельной ноды области расслаивания — точка B. Эта смесь распадается на две жидкие фазы. Соотношение фаз: верхняя (точка С) — 49.40%, нижняя (точка М) — 50.60%. Фазы разделяют при 30 °C.
Верхнюю фазу точка C снова упаривают. Ее состав изменяется по лучу испарения до точки K, при этом в осадок выпадает формиат натрия. Состав упаренного раствора соответствует эвтоническому раствору при 30 °C точка E. Соотношение выпавшей твердой фазы и эвтонического раствора равно 5.16: 94.84 соответственно. К получившемуся раствору добавляют метанол в количестве 0.23 мас.ч. чтобы получился эвтонический раствор разреза неопентилгликоль — формиат натрия — 10% водный раствор метанола. При этом должна выпасть в осадок смесь формиата натрия и неопентилгликоля. Состав эвтонического раствора (масс.%): неопентилгликоль — 83.5; формиат натрия — 1.5; вода — 13.5; метанол — 1.5. После обезвоживания этого раствора при 60 °C получается кристаллический неопентилгликоль. Теоретический выход целевого продукта в данном процессе составил 86.8%.
Система неопентилгликоль — формиат натрия — реакционная смесь — метанол Синтезат точка P (рис. 27, табл. 7) упаривается. Его состав изменяется по лучу испарения до предельной ноды — точка В1. Эта смесь распадается на две жидкие фазы. Состав верхней фазы определяется по диаграмме растворимости, а соотношение фаз и состав нижней фазы определяется по массе и показателю преломления соответственно: верхняя фаза (точка С1) — 40,3%, нижняя фаза (точка М1) 59,7%. Фазы разделяют. Верхнюю фазу — точка C1 снова упаривают. Ее состав изменяется по лучу испарения до предельной ноды — точка K1, при этом в осадок выпадает формиат натрия. Состав упаренного раствора соответствует эвтоническому раствору при 30 °C точка E1. Соотношение выпавшей твердой фазы и эвтонического раствора равно 3.76: 96.24 соответственно. К получившейся смеси добавляют метанол, чтобы получился эвтонический раствор разреза неопентилгликоль — формиат натрия — 10% водный раствор метанола. При этом в осадок выпадает смесь формиата натрия и неопентилгликоля. После фильтрации получаем эвтонический раствор состава (масс.%): неопентилгликоль — 80.5; формиат натрия — 0.5; реакционная смесь — 17.1; метанол — 1.9. При его обезвоживании получается кристаллический неопентилгликоль. Теоретический выход целевого продукта в данном процессе составил 69.3%.
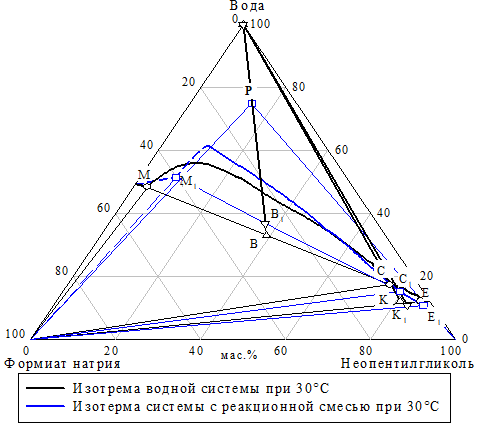
Рис. 27 Проекция разреза неопентилгликоль — формиат натрия — реакционная смесь на грань тетраэдра неопентилгликоль — формиат натрия — вода
Таблица 7.
Состав смесей процесса кристаллизации неопентилгликоля.
Точка на диаграмме. | Состав, масс.%. | |||
Неопентилгликоль. | Формиат натрия. | Вода /Вода + примеси. | ||
P. | 14.55. | 10.44. | 75.01. | |
В. | 39.01. | 27.99. | 33.00. | |
С. | 75.92. | 6.78. | 17.30. | |
М. | 3.25. | 48.35. | 48.40. | |
E. | 85.50. | 2.00. | 12.50. | |
В1. | 36.80. | 26.45. | 36.75. | |
С1. | 79.43. | 5.36. | 15.21. | |
М1. | 8.50. | 40.00. | 51.50. | |
E1. | 84.09. | 1.07. | 14.84. | |
Процессы кристаллизации неопентилгликоля осуществлены в лабораторных условиях с разными исходными растворами: трехкомпонентная смесь неопентилгликоля, формиата натрия и воды, соотношение компонентов соответствует реакционной смеси; реакционная смесь, полученная в результате синтеза неопентилгликоля из изомасляного альдегида и формальдегида в присутствии гидроокиси натрия.
1. Модельная водно-органическая смесь.
Материальный баланс процесса получения неопентилгликоля из модельного раствора приведен в таблице 8. Выход неопентилгликоля составил 63.8%, что на 23% ниже теоретического — 86.8%. Это связано с потерями маточного раствора на стадиях разделения фаз и фильтрации.
Таблица 8.
Материальный баланс процесса получения неопентилгликоля.
из модельного раствора.
Приход. | Расход. | |
1 стадия. Упаривание раствора. | ||
Исходный раствор (точка P) — 500 г, nD30°=1.3610. | Упаренная вода — 313.5 г Концентрированный раствор (точка В) — 186.5 г. | |
2 стадия. Расслаивание. Разделение фаз*. | ||
Концентрированный раствор (точка В) — 186.5 г. | Верхняя фаза (точка С) — 68.33 г, nD30°=1.4280. Нижняя фаза (точка М) — 113.35 г, nD30°=1.3945. Потери — 4.82 г. | |
3 стадия. Упаривания органической верхней фазы. | ||
Верхней фазы (точка С) — 68.33 г, nD30°=1.4280. | Упаренная вода — 4.41 г Концентрированный раствор (точка Е) — 60.62 г Осадок формиата натрия — 3.3 г. | |
4 стадия. Добавление метанола к эвтоническому раствору и фильтрация получившейся смеси. | ||
Концентрированный раствор (точка Е) — 60.62 г Осадок — 3.3 г Метанол — 0.9 г. | Эвтонический раствор системы неопентилгликоль — формиат натрия — 10% водный раствор метанола — 55.62 г Осадок — 3.7 г Потери — 2.2 г. | |
5 стадия. Кристаллизация неопентилгликоля. | ||
Эвтонический раствор системы неопентилгликоль — формиат натрия — 10% водный раствор метанола — 55.62 г. | Кристаллический неопентилгликоль — 46.44 г. | |
- *Примечание: разделение фаз проводили при температуре 45 °C, т.к. повышение температуры ускорило коалесценцию фаз.
- 2. Водно-органическая смесь — реакционная смесь.
Синтез неопентилгликоля проведен следующим образом. 170 г формальдегида (содержание основного вещества 37 мас.%), 72 г изомасляного альдегида, 230 г раствора гидроокиси натрия (концентрация 20−21 мас.%) и 200 г воды выдерживались в течение 3 часов при температуре 60 °C и постоянном перемешивании, после чего в раствор добавляли 14 мл муравьиной кислоты (концентрация 99.7 мас.%).
Материальный баланс процесса получения неопентилгликоля приведен в таблице 9. Выход неопентилгликоля составил 73.4%, что на 4.1% выше теоретического выхода (69.3%). Это связано с тем, что при введении метанола на 4 стадии вместо смеси формиата натрия и неопентилгликоля кристаллизуется только формиат натрия.
Таблица 9.
Материальный баланс процесса получения неопентилгликоля из реакционной смеси.
Приход. | Расход. | |
1 стадия. Упаривание раствора. | ||
Исходный раствор (точка P) — 500 г, nD30°=1.3660. | Упаренная вода — 304.55 г Концентрированный раствор (точка В1) — 195.45 г. | |
2 стадия. Расслаивание. Разделение фаз*. | ||
Концентрированный раствор (точка В1) -195.45 г. | Верхняя фаза (точка С1) — 77.78 г, nD30°=1.4295. Нижняя фаза (точка М1) — 113.79 г, Потери — 3.88 г. | |
3 стадия. Стадия упаривания органического верхней фазы. | ||
Верхняя фаза (точка С1) — 77.78 г,. nD30°=1.4310. | Упаренная вода — 4.67 г Концентрированный раствор (точка Е1) — 69.59 г Осадок формиата натрия — 3.52 г. | |
4 стадия. Добавление метанола к эвтоническому раствору и фильтрация получившейся смеси. | ||
Концентрированный раствор (точка Е1) — 69.59 г Осадок — 3.52 г Метанол — 1.16 г. | Эвтонический раствор системы неопентилгликоль — формиат натрия — 10% раствор метанола в реакционной смеси — 66.3 г Осадок — 5.3 г Потери — 2.67 г. | |
5 стадия. Кристаллизация неопентилгликоля. | ||
Эвтонический раствор системы неопентилгликоль — формиат натрия — 10% раствор метанола в реакционной смеси — 66.3 г. | Кристаллический неопентилгликоль — 53.37 г. | |
*Примечание: разделение фаз проводили при температуре 38 °C, т.к. повышение температуры ускорило коалесценцию фаз.
Полученные экспериментальные данные достаточно хорошо согласуются с теоретическими расчетами на основании диаграмм растворимости поликомпонентных систем. Данные таблиц 8 и 9 дают важную информацию о возможных потерях маточного раствора с твердой фазой на стадии фильтрации и при разделении двух жидких фаз. Они составили не более 1.4%, что вполне допустимо с точки зрения дальнейшего осуществления процесса на опытной установке.
Полученные осадки неопентилгликоля анализировались на содержание формиата натрия путем определения зольности. Содержание формиата натрия в неопентилгликоле полученного из водной системы составляет 0.6 масс.%, а из реакционной смеси — 0.3 масс.%. Этот продукт может найти широкое применение при получении органоминеральных, наноструктурированных композиционных материалов [33,34].
Из нижней фазы может быть получен безводный формиат натрия путем изотермической кристаллизации или кристаллогидрат путем политермической кристаллизации.
На основании выполненных исследований предложена принципиальная схема получения неопентилгликоля и формиата натрия путем кристаллизации (рис. 28).
Заключение
Лабораторные эксперименты позволили установить ряд особенностей предлагаемого процесса:
- 1. Теоретически при упаривании органической фазы и после добавления метанола в осадок должны выпадать как формиат натрия, так и неопентилгликоль, однако эксперимент показал, что неопентилгликоль не выпадает в осадок, а остается в растворе, поскольку это вещество склонно к образованию пересыщенных растворов, что снижает его потери в процессе.
- 2. Разделение двух жидких фаз происходит значительно быстрее при повышении температуры до 35−45°C.
- 3. Маточные растворы, которые остаются после выделения неопентилгликоля и формиата натрия можно возвращать в голову процесса на стадию упаривания. Возврат маточных растворов не влияет на выход неопентилгликоля.
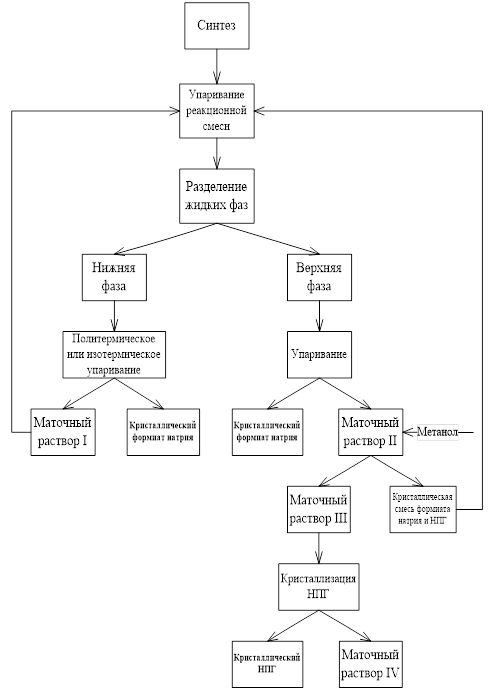
Рис. 28 Принципиальная технологическая схема получения НПГ и формиата натрия
- 1. Berlow, E. The pentaerythritols. N.Y.: Reinhold Publ. Corp., 1958. 387 p.
- 2. Рудковский, Д. М. Многоатомные спирты. Л.: Химия, 1972. 168 с.
- 3. Викторов, М. М. Графические расчеты в технологии неорганических веществ — 3-е изд., перер. и доп. Л.: Химия, 1972. 464 с.
- 4. Котельникова, М.В. Физико-химические основы процессов извлечения неопентилгликоля из водно-органических смесей. Дис… канд. хим.наук. Пермь, 2010. 131 с.
- 5. Губина (Котельникова), М.В. Физико-химические основы выделения неопентилгликоля из реакционной смеси // Отчетная научная конференция студентов и аспирантов Пермского государственного университета: материалы конф. Пермь: издательство ПГУ, апрель 2003. С. 17.
- 6. Котельникова, М.В. Физико-химические основы процесса кристаллизации неопентилгликоля из водно-органических смесей // Студент и научнотехнический прогресс: материалы XLIII международной научной студенческой конференции. Новосибирск, 2005. С. 87−88.
- 7. Котельникова, М.В. Физико-химические основы процессов выделения неопентилгликоля и формиата натрия из водно-органических смесей // Проблемы химия и экология: тезисы докладов областной конференции студентов и молодых ученых. Пермь, 2005. С. 21−22.
- 8. Котельникова, М.В. Физико-химические основы процессов кристаллизации полиолов. Экологический аспект // Эколого-экономические проблемы освоения минерально-сырьевых ресурсов: тезисы докладов Международной научной конференции. ФГНУ «ЕНИ» и др. Пермь, 2005. С. 43−44.
- 9. Кудряшова, О.С. Физико-химический анализ — теоретическая основа энергосберегающих и экологически мягких химических технологий // Высокие технологии, фундаментальные и прикладные исследования, образование: сб. тр. Санкт — Петербург, 2005. С. 130−131.
- 10. Котельникова, М.В. Физико-химические основы процессов разделения веществ в водно-органических системах // XV международная конференция по химической термодинамике в России. — Москва, 2005. — С. 18.
- 11. Самохвалов, И. И. Оптимизация процессов кристаллизации дипентаэритрита и неопентилгликоля на основе диаграмм растворимости многокомпонентных систем // Актуальные проблемы химической науки, практики и образования. Курск, 2009. С. 234−236.
- 12. CAS 126−30−7. Neopentyl Glycol (Neo). Data Sheet. — Perstorp Specialty Chemicals. inchem.org/documents/sids/sids/126 307.pdf
- 13. ТУ 2432−011−203 803−98. Натрий муравьинокислый (натрия формиат) HCOONa. — Предприятие-изготовитель: ОАО «Метафракс». metafrax.ru/ru/product-list/natriy-formiat/
- 14. ГОСТ 6709–72. Вода дистиллированная. Технические условия. М.: Стандартинформ, 2007. 11 с.
- 15. ГОСТ 8981–78. Эфиры этиловый и нормальный бутиловый уксусной кислоты технические. Технические условия. 18 с.
- 16. ГОСТ 2222–95. Метанол технический. Технические условия. М.: ИПК Изд-во стандартов, 2000. 19 с.
- 17. Никурашина, Н. И. Метод сечений. Приложение его к изучению многофазного состояния многокомпонентных систем. Саратов: Саратовский ун-т, 1969. 122 с.
- 18. Мерцлин, Р. В. Приложение метода сечений к определению равновесий в трехкомпонентных системах с твердыми фазами // Журн. общей химии. 1940. Т. 10. Вып. 22. С. 1999;2004.
- 19. Журавлев, Е. Ф. Изучение растворимости в водно-солевых системах графоаналитическим методом сечений // Журн. неорганической химии. 1960. Т. 5. Вып. 11. С. 2630−2637.
- 20. Иоффе, Б. В. Рефрактометрические методы химии — 3-е изд. Л.: Химия, 1983. 350 с.
- 21. ГОСТ 9286–89 Пентаэритрит технический. Технические условия — М.: ИПК Изд-во стандартов, 1998. 12 с.
- 22. Кудряшова, О. С. Изучение растворимости в многокомпонентных системах, содержащих неопентилгликоль и органические растворители // Химия и химическое образование: сб. тр. 3-го международного симпозиума. — Владивосток: Дальневосточный университет, 2003. С. 152−154.
- 23. Губина (Котельникова), М. В. Изучение растворимости в многокомпонентных системах, содержащих неопентилгликоль и органические растворители // Химия и экология: тезисы докладов областной конференции студентов и молодых ученых. Пермь, 2003, с. 47−48.
- 24. Трейбал, Р. Жидкостная экстракция / Перевод с англ. Ю. Н. Ковалева, В. Г. Труханова, под ред. С. З. Кагана. М.: Химия, 1966. 724 с.
- 25. Ильин. К. К. Топология фазовых диаграмм трехи четырехкомпонентных систем с равновесиями конденсированных фаз: дис. … докт. хим. наук: 02.00.04 / Константин Кузьмич Ильин. Саратов, 2000. 383 с.
- 26. Мерцлин, Р.В. О кристаллизации тройных систем с двумя двойными расслаиваниями // Изв. Сектора ФХА ИОНХ. 1949. Т. 18. С. 33−59.
- 27. Котельникова, М. В. Растворимость систем неопентилгликоль — формиат натрия — метанол — вода // Ж. физ. Химии, 2006. Т. 80, Вып. 11. С. 1−6.
- 28. Губина (Котельникова), М. В. Изучение растворимости в многокомпонентных системах, содержащих неопентилгликоль и метанол // Молодежная наука Прикамья: сб. науч. тр. — Пермь: ПГТУ, 2004. С. 71−75.
- 29. Губина (Котельникова), М. В. Изучение растворимости в многокомпонентных системах, содержащих неопентилгликоль и метанол // Проблемы химия и экология: тезисы докладов областной конференции студентов и молодых ученых. Пермь, 2004. С. 51−52.
- 30. Губина (Котельникова), М. В. Изучение растворимости в системе неопентилгликоль — формиат натрия — метанол — вода // Современное состояние и приоритеты развития фундаментальных наук в регионах: тезисы докладов Всероссийской научной конференции молодых ученых и студентов. Краснодар: издательство Просвещение. Юг, 2004. Т. 2. С. 133.
- 31. Котельникова, М. В. Изучение влияния технологических примесей и метанола на процесс кристаллизации неопентилгликоля и его чистоту // Проблемы теоретической и экспериментальной химии: тезисы докладов XV Российской студенческой научной конференции, посвященной 85-летию Уральского государственного университета им. А. М. Горького. — Екатеринбург, 2005. С. 339.