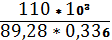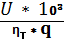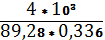1 — ячейка; 2 — анод; 3 — электролит; 4 — жидкий алюминий; 5 — катод; 6 — токоподвод; 7 — изоляционный материал; 8 — корпус.
Рисунок 4 — Электролитическая ячейка для получения алюминия
Электрохимическая ячейка представляет собой стакан (1), помещенный в силитовую печь. В стакане устанавливается графитовая пластина, служащая катодом (5), ток к которому подводится с помощью токоподводов (6) из нержавеющей стали, защищенных от воздействия расплава слоем защитной обмазки. Сверху в ванну вводится анод (2) с ввинченными в него токоподводом. В стенке ячейки имеется канал для установки термопары.
В начале опыта в ячейку загружается криолито-глиноземная смесь с 10% глинозема. В расплавленный электролит вводится точно взвешенное количество алюминия, устанавливается анод и по достижении заданной температуры включается постоянный ток. В течение опыта через каждые 15 мин. необходимо фиксировать следующие величины: напряжение и силу переменного тока, температуру, напряжение на ячейки и силу постоянного тока, обратную Э.Д. С. Опыт должен продолжаться (23)часа при силе постоянного тока (1520) А.
По окончании опыта проводятся следующие операции: поднимается анод, отключается постоянный ток, снимаются показания счетчиков переменного и постоянного тока. Анод извлекается из ячейки, охлаждается, снимается с токоподводящего стержня и взвешивается. По разности веса анода до и после опыта определяется фактический расход углерода. Внутренний стакан за тяги извлекается из печи и электролит вместе с алюминием выливается в чугунную изложницу. После кристаллизации электролита и металла сплав разбивается, металл отделяется от соли и взвешивается. По привесу алюминия определяется выход по току. Снятые и расчетные данные заносят в таблицу 1.
Таблица 1 — Результаты опыта.
|
Время, час. | Сила тока, А. | Напряжение, В. | t,. | Обратная Э.Д.С. | Расход углерода. | Выход по току, %. | Удельный расход электроэнергии, кВт*ч/кг. | Выход по энергии, г/КВт*ч. |
Переменного. | Постоянного. | На ячейке. | На печи. | г/(А*ч). | г/г. | Переменного. | Постоянного. |
| | | | | | 1,5. | 0,038. | 0,19. | 89,28. | 336,69. | 13,33. | 75,01. |
Находим выход по току:
?т = mп/mт = 9 / 10,08 * 100% = 89,28%.
Находим удельный расход электроэнергии: — переменный:
W = = = 336,69 кВт*ч/кг;
— постоянный:
W = = = 13,33 кВт*ч/кг.
Находим выход по энергии:
?э = * 106 = 75,01 г/КВт*ч.
Вывод: Получили алюминий электролизом глинозема, растворенного в расплавленном электролите, выход по току составил 89,28%.