Условия минимальной диссипации для конкретных процессов

Деформационное взаимодействие Пусть две термодинамические подсистемы разделены поршнем. В этом случае функции g (ul5 и2) соответствует зависимость скорости перемещения поршня v от давлений р1 и р2 контактирующих подсистем. В большинстве случаев скорость зависит только от разности давлений (р: -р2), так что производство энтропии можно записать как. Если a (v) выпукла вниз, то оптимальная скорость… Читать ещё >
Условия минимальной диссипации для конкретных процессов (реферат, курсовая, диплом, контрольная)
Конкретезируем условия минимальной диссипации для некоторых термодинамических процессов. При этом ключевые процессы тепло и массопереноса будут рассмотрены подробнее в отдельных разделах с приложением к конкретным технологическим системам.
Теплообмен Управляющей интенсивной переменной будем для определенности считать температуру нагреваемого тела. Движущая сила X в задаче о минимальной диссипации процесса теплопереноса равна.
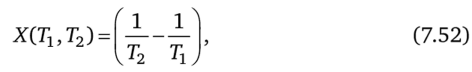
а поток теплоты q (T1} Т2). Функция ф в условиях (8.6), определяет скорость изменения температуры Т1. В большинстве случаев можно считать, что.
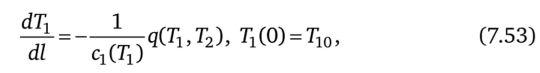
где CjCTi) — теплоемкость горячего источника. Для процесса, протекающего во времени, с сосредоточенными параметрами горячего источника аргумент I имеет смысл времени, a L — продолжительности процесса. Для трубчатого теплообменника, в котором температура горячего потока меняется от сечения к сечению, величина с представляет собой водяной эквивалент потока (произведение его расхода на удельную теплоемкость), a L — длину теплообменника.
В соответствии с условиями (7.17), (7.18), (7.11) минимальной диссипации при заданной средней интенсивности теплового потока q для процесса теплообмена получим условия минимальной диссипации для произвольного закона теплопереноса:
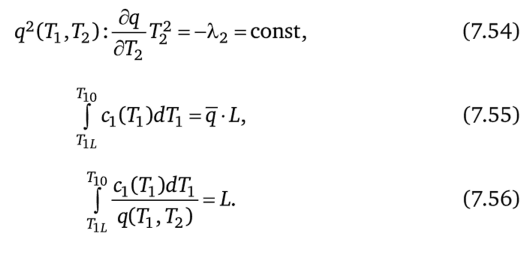
Первое из этих условий определяет Т20!Д2), второе — T1L, а третье — константу Х2.
Рассмотрим в качестве примера использования условий (7.54) — (7.56) ньютоновский закон теплопереноса.

с постоянной теплоемкостью (водяным эквивалентом) с. Из условий (7.54)—(7.56) получим.
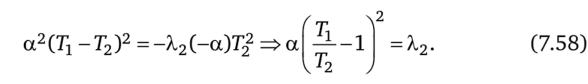
Таким образом, в процессе минимальной диссипации для любого I отношение Т1/Т2 должно быть постоянно и равно.

Из (7.55) следует, что Тц ~ Т10 -qL/c; наконец, из условия (7.56) вытекает, что Минимальное производство энтропии, получаемое после подстановки (7.59), (7.60) в выражение.
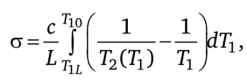
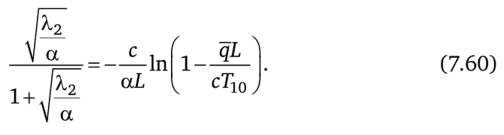
равно.
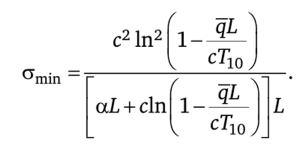
Отметим, что в процессе минимальной диссипации для ньютоновского теплообмена производство энтропии в каждом сечении теплообменника или в каждый момент времени одинаково.
Для более общего закона теплопереноса вида.

условия (7.54) примут форму 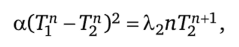 или.
или.
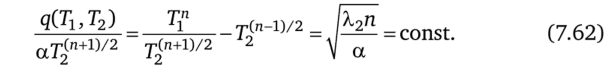
В частности, для лучистого теплообмена, когда поток пропорционален разности четвертых степеней температур, условие минимальной диссипации имеет вид.

В общем случае из условия (7.62) следует, что при п > -1 тепловой поток с ростом температуры Т2 растет, а при п < -1 — падает. При п = = -1 (закон теплообмена Фурье) тепловой поток, соответствующий минимальной диссипации, постоянен и равен q, а само минимальное производство энтропии, подсчитанное по формуле (7.5), равно.

При этом для п = -1 минимуму диссипации и постоянству потока теплоты соответствует постоянство производства энтропии в каждом сечении теплообменника или для каждого момента времени, как и для ньютоновского теплообмена.
На первый взгляд кажется, что для любого термодинамического процесса минимальной диссипации производство энтропии, а равномерно распределено по времени или по поверхности контакта. Если бы это было справедливо, то сильно упростило бы все расчеты. Но оказывается, что далеко не всегда в процессе минимальной диссипации производство энтропии постоянно. Ниже получено условие, выделяющее те термодинамические процессы, для которых это свойство справедливо.
Изотермический массоперенос Интенсивными переменными подсистем в этом случае являются векторы концентраций Q (i = 1, 2) с составляющими Cik, характеризующими состав подсистем. Как потоки веществ, так и химические потенциалы зависят от концентраций. В выражении (7.2) потоки и движущие силы имеют вид.
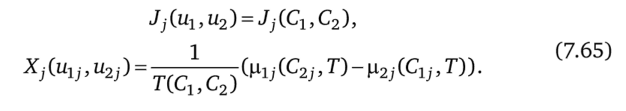
Остановимся на случае, когда из одной подсистемы в другую переходит только один ключевой компонент. При этом давление в подсистеме вследствие диффузии не изменяется. Концентрация ключевого компонента в первой подсистеме задана, а так как задан средний поток g

то и конечный состав фиксирован. Минимизация диссипации сводится к минимизации среднего производства энтропии, возникающего вследствие диффузии:
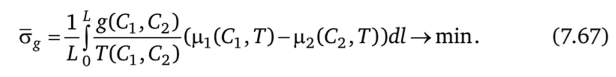
Чтобы получить зависимость от Сх и С2 скорости изменения концентрации, необходимо учесть, что поток g меняет как состав первой подсистемы, так и общее количество вещества G1 в ней, так как это поток лишь одного (ключевого) компонента. По условиям материального баланса.
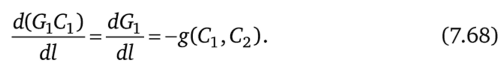
Из уравнения (7.68) следует, что 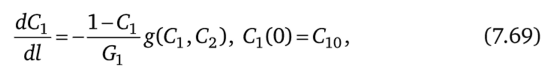 а.
а.
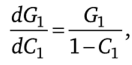
откуда.
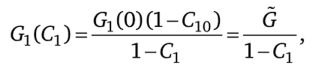
где G — количество инертного компонента в первой подсистеме. После подстановки G1(C1) в (7.69) получим.
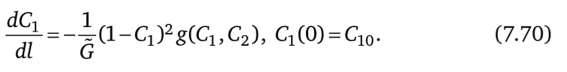
Общие условия минимальной диссипации (7.17), (7.18) примут форму.
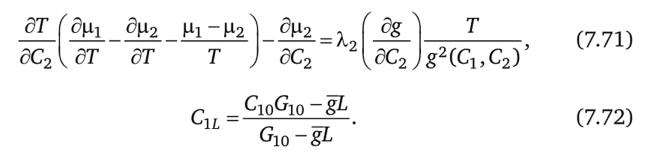
Для химических потенциалов вида.
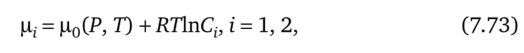
дц2 RT Л
производная —— =—, так что условия (7.71) перепишем как дС2 С2 
Константу Х2 находят из условия.
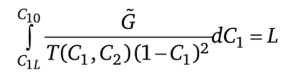
после подстановки в него решения С2(Сг, Х2) уравнения (7.74).
Особенно простое решение соответствует случаю, когда поток диффузии пропорционален разности химических потенциалов и температура Т постоянна:
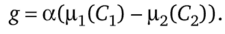
В этом случае из (7.71) следует, что поток массопереноса постоянен:
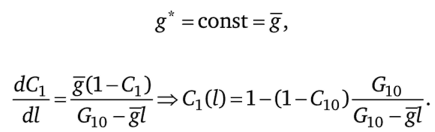
Для химических потенциалов в форме (7.73) постоянству потока соответствует постоянство отношения концентраций.
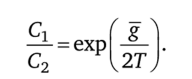
Минимальное производство энтропии при этом.
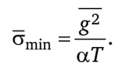
Деформационное взаимодействие Пусть две термодинамические подсистемы разделены поршнем. В этом случае функции g (ul5 и2) соответствует зависимость скорости перемещения поршня v от давлений р1 и р2 контактирующих подсистем. В большинстве случаев скорость зависит только от разности давлений (р: -р2), так что производство энтропии можно записать как.
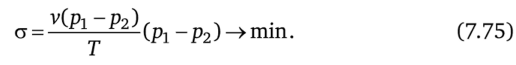
Среднее значение этой величины минимизируют при заданном среднем значении скорости v:
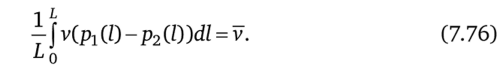
Выражая Ар =Р] -р2 через v как Ap (v), можно записать усредненную задачу о минимуме диссипации как.
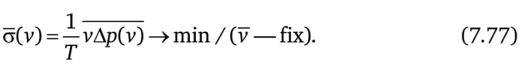
Если a (v) выпукла вниз, то оптимальная скорость должна быть постоянна и равна v. В противном случае решению усредненной задачи нелинейного программирования (7.77) соответствует ордината выпуклой оболочки функции o (v) для v = v. Скорость в этом последнем случае принимает не более двух значений v1 и v2, определяемых условиями.
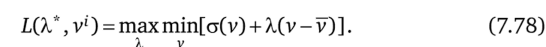
Значения функции L в точках v' (i = 1, 2) одинаковы. Долю у периода L, в течение которой v*(0 = v1, находят из условия.
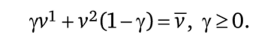
Дросселирование Рассмотрим процесс расширения газа, проходящего через сужающее устройство. Обозначим рг и р2 давление до и после сужающего устройства, a g (.pb р2) — расход газа и предположим, что процесс происходит изотермически, т. е. температура не изменяется. Производство энтропии.
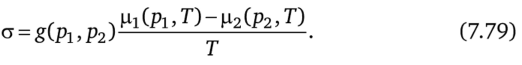
Для идеального газа выражение (7.79) примет форму.

Пусть рг —давление в замкнутой емкости объемом V, оно снижается при истечении газа через сужающее устройство. Заданы продолжительность процесса т и средний поток g. Требуется минимизировать диссипацию:
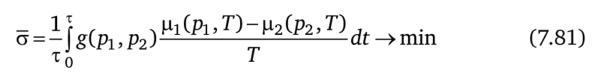
при условиях.
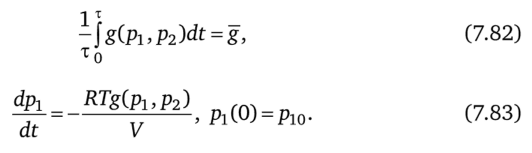
Из общих условий (7.17), (7.18) для этой задачи получим соотношения.
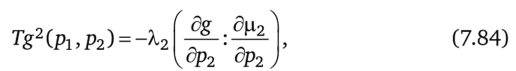

Для идеального газа и зависимости 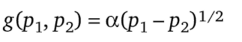 условие (7.84) приводит к соотношению.
условие (7.84) приводит к соотношению.
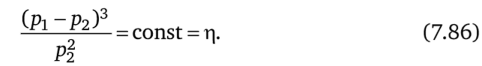
Подстановка условия (7.86) в уравнения (7.81) и (7.83) позволяет найти оптимальный закон изменения р2 (О и минимальное производство энтропии amin.
Оптимальный закон изменения давления определяется после решения уравнений (7.83), (7.86) с точностью до константы т:
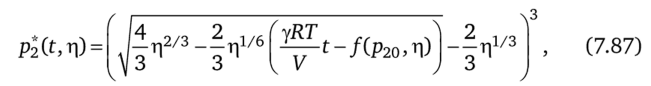
где.
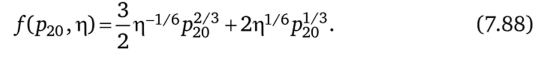
Так как равенство (7.86) справедливо и для начальных значений давления, то величина р20 удовлетворяет уравнению.

Минимальное производство энтропии после подстановки этих выражений в (7.81) равно.
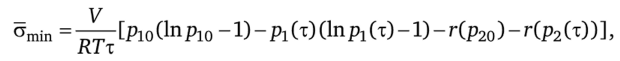
где.
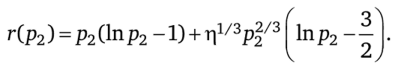
Кристаллизация Производство энтропии в процессе кристаллизации, как в любом процессе массопереноса, выражается формулой.
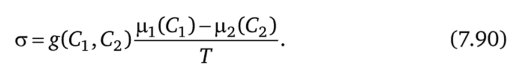
Для идеальных растворов химический потенциал кристаллизирующегося вещества в растворе при постоянных температуре и давлении зависит от его концентрации Ср
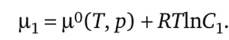
Потенциал ц2 определяется равновесной концентрацией С2 = С: 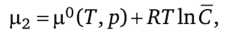 так что.
так что.

Поток g зависит от поверхности кристаллов F, которая в свою очередь определяется массой кристаллов М. Для линейной кинетики масса изменяется в соответствии с уравнением.
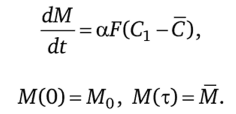
Если размеры и форма кристаллов при t = О одинаковы, то.

Коэффициент К зависит как от коэффициента массопередачи, так и от формы кристалла.
Задача о минимуме диссипации в процессе кристаллизации примет форму.
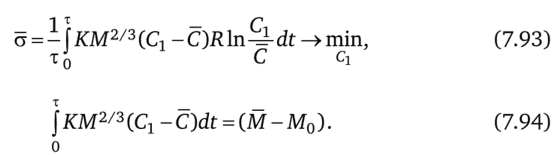
Условия оптимальности этой задачи вытекают из общих условий (7.17), (7.18) и имеют вид.
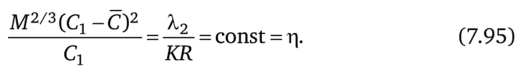
Из условий (7.95) и уравнения (7.92) получим дифференциальное уравнение, которое с точностью до константы г = г определяет C*(t). Для этого заменим МиМ через С1иС1:
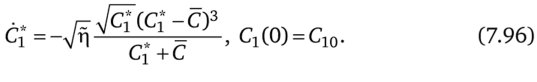
Нетрудно видеть, что для случая, когда начальные массы кристаллов различны, использование уравнения (7.92) для средней начальной массы дает (в силу выпуклости вверх зависимости поверхности от М) оценку снизу для производства энтропии.
Химические превращения Кинетика химических превращений очень разнообразна. Поэтому покажем использование общих условий минимальной диссипации на конкретном примере.
Рассмотрим изотермический приодически действующий реактор идеального смешения, в котором протекает реакция вида.
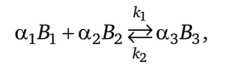
где ос, — стехиометрические коэффициенты; Bf — реагенты; kt — константы прямой и обратной реакций. Далее будем считать, что а: < О, а2 < 0, а3 > 0. Скорость реакции определяется законом действующих масс:
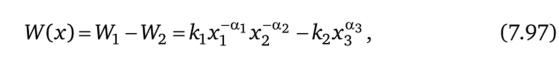
где Xj = ^ —-молярная доля i-ro компонента; щ — количество молей.
1-го компонента в аппарате; N (t) =.
Производство энтропии '.

где.
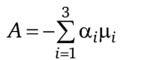
— химическое сродство реакции.
Для идеальных растворов.
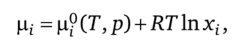
откуда.
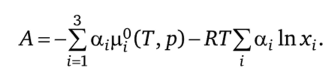
Первое слагаемое в этом выражении равно[1]
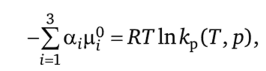
где константа равновесия кр представляет собой отношение констант скоростей прямой и обратной реакций:
Таким образом, 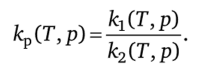
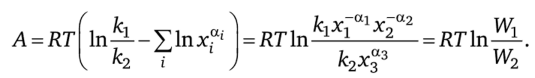
Пусть задана средняя скорость реакции.

а скорость реакции W (t) является управлением. Она определяет изменение степени превращения.

и скорость изменения числа молей каждого из компонентов в ходе реакции Отсюда 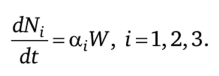
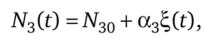
а общее количество молей 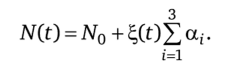 Скорость обратной реакции.
Скорость обратной реакции.
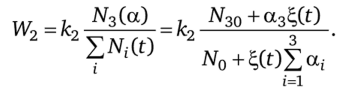
С учетом сказанного задача о минимуме диссипации примет вид.
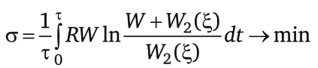
при условиях.
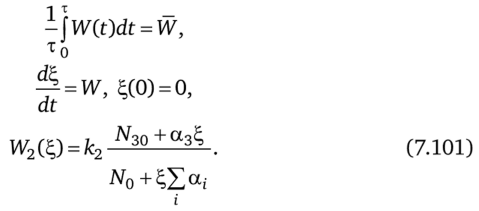
Используя замену переменных dt=f, запишем функцию Лагранжа:
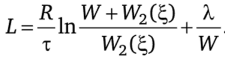
Из условия стационарности L по W получим.
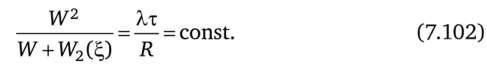
Это требование вместе с уравнением (7.100) и условием на среднее значение W позволяет найти W*(t), ?*(t) и оценку для производства энтропии.
Для некоторых процессов условия минимальной диссипации и полученные из них выражения для минимального производства энтропии приведены в табл. 7.1.
Таблица 7.1
Условия минимальной диссипации термодинамических процессов.
Процесс | Условия минимальной диссипации и производство энтропии |
Теплообмен q = a (T2-T1) |  |
Векторный поток J = LX |  |
Односторонний изотермический массоперенос g (c 1, с2) =. = fc (Cl(Z)-c2 (0). |  |
Процесс | Условия минимальной диссипации и производство энтропии |
Двусторонний изотермический эквимолярный массоперенос. |  |
- [1] Бошнякович Ф. Техническая термодинамика. Т. 2. М.: Госэнергоиздат, 1956.