Элементы группы IVВ

Титан очень устойчив по отношению к кислотам. Устойчивость титана связана со свойствами его поверхности, так как по значению редокс-потенциала (<�р° = -0,91 В) титан является активным металлом. При нагревании титана с концентрированной соляной кислотой образуется раствор соли Т1С13 фиолетового цвета. Это пример возникновения окрашенного вещества при наличии на-подуровне хотя бы одного электрона… Читать ещё >
Элементы группы IVВ (реферат, курсовая, диплом, контрольная)
Группа 1УВ состоит из четырех (/-элементов с четными атомными номерами: титан 22Ть цирконий 402 г, гафний 72Н1 и резерфордий 104К1 (табл. 27.4).
Таблица 27.4
Характеристика элементов группы 1УВ.

Последний элемент впервые получен в 1964 г. в Дубне, и его предлагалось назвать курчатовий в честь академика, руководителя работ по атомной науке и технике в СССР И. В. Курчатова, но было принято название резерфордий. Этот элемент был идентифицирован на препаратах, содержавших лишь до 20 атомов. Удалось установить, что это аналог гафния, а не актиноидов. Самый долгоживущий изотоп резерфордия имеет период полураспада 66 с.
Титан имеет пять стабильных изотопов, из которых самый распространенный — (73,8%). У циркония четыре стабильных изотопа и один радионуклид -{[^г с /½ > 3,6• 1017 лет. Самый распространенный изотоп 4{)2г (51,5%). Гафний имеет шесть стабильных изотопов, из которых по распространенности преобладает (35,1%).
Титан по относительному содержанию в земной коре стоит па 10-м месте, а среди (/-элементов оказывается на втором месте после железа. Однако из-за трудности отделения титана от сопутствующих элементов его долгое время считали редким элементом. Важнейшими минералами титана являются титаномагнетиты ЕеТЮ3-иЕе304, ильменит ГеТЮ3, сфен СаТ18Ю5 и рутил ТЮ2. Крупные месторождения титановых руд имеются на Урале. Титан в виде оксида был открыт У. Грегором (1791 г., Англия) и, независимо от него, М. Клапротом (1795 г., Германия).
Цирконий тоже относится к достаточно распространенным химическим элементам. Основные руды циркония циркон 2г8Ю4 и бадделеит Zг02. Гафний, чрезвычайно близкий по свойствам к цирконию, в природе всегда сопутствует цирконию, и технология их разделения очень сложна. Цирконий был открыт М. Клапротом (1789 г., Германия). Гафний оказался предпоследним по времени открытия (1923 г., Д. Костер, Д. Хевеши, Дания) из стабильных элементов, имеющихся в земной коре.
Таблица 27.5
Физические свойства металлов 1УВ.
Свойство. | Металл. | ||
титан. | цирконий. | гафний. | |
Плотность, г/см3 | 4,540. | 6,506. | 13,31. |
t °г. 1п.ч> | |||
; о о. | |||
Электрическое сопротивление, Ом м (при 273 К). | 42• 10″ 8 | 42,1 Ю" 8 | 35,1 10 8 |
Титан, цирконий и гафний в виде металлов похожи на сталь, имеют высокие температуры плавления и кипения и относительно невысокую электропроводность (табл. 27.5).
Лишь в XX в. были по достоинству оценены конструкционные свойства титана. Он пластичен и хорошо поддается механической обработке, обладает коррозионной стойкостью и жаропрочностью. Он нашел широкое применение в авиации, ракетостроении и судостроении. Нашли применение и простые хозяйственные инструменты из титана. Можно считать пророческим название титан, данное этому элементу в конце XVIII в. Производство титана превышает 100 000 т в год.
Широкое применение нашел и цирконий в чистом виде в ядерной технике, а также в сплавах с магнием, алюминием и другими металлами. Цирконий совместим с биологическими тканями и может применяться для изготовления искусственных суставов. Есть представление о том, что ношение циркониевого браслета стабилизирует артериальное давление. Мировое производство соединений циркония достигает 1 млн т в год. Из данных табл. 27.4 следует, что примесь гафния в цирконии составляет около 3%. Если бы весь этот гафний был выделен в виде чистых соединений при производстве циркония, то их масса составила бы приблизительно 30 000 т. Фактически производство гафния составляет около 60 т/год.
Титан, цирконий и гафний проявляют типичные свойства ^/-элементов. Электронная структура титана показана в параграфе 208. Титан и цирконий в химических соединениях имеют СО +2, +3 и +4. От титана к гафнию повышается устойчивость высшей СО. Для гафния становится не характерной СО +2.
При переработке титановых руд сначала получается оксид титана ТЮ2. Это вещество, как и оксиды ряда других металлов, восстанавливается углем, но для получения титана этот метод не применяется, так как одновременно с металлом образуется карбид титана, ухудшающий его свойства. Поэтому оксид титана превращают в хлорид ТЮ14 действием хлора на раскаленную смесь оксида и угля:

Хлорид титана (1У) представляет собой бесцветное вещество, плавящееся при 23 °C и кипящее при 137 °C. Это пример галогенида металла с молекулярной структурой, который в силу этого не относится к классу солей. Хлорид титана (1У) восстанавливают в атмосфере аргона до металла магнием:
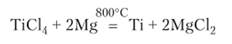
Титан очень устойчив по отношению к кислотам. Устойчивость титана связана со свойствами его поверхности, так как по значению редокс-потенциала (<�р° = -0,91 В) титан является активным металлом. При нагревании титана с концентрированной соляной кислотой образуется раствор соли Т1С13 фиолетового цвета. Это пример возникновения окрашенного вещества при наличии на-подуровне хотя бы одного электрона. Действительно, электронная структура иона Тг3+ [Аг]3^/1. Под действием 50%-ной серной кислоты титан образует смесь двух сульфатов — Т1504 и Т]2(504)3. При этом выделяется водород.
В высшей СО титан проявляет амфотерность. При нагревании титана с расплавленной щелочью в атмосфере кислорода образуется титанат:
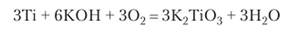
При обычной температуре титан не реагирует с водой, кислородом, углекислым газом, водными растворами солей. Он устойчив к действию морской воды. При нагревании реагирует со многими неметаллами. В пылеобразном состоянии как титан, так и цирконий пирофорны, т. е. воспламеняются от искр.
В растворах соединения ТКИ!) легко окисляются до ТлПУ):

Все элементы группы 1УВ образуют комплексные соединения. Титан и цирконий образуют комплексные фториды при реакции с плавиковой кислотой:
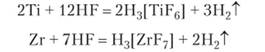
У циркония и гафния возможны координационные числа, превышающие 6. Например, известна комплексная соль Ыа4[ШР8].