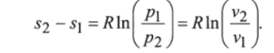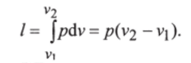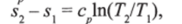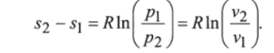Изобарным называется процесс, происходящий при постоянном давлении. Из уравнения состояния идеального газа при
р = const находим:
или т. е. в изобарном процессе объем газа пропорционален его абсолютной температуре (закон Гей-Люссака). На рис. 2.7 изображены графики процесса в p, v и Г^-диаграммах.
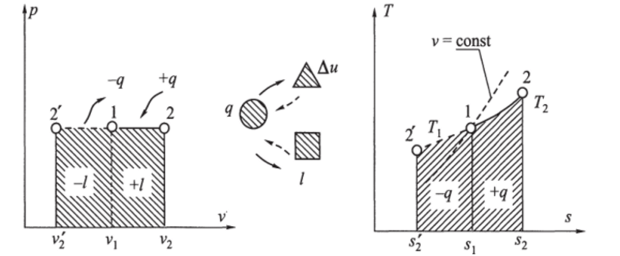
Рис. 2.7. Изобарный процесс вp, vи Г, л-диаграммах и схема энергобаланса.
Из выражения (2.2) следует, что:
Так как pvx = RTy и pv2 = RTV то одновременно.
1 = R (T2 — Г,).
Количество теплоты, сообщаемое газу при нагревании (или отдаваемое им при охлажденииV нахолим из /павнения: 
Изменение энтропии при сп = const равно.
т.е. температурная зависимость энтропии при изобарном процессе тоже имеет логарифмический характер, но поскольку с > cv, то изобара в 7>- диаграмме идет более полого, чем изохора.
Изотермический процесс.
При изотермическом процессе температура постоянна, следовательно, или 
т.е. давление и объем обратно пропорциональны друг другу, так что при изотермическом сжатии давление газа возрастает, а при расширении — падает (закон Бойля-Мариотта).
Графиком изотермического процесса в /?, у-координатах является равнобокая гипербола, для которой координатные оси служат асимптотами (рис. 2.8).
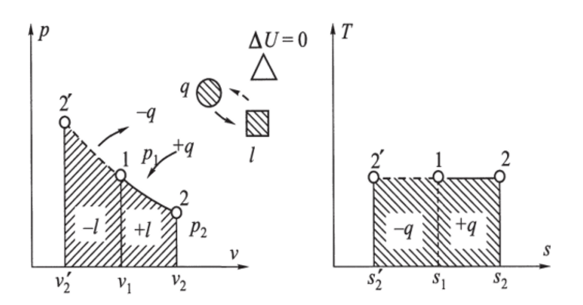
Рис. 2.8. Изотермический процесс вp, vи /^-диаграммах и схема энергобаланса.
Работа процесса:
Так как температура не меняется, то внутренняя энергия идеального газа в данном процессе остается постоянной (Ди = 0) и вся подводимая к газу теплота полностью превращается в работу расширения:
.
При изотермическом сжатии от газа отводится теплота в количестве, равном затраченной на сжатие работе.
Изменение энтропии в изотермическом процессе выражается формулой: