Реальные газы, вода и водяной пар

Практически пользоваться уравнением Ван-дер-Ваальса нельзя, так как оно дает результаты, недостаточно точные для нужд современной паротехники. Наиболее точным является в настоящее время уравнение состояния реальных газов, разработанное М. П. Вукаловичем и Н. И. Новиковым (Московский энергетический институт) применительно в основном к водяному пару. Вывод этого уравнения основан на предположении… Читать ещё >
Реальные газы, вода и водяной пар (реферат, курсовая, диплом, контрольная)
К реальным газам в технической термодинамике принято относить перегретые пары некоторых жидкостей. В отличие от воображаемого идеального газа реальный газ, при соответствующих условиях, может быть сжижен, т. е. сконденсирован, или же переведен в твердое состояние.
В технике широко применяют пары различных веществ: воды, аммиака, хлористого метила, сернистого ангидрида и др. Наибольшее применение имеет водяной пар, являющийся основным рабочим телом паровых двигателей, отопительных и других устройств.
Известно, что законы идеальных газов нельзя распространить на рабочие тела, состояние которых не очень удалено от жидкой фазы.
В связи с этим на водяной пар при давлениях и температурах, обычно применяемых в теплоэнергетике, не распространяется уравнение состояния Клапейрона. Из ряда предлагавшихся уравнений состояния, применимых для него с известной степенью приближенности, можно отметить уравнение Ван-дер-Ваальса, составленное для оеальных газов и имеющих вид:
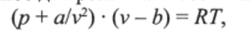
где а и Ъ — постоянные для данного газа.
Слагаемым д/v2 в первом множителе учитывается влияние сил взаимодействия молекул, во втором множителе вычитаемым Ь учитывается влияние объема молекул (поскольку в идеальном газе, для которого и справедливо уравнение состояния Клапейрона, объем молекул полагается равным нулю).
Практически пользоваться уравнением Ван-дер-Ваальса нельзя, так как оно дает результаты, недостаточно точные для нужд современной паротехники. Наиболее точным является в настоящее время уравнение состояния реальных газов, разработанное М. П. Вукаловичем и Н. И. Новиковым (Московский энергетический институт) применительно в основном к водяному пару. Вывод этого уравнения основан на предположении наличия в реальных газах ассоциаций молекул, механически объединенных в двойные, тройные и более сложные комплексы, образующиеся в результате взаимодействия между ними. Для этого уравнения характерно близкое совпадение результатов расчетов с опытными данными. Однако для практических целей пользование этим, как и другими уравнениями состояния реального газа, неудобно вследствие сложности их и необходимости выполнения трудоемких вычислений. Обычно пользуются готовыми данными, которые берут из таблиц водяного пара или из диаграммы i, s водяного пара.
Промежуточное состояние вещества между состоянием реального газа и жидкостью принято называть парообразным, или просто паром. Превращение жидкости в пар представляет собой фазовый переход из одного агрегатного состояния в другое. При фазовом переходе наблюдается скачкообразное изменение физических свойств вещества.
Примерами таких фазовых переходов являются процесс кипения жидкости с появлением влажного насыщенного пара и с последующим переходом его в лишенный влаги сухой насыщенный пар или обратный кипению процесс конденсации насыщенного пара. Во всех этих фазовых переходах существует однозначная связь между давлением и температурой (в данном примере — связь давления с температурой кипения или конденсации).
Одно из основных свойств сухого насыщенного пара заключается в том, что дальнейший подвод теплоты к нему приводит к возрастанию температуры пара, т. е. переходу его в состояние перегретого пара, а отвод теплоты — к переходу в состояние важного насыщенного пара. В современной теплоэнергетике основным рабочим телом является водяной пар. Поэтому изучение термодинамических свойств паров рассмотрим на примере водяного пара.