Оксид алюминия.
Материаловедение.
Техническая керамика в машиностроении

В оксиде алюминия А120з атомы кислорода благодаря своей высокой электроотрицательности отвлекают электроны атомов алюминия из зоны проводимости на связь, стабилизируя тем самым устойчивые конфигурации S2 и sp' а точнее их суперпозицию. В результате каждый атом алюминия в АЬОз оказывается окруженным шестью атомами кислорода, которые образуют алюмооксидный октаэдр, а октаэдры связаны между собой… Читать ещё >
Оксид алюминия. Материаловедение. Техническая керамика в машиностроении (реферат, курсовая, диплом, контрольная)
В системе алюминий — кислород существует единственное термодинамически стабильное соединение — полуторный оксид алюминия АЬОз, в котором может быть растворена массовая доля А1 10'4%. Растворимость кислорода в алюминии практически равна нулю. Чистый оксид алюминия часто встречается в двух модификациях а и у. Кроме них, в процессе дегидратации гидроксидов алюминия при неравновесной кристаллизации расплавов оксида алюминия зафиксированы 0, к, х и некоторые другие модификации, которые при термообработке свыше 1200° С переходят в а-форму.
В оксиде алюминия А120з атомы кислорода благодаря своей высокой электроотрицательности отвлекают электроны атомов алюминия из зоны проводимости на связь, стабилизируя тем самым устойчивые конфигурации S2 и sp' а точнее их суперпозицию. В результате каждый атом алюминия в АЬОз оказывается окруженным шестью атомами кислорода, которые образуют алюмооксидный октаэдр, а октаэдры связаны между собой через атомы кислорода общей гранью (рис. 1.1, а). Анализируя полученную структуру, можно выделить в ней группировки АЬОз, в которых атомы кислорода связаны непосредственно друг с другом и атомами алюминия. Следовательно, основным структурным мотивом в оксиде алюминия служат алюмооксидные октаэдры, а не дискретные молекулы АЬОз. На это обстоятельство впервые обратил внимание академик Н. В. Белов, который показал (из чисто кристаллохимических соображений), что обычно изображаемые структуры оксида алюминия, либо с выделенными дискретными молекулами АЬОз, либо подчеркивающие его гексагональное строение (рис. 1.1, б, в), не позволяют объяснить высокую прочность и твердость этого соединения. Поэтому предложена структура оксида алюминия, в которой основным структурным мотивом служит алюмокислородный октаэдр. На рис. Ы, г и рис. 1.1, д, е показано строение оксида алюминия по Н. В. Белову, которое полностью согласуется с современными представлениями о природе химической связи и соответствует им.

Рис. 1.1. Структура оксида алюминия: а — элемент структуры корунда; б — кристаллическая структура с выделенными дискретными молекулами А120з; в — гексагональное расположение атомов в структуре А120з (по У. Файфу);
г — основной мотив из спаренных октаэдров (по Н. В. Белову); д — элементарный ромбоэдр, разбитый для ясности на элементарные слои.
(по Н. В. Белову) Сохраняя подобный подход, значительно легче понять формирование структуры оксида алюминия из его гидратных форм. В частности, сильно гидратированные растворы гидратов алюминия.
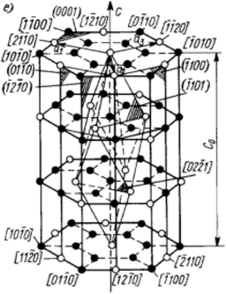
Рис. 1.1. е — современное изображение структуры АЬОЗ; о — атомы алюминия; • - атомы кислорода
содержат октаэдрические анионы [А1(ОН)б]"3 и катионы [А1(Н20)б]3. В присутствии ионов щелочных металлов эти анионы становятся более устойчивыми, что и определяет в конечном итоге трудности удаления щелочей из оксида алюминия. Кристаллические гидраты оксида алюминия: гидраргиллит, диаспор и бемит также построены из алююмокислородных октаэдров, имеющих общие ребра. В кубическом уАЬОз сохраняется структура гидратов. При переходе в аА120з структура уплотняется за счет того, что элементарные октаэдры сопрягаются не ребрами, а гранями.
Оксид у-АЬОз является исходным сырьем в технологии корундовой керамики и получается при термической обработке (500 — 950° С) гидраргиллита Al20.v3H20 или бемита А120,гН20. В у-АЬОз, кристаллизующимся в кубической сингонии (типа шпинели), сохраняется до 2% структурно связанной воды. В зависимости от предыстории плотность у-А120з находится в пределах от 3,47−10^ до 3,66−10^ кг/мЗ. Переход у-АЬОз в a-форму (корунд) протекает весьма медленно в кинетической области при.
800 — 1000° С и полностью завершается при 1200 — 1300° С. Точные значения температуры и времени выдержки при этой температуре для полного у—их-перехода зависят от предыстории у-формы, наличия примесей и других факторов. Необходимость контроля полноты перехода вызвана увеличением плотности на 14 — 18% и снижением удельной поверхности порошка.
Кинетическое уравнение у—их-перехода АЬСЬ может быть представлено в виде а=1-ехр[-(кт)"], где, а — степень превращения у-А12СЬ в а-АЬСЬ за время т; к — константа скорости этого процесса, температурная зависимость которой описывается уравнением Аррениуса:
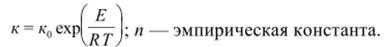
Скорость у—>а-перехода АЬОя существенно зависит от добавок в исходную у-форму частиц a-формы, что отражается на значении кинетических параметров и температуре завершения перехода (табл. 1.2).
Снижение температуры у—их-перехода АЬСЬ способствует сохранению в ходе нагревания высокой дисперсности порошка, которая необходима для активирования спекания и создания в спеченном материале мелкозернистой структуры.
Таблица 1.2.
Параметры кинетического уравнения у—их-перехода АЬСЬ
Количество добавки А12Оз в виде зерен, м3 | Энергия активации ?, кДж/моль. | *0, С'1 | п | Температура завершения перехода Г, К. |
Без добавок. | 442,0. | 2,6−1013 | 0,10. | |
1,8-Ю17 | 439,0. | 5,9−1012 | 0,16. | |
9,2−1017 | 381,0. | 9,3−10″ . | 0,18. | |
2,7−1019 | 352,0. | 1,7−10″ . | 0,20. | |
В технологии высокопрочной корундовой керамики наиболее важны системы Al203-Mg0, AI2O3-Z1O2 и AI2O3-Y2O3 (рис. 1.2, а-в).

Рис. 1.2. Наиболее важные системы в корундовой керамике: а — система АЬОз-MgO; б — система AI2O3-Z1O2; в — система AI2O3-Y2O3.
В системе А1203 — MgO (рис. 1.2, а) имеется одно соединение — нормальная шпинель MgAl204. Ее элементарная ячейка состоит из 32 ионов кислорода, восьми ионов магния и 16 ионов алюминия; причем восемь двухвалентных ионов Mg2+ находятся в тетраэдрическом положении плотной гранецентрированной решетки кислорода, а 16 трехвалентных ионов А13+ — в октаэдрическом. Постоянная кристаллической решетки 0,806−0,808 нм. Магнезиальная шпинель образует твердые растворы с А120з и MgO, дающие эвтектики с корундом и периклазом при 1925 и 1995° С соответственно. Термический коэффициент линейного расширения MgAl204 приблизительно 8,2 10−6 К-1, модуль Юнга (2,2;
2,5)105 МПа, плотность 3,58* 10^ кг/м^, диэлектрическая проницаемость 7,5 — 8,0.
Традиционным способом получения а-А1203 является выплавка его из бокситной руды в руднотермической электропечи в виде электрокорунда. Массовая доля а-А120з в этом материале составляет не менее 95%. Основные примеси: Si02 (до 0,7%), ТЮ2 (до 3,2%), СаО (до 0,68%), Ре20з (до 0,47%). Такой материал используется для изготовления абразивных инструментов. Этим способом получают a-АЬОз в виде крупных слитков, которые подвергаются измельчению до порошков различной крупности (крупные, средние, тонкие, микропорошки). В керамической технологии применяются высокодисперсные порошки электрокорунда белого после сверхтонкого механического измельчения.
Мелкие частицы АЬОз размером менее 1 мкм получают путем регулирования условий осаждения А1(ОН)3, который затем прокаливают, а полученный при этом АЬОз измельчают. Содержание а-АЬ03 в готовом продукте — 99,99% средний размер частиц — 0,5 мкм.
При получении чистого АЬОз этиленхлоргидриновым методом раствор Na[Al (OH)4], нейтрализуют с помощью этиленхлоргидрина органической кислоты для образования А1(ОН)3, который затем выдерживают при 323 К до перехода в бемит. Полученный бемит обжигают для получения а-АЬ03, а этиленоксид, образовавшийся при нейтрализации, обрабатывают соляной кислотой с выделением этиленхлоргидрина, который снова возвращают в процесс. В целом весь процесс синтеза АЬОз этиленхлоргидриновым методом можно представить в виде следующих реакций:
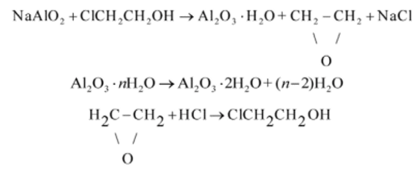
Поскольку этиленхлоргидрин, являясь слабой кислотой, весьма медленно осаждает А1(ОН)3, то примеси натрия, железа и другие могут быть удалены в виде водных растворов их хлоридов. Полученный таким способом порошок а-АЬ03 с содержанием основного вещества не менее 99,99% имеет удельную поверхность до 40 м2/г.
Получение а-А120з особой чистоты при высокой дисперсности основано на синтезе и перекристаллизации алюмоаммонисвых квасцов с последующим их термолизом в соответствии с реакциями:

При pH среды менее 1,0 удаляется 70 — 80% примесей железа и титана уже во время синтеза квасцов. При очистке квасцов методом перекристаллизации растворов удается полностью удалить примеси железа и титана.
Высокочистый АЬОз можно получить термолизом сложного карбоната аммония и алюминия, который образуется из квасцов по реакции.

Для проведения процесса наиболее оптимальными условиями являются: концентрация NH4HCO3 — более 1 моль/л, а мольное отношение NH4A1(S04)2 к NH4HCO3 должно составлять 10−15 при температуре реакции 308 К. Преимуществом данного процесса является отсутствие плавления материала при его термическом разложении, что позволяет довольно легко регулировать размер частиц а-А120з. Кроме того, при этом процессе не выделяется SO3. При оптимальных условиях процесса размер частиц а-А120з составляет 0,1 — 0,5 мкм.
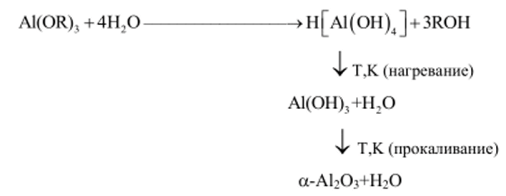
Наиболее чистый и высокодисперсный порошок А1203 получают методом гидролиза его металлоорганических соединений (AIR3 или А1((Ж)з, где R — алкил) до А1(ОН)з с последующим его прокаливанием до образования сх-А120з в соответствии с реакциями: 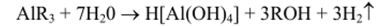
Гидролизом алюминийорганических соединений можно получить наиболее чистый a-АЬОз, в котором количество примесей не превышает 10'3%. Кроме того, способ достаточно дешев, поскольку его стоимость определяется только стоимостью алюминия, а участвующий в реакции спирт можно регенерировать. По этим причинам получение особо чистого АЬОз гидролизом его алкилов или оксиалкилов можно считать наиболее перспективным.
Для получения АЬОз плазмохимическим методом из хлорида алюминия (А1С1з) используется высокочастотный плазмотрон с колебательной мощностью 60 кВт и рабочей частотой 5,28 Мгц.