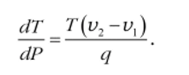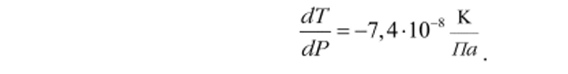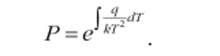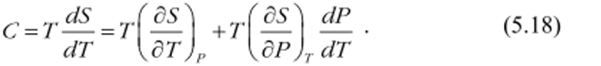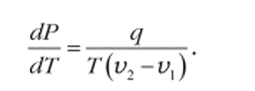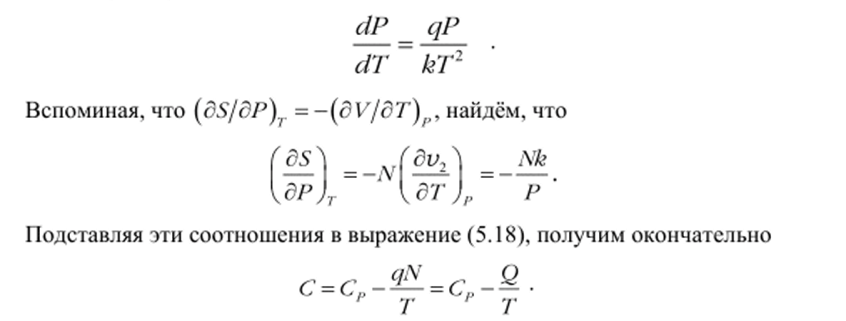1. Удельная теплота плавления льда ^ при 0 °C и давлении 1 атм составляет 80 кал/г. Отношение удельных объёмов льда и воды составляет 1,091: 1,000. Оценить изменение температуры плавления при изменении давления.
Решение. Применим к фазовому переходу лёд-вода уравнение Клапейрона-Клаузиуса в форме: 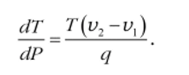
Если иод q в этом уравнении понимать удельную теплоту плавления льда, то V] и v2 — удельные объёмы льда и воды соответственно. Известно, что 1 м3 вмещает 1000 кг воды, следовательно, iл = 10~3 л?/кг, а ь> = 1,091 ih. В системе СИ 80 кал/г = 80 ккал/кг = 80−4,19−10' Дж/кг. Подставляя эти данные в уравнение Клапейрона-Клаузиуса, получим, что.
Это означает, что при изменении давления на 1 Па температура плавления.
_8.
уменьшается на 7,4−10 К.
2. Температурная зависимость удельной теплоты испарения воды выражается уравнением q' = a — bT, где а = 164 кал/гч b = 0,6 кал/гК. Чему равно давление насыщенного водяного пара при температуре / =80°С?
Решение. Воспользуемся выражением для давления насыщенного пара, которое было получено в § 3:
Теплота q в этом выражении — молекулярная теплота, то есть q = Q/N. В нашей задаче задана удельная теплота: q = Q/m, следовательно, q = q’m/N. Учитывая, что N = TV. m/p, получим.
где А — постоянная интегрирования, которую можно определить, если учесть, что при нормальной температуре (Т0= 0 °C = 273К) давление насыщенного пара равно нормальному давлению (Р0 = 1 шпм). Тогда:
Подставляя сюда численные данные, получим, что Р = 0,471 шил/.
3. Определить теплоёмкость пара для процесса, при котором жидкость все время находится в равновесии со своим насыщенным паром.
Решение. Искомая теплоёмкостью С равна.
Величина T{dS/dT)p =СГ, а производная dP/dT вычисляется вдоль кривой равновесия фаз и, следовательно, определяется уравнением Клапейрона-Клаузиуса 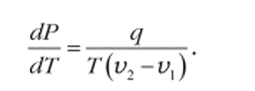
Будем считать пар идеальным газом, тогда PV2 = NkT, то есть v2 =kT/P. Удельным объемом жидкости по сравнению с удельным объемом пара можно пренебречь, тогда.
При низких температурах теплоёмкостью пара становится отрицательной, это означает, что если отнимать тепло так, чтобы пар все время находился в равновесии с жидкостью, то его температура может и повышаться.