Вода.
Химия. В 2 ч. Часть 1. Общая и неорганическая химия

Вода — широко распространенное в природе вещество, поэтому ее, как химическое соединение, не получают из других веществ, а подвергают очистке (в разной степени, в зависимости от областей использования). Для научных целей воду подвергают полному обессоливанию (дистилляции), которое проводят или методом перегонки, или ионитным способом. В промышленности для технических целей воду очищают… Читать ещё >
Вода. Химия. В 2 ч. Часть 1. Общая и неорганическая химия (реферат, курсовая, диплом, контрольная)
I. Общая характеристика.
Вода состоит из водорода и кислорода. Существует более 18 разновидностей молекул воды (так как в природе известны три изотопа водорода и столько же изотопов кислорода). Вода, содержащая дейтерий, называется тяжелой водой.
Обычная (протиевая) вода при 4 °C имеет молекулярную фор;
мулу Н20; ее структурная формула: Н Н; валентный угол равен 104,5°. Электронная формула: Н:0-Н.
• •.
В молекулах воды реализуется полярная ковалентная сигма 5—/7-связь по обменному механизму. В жидком и твердом состоянии между молекулами воды возникают водородные связи, т. е. формула воды при температурах меньше 4 °C (277 К), (Н20)", где п = 2,3,4,… ит.д.:

II. Физические свойства.
В условиях планеты Земля вода находится в трех агрегатных состояниях: парообразном (газ), жидком и твердом (кристаллическое, лед). Жидкая вода сильнополярна, поэтому она хорошо растворяет в себе вещества, имеющие полярные молекулы или являющиеся ионными кристаллами. При 277 К (4 °С) р = 1 (г/см3, кг/дм3, т/м3 в СИ — 1000 кг/м3, так как 1 см3 = 1 мл, а 1 дм3 = 1 л, то плотность воды выражают или в г/мл, или в кг/л). При понижении температуры ее плотность уменьшается (первая аномалия воды, связанная с тем, что в твердом состоянии структура воды менее компактна из-за того, что ассоциаты воды, образованные тремя и более молекулами, образуют «рыхлую», занимающую больший объем, чем ассоциат, состоящий из двух молекул). Второй аномалией воды является то, что вода имеет очень высокую теплоемкость, так как между ее молекулами реализуются водородные связи. Температура кипения воды составляет 373 К (100 °С), а плавления — 273 К. Аномалией воды является и то, что она — жидкость, тогда как все халькогеноводороды, имеющие молярную массу, большую, чем вода, — газы (третья аномалия). Все аномалии воды связаны, с одной стороны, с высокой полярностью молекул воды, а с другой — со способностью этих молекул образовывать водородные связи. В кристаллическом состоянии молекулы воды образуют сетчатую структуру, характеризующуюся большой рыхлостью, а поэтому относительно малой плотностью.
III. Химические свойства.
Из-за особенностей химического строения вода является очень активным химическим реагентом.
1. Вода — слабый электролит и диссоциирует по схеме:
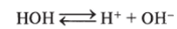
т. е. она — амфолит (амфотерный электролит).
2. Вода взаимодействует с оксидами, образуя растворимые гидроксиды (кислоты или щелочи):
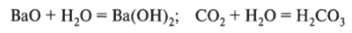
3. Вода вступает в реакцию гидратации — химически взаимодействует с солями и другими веществами, образуя кристаллогидраты или другие соединения:
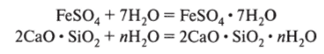
- 2СаО • Si02 • лН20 — гидратированный двукальциевый силикат — составная часть искусственного цементного камня.
- 4. Реагирует с органическими непредельными соединениями (реакция гидратации):
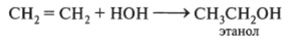
5. Вступает в реакции гидролиза — разрушение веществ водой. Гидролизу подвергаются и неорганические (соли), и органические (эфиры, углеводы, белки и т. д.) вещества: 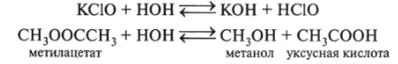
- 6. Реагирует с металлами:
- а) при обычных условиях:
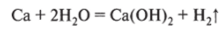
б) при нагревании:
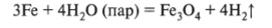
в) при обычных условиях взаимодействует с металлами, вызывая коррозию, которая активно протекает в присутствии различных примесей:
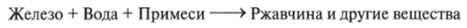
7. Взаимодействует с неметаллами:
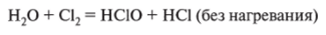
8. Вступает в различные реакции совместно с другими веществами:
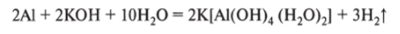
9. Участвует в реакциях электролиза, при этом вода может и восстанавливаться (на катоде), и окисляться (на аноде).
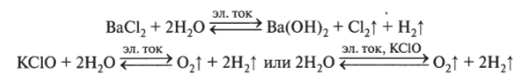
Для воды характерны и другие свойства.
IV. Получение.
Вода — широко распространенное в природе вещество, поэтому ее, как химическое соединение, не получают из других веществ, а подвергают очистке (в разной степени, в зависимости от областей использования). Для научных целей воду подвергают полному обессоливанию (дистилляции), которое проводят или методом перегонки, или ионитным способом.
В промышленности для технических целей воду очищают от взвешенных частиц, а для получения питьевой воды природную воду подвергают сложной обработке, при которой удаляют грубые взвеси, коллоидные частицы, уничтожают вредные микроорганизмы и т. д. Питьевую воду получают на станциях водоочистки; такая вода называется «водопроводной».
В лаборатории воду принципиально можно получить следующими способами:
1. Синтезом из водорода и кислорода: 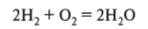
2. Разложением гидроксидов:
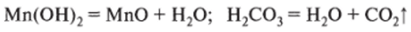
3. Горением органических веществ:
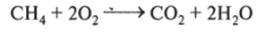
4. Реакцией нейтрализации:
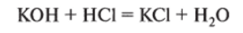
и другими способами.
V. Применение.
Вода — вещество, без которого невозможна жизнь любых организмов, в том числе и человека. Ее широкое использование связано с комплексом разнообразных свойств. Так, она — прекрасный растворитель, поэтому ее используют в быту (стирка одежды, гигиенические процедуры и т. д.), в производстве (удаление растворимых загрязнений, приготовление различных растворов и т. д.); в учебных и научных целях (готовят растворы различных веществ и т. д.). Воду применяют и как реагент в органическом (получение уксусной кислоты из ацетилена, при гидролизе жиров, белков, углеводов и т. д.) и неорганическом (получение кристаллогидратов и других веществ) синтезах. Вода находит широкое использование в сельском хозяйстве (для полива полей, мытья применяемого оборудования, в животноводстве и т. д.), в строительстве при изготовлении бетона и т. д.
- ? Задания для самостоятельной работы
- 1. Назовите особенности строения молекул воды, с которыми связаны аномалии в ее физических свойствах.
- 2. Поясните, почему для воды характерна высокая теплоемкость.
- 3. Поясните, почему сероводород является газом, а вода — жидкостью при 277 К, несмотря на то что молярная масса первого вещества больше, чем второго.
- 4. Поясните, почему вода является амфолитом.
- 5. Приведите три обоснованных примера использования воды человеком в своей жизнедеятельности.