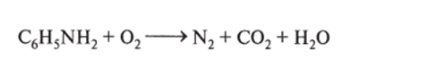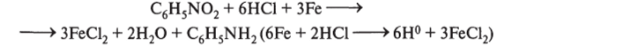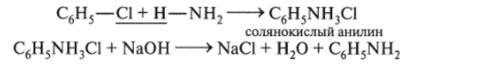I. Общая характеристика.
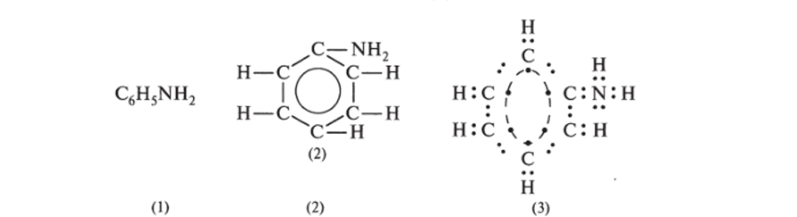
Ниже представлены различные формулы анилина: эмпирическая (1), структурная (2), электронная (3):
Взаимное влияние атомов в молекуле анилина такое же, как и в феноле (на свойства бензольного ядра; см. фенол). Влияние бензольного ядра на свойства аминогруппы состоит в том, что оно оттягивает к себе электронные облака от атома азота, чем ослабляет основные свойства аминогруппы (анилин является более слабым основанием, чем NH4OH и предельные амины).
II. Физические свойства.
Анилин — бесцветная маслянистая жидкость. Малорастворим в воде. Химически чистый анилин бесцветен; цвет анилина, встречающегося в лаборатории, светло-коричневый, так как он частично окисляется кислородом воздуха. Очень токсичен (ядовит).
III. Химические свойства.
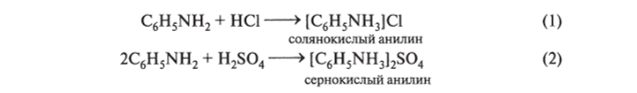
Солянокислый и сернокислый анилины представляют собой соли фениламмония; они по свойствам напоминают соли аммония.
Анилин, в отличие от аммиака, практически не взаимодействует с водой, его раствор в воде не изменяет окраски индикаторов.
- 4. Свойства анилина, связанные с бензольным ядром:
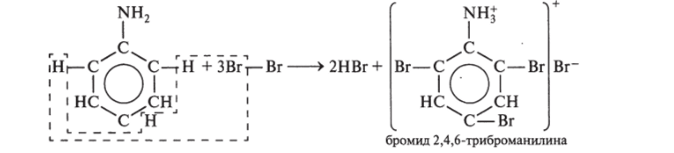
- 4.1. Реакция замещения; анилин содержит аминогруппу —NH2, являющуюся заместителем I рода, поэтому анилин при обычных условиях вступает в реакции замещения с электрофильными реагентами (галогенами, азотной кислотой и др.).
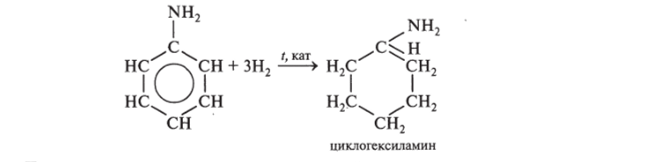
4.2. Взаимодействует с Н2 (реакция присоединения):
Для анилина характерны и другие свойства.
IV. Получение.
Анилин получают разными способами. Рассмотрим некоторые из них.
1. Реакция Зинина — из нитробензола, который восстанавливают водородом в момент выделения:
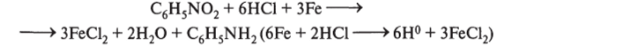
Атомарный водород в момент выделения способен восстанавливать нитросоединения до аминов.
2. Взаимодействием галогенопроизводных с аммиаком:
V. Применение.
Анилин является основным исходным веществом при синтезе красителей. Он применяется при получении лекарственных препаратов и различных полимеров.
Анилин токсичен, поэтому экологически опасен и требует осторожного обращения.
- ? Задания для самостоятельной работы
- 1. Поясните, почему анилин является ароматическим первичным амином.
- 2. Обоснуйте особенности химических свойств анилина, исходя из строения его молекул.
- 3. Обоснуйте области применения анилина (два примера).
- 4. Из хлорбензола получите фениламин.
- 5. Приведите обоснованный пример, иллюстрирующий экологическую роль анилина.