Титрование многоосновных (полипротонных) кислот (и многокислотных оснований)

Чем слабее кислота, тем выше pH в начале титрования и в области буферного действия. Следовательно, ветвь кривой титрования до ТЭ смещается в щелочную область. В ТЭ образуется основание тем более сильное, чем слабее исходная кислота, следовательно, pH смещается также в щелочную область. В то же время ветвь за ТЭ остается неизменной, но в целом скачок уменьшается (рис. 17.6). Аналогично для… Читать ещё >
Титрование многоосновных (полипротонных) кислот (и многокислотных оснований) (реферат, курсовая, диплом, контрольная)
Многоосновные кислоты (Н3Р04, Н2С03 и т. п.), а также многокислотные основания (Ва (ОН)2, Mg (OH)2 и др.) диссоциируют по ступеням. Например, диссоциация Н3Р04 протекает в три ступени:
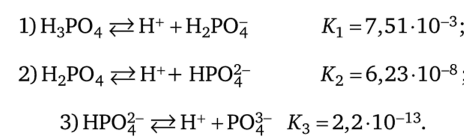 «.
«.
Однако диссоциация по второй и третьей ступеням почти не происходит из-за того, что катионы Н+, образовавшиеся по первой ступени, смещают влево равновесия второй и третьей реакций. При титровании ортофосфорной кислоты Н3Р04 щелочью сначала нейтрализуются ионы Н+, образовавшиеся по первой ступени диссоциации, и в точке эквивалентности наблюдается скачок pH (рис. 17.5). Если продолжать титрование, то далее будут нейтрализоваться ионы Н+, получившиеся по второй ступени диссоциации, а на кривой появляется второй скачок pH. Казалось бы, что в момент нейтрализации около точки эквивалентности должен произойти третий скачок pH. Однако он не наблюдается, так как pH растворов фосфата калия и гидроксида калия очень близки.
Таким образом, кривые титрования многоосновных (полипро-тонных) кислот (или многокислотных оснований) имеют несколько перегибов, отвечающих разным ступеням диссоциации. Чаще всего эти перегибы недостаточно четки, особенно около второй и третьей точек эквивалентности, но в отдельных случаях они бывают хорошо выражены. Разделение и отчетливое проявление этих скачков на кривой титрования зависят от величин констант последовательной ступенчатой диссоциации кислоты и от концентрации кислоты в титруемом растворе. Скачки на кривой титрования проявляются более четко при условии, что константы диссоциации отличаются не менее чем в 10 000 раз.
Кривая титрования 10 мл 0,1 н. раствора Н3Р04 0,1 н. раствором NaOH изображена на рис. 17.5.
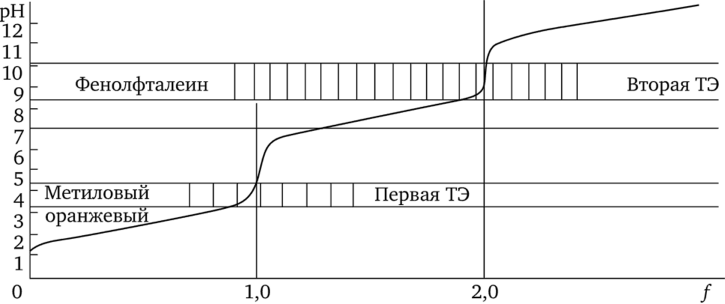
Рис. 17.5. Кривая титрования полипротонной (многоосновной) кислоты и области перехода индикаторов.
При титровании ортофосфорной кислоты Н3Р04 щелочью окраска метилового оранжевого изменяется в тот момент, когда вся кислота превратится в дигидрофосфат:
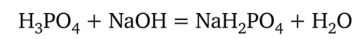
Объясняется это тем, что pH раствора NaH2P04 приблизительно равен 4,5, т. е. лежит вблизи области перехода метилового оранжевого. Следовательно, ортофосфорная кислота титруется с метиловым оранжевым как одноосновная кислота. В этом случае молярная масса эквивалентов кислоты Н3Р04 равна ее молярной массе.
С фенолфталеином ортофосфорная кислота титруется как двухосновная:
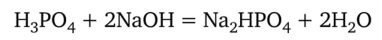
Раствор гидрофосфата натрия Na2HP04 имеет вследствие протолиза pH 9,7, лежащий в области перехода окраски фенолфталеина. Здесь молярная масса эквивалентов Н3Р04 равна ½ ее молярной массы.
Изменение окраски обоих индикаторов не бывает резким вследствие плавного изменения pH около точек эквивалентности. Поэтому рекомендуется титровать ортофосфорную кислоту щелочью в присутствии «свидетеля». Более резкому изменению окраски фенолфталеина способствует прибавление к раствору хлорида натрия.
В аналитической практике ортофосфорную кислоту титруют с разными индикаторами.
- 1. Титрование Н3Р04 до КН2Р04. К раствору кислоты прибавляют 1—2 капли метилового оранжевого и титруют раствором КОН до окраски, одинаковой со стандартным раствором. В качестве последнего служит ОД М раствор дигидрофосфата калия с метиловым оранжевым.
- 2. Титрование Н3Р04 до К2НР04. К раствору кислоты добавляют 1—2 капли фенолфталеина и избыток хлорида натрия. Затем титруют раствором КОН до появления слабой малиновой окраски. Титрование ортофосфорной кислоты щелочью до трехзамещенной соли невозможно.
Факторы, влияющие на скачок титрования. На величину скачка влияют все факторы, от которых зависят значения pH: константа диссоциации титруемого вещества, концентрация титруемого вещества и титранта, температура, ионная сила.
Чем слабее кислота, тем выше pH в начале титрования и в области буферного действия. Следовательно, ветвь кривой титрования до ТЭ смещается в щелочную область. В ТЭ образуется основание тем более сильное, чем слабее исходная кислота, следовательно, pH смещается также в щелочную область. В то же время ветвь за ТЭ остается неизменной, но в целом скачок уменьшается (рис. 17.6). Аналогично для оснований: чем слабее титруемое основание, тем скачок меньше и тем более он смещен в кислую область. Для кислот и оснований с константой диссоциации менее 5 • lO8 ТЭ сливается с началом правой ветви кривой, т. е. скачок отсутствует. Так, нельзя оттитровать в водных растворах такие вещества, как Н3В03 (Кк = 5,6 • lO10), C5H5N (.К0 = 1,5 • lO9) и т. п.
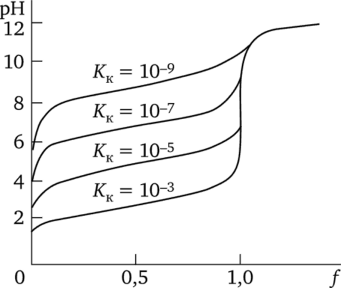
Рис. 17.6. Влияние силы кислоты на величину скачка титрования.
Чем меньше концентрация титруемого вещества и титранта, тем уже скачок. Практически невозможно оттитровать сильные кислоты с концентрацией меньше 10-4 М, а слабые — с концентрацией меньше 10~2 М.
При изменении температуры сильно изменяется константа автопротолиза воды, входящая во многие формулы расчета pH. В результате при повышении температуры скачок уменьшается и смещается в более кислую область.