Девятикарбонил железа.
Карбонилы и хлориды металлов VIII В группы, их свойства и применение

Кристаллы чистого девятикарбонила на воздухе долго сохраняют свой блеск. Загрязненные следами пятикарбонила железа, они на воздухе неустойчивы и могут воспламеняться. Хлор и бром разлагают кристаллы. Бромная вода растворяет их с выделением газа. При этом частично образуется Fe2(CO)7Br4. Соляная и серная кислоты при комнатной температуре на кристаллы девятикарбонила не действуют. Азотная кислота… Читать ещё >
Девятикарбонил железа. Карбонилы и хлориды металлов VIII В группы, их свойства и применение (реферат, курсовая, диплом, контрольная)
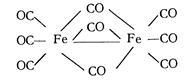
Для молекулы девятикарбонила железа были предложены две модели: с одним и с тремя СО-мостиками между обоими центральными атомами.
Если при образовании девятикарбонила атом железа вступает в соединение без предварительной перегруппировки своих двух 4s-электронов, то молекулы окиси углерода могут координироваться только с тремя свободными 4р-ячейками центрального атома железа. В этом случае у атома железа остаются четыре холостых Зd-электрона, из которых один образует связь типа ковалентной со вторым атомом металла, а остальные три спариваются с двумя 2s-электронами атома углерода трех молекул окиси углерода. Из них строятся три мостика в молекуле девятикарбонила:
Чистый продукт получается при засвечивании раствора пятикарбонила железа в уксусной кислоте. Освобождающуюся окись углерода надо непрерывно удалять, например, потоком водорода. Если возобновить облучение маточного раствора, то появляются дополнительные количества девятикарбонила. Для получения чистых кристаллов девятикарбонила можно разлагать солнечным светом в вакууме раствор пятикарбонила железа в сухом эфире или в петролейном эфире.
Фотохимическое разложение пятикарбонила железа ускоряется по мере повышения температуры. Однако около 56 °C наступает перелом и выше этой температуры свет уже не выделяет девятикарбонила. В темноте идет обратная реакция воссоединения и регенерации пятикарбонила. Следовательно, имеем равновесную реакцию:
2Fe (СО)5-Fe2 (СО)9 + СО, которая в зависимости от внешних условий — температуры, освещения, затемнения, давления окиси углерода — может сдвигаться вправо или влево [2].
Девятикарбонил железа кристаллизуется в виде металлически блестящих золотистых пластинок или оранжевых, иногда оранжево-красных, гексагональных листочков. Без подогрева кристаллы устойчивы даже при длительном нахождении на солнечном свете. На влажном воздухе девятикарбонил медленно с поверхности кристаллов превращается в окись железа. Пленка окислов может предохранить продукт от дальнейшего окисления. При хранении больших количеств девятикарбонила наблюдается самопроизвольное возгорание кристаллов. Видимо, теплота экзотермической реакции разложения большой массы девятикарбонила оказывается достаточной для нагрева кристаллов до точки самовоспламенения. Соединение диамагнитно.
Кристаллы чистого девятикарбонила на воздухе долго сохраняют свой блеск. Загрязненные следами пятикарбонила железа, они на воздухе неустойчивы и могут воспламеняться. Хлор и бром разлагают кристаллы. Бромная вода растворяет их с выделением газа. При этом частично образуется Fe2(CO)7Br4. Соляная и серная кислоты при комнатной температуре на кристаллы девятикарбонила не действуют. Азотная кислота разлагает их. Окись азота при 70−85°С реагирует с образованием карбонилнитрозила по уравнению [2]:
Fe2(СО)9 + 4NO = 2Fe (СО)2(NO)2 + 5СО.
При 100° реакция идет до полного разложения карбонила.
В спиртовом растворе едкого кали девятикарбонил растворяется, в жидком аммиаке — нет. Девятикарбонил реагирует с металлическим натрием, растворенным в жидком аммиаке [2]:
Fe2(CO)9 + 4Na = 2Na2Fe (CO)4 + CO.
Окись углерода медленно реагирует с девятикарбонилом в темноте при комнатной температуре:
Fe2(СО)9 + СО = 2Fe (СО)5.
При 46° реакция идет быстрее. Появление зеленого окрашивания показывает, что одновременно начинается термическое разложение девятикарбонила [1].
Если нагревать кристаллы твердого девятикарбонила железа с пиридином в запаянной пробирке в атмосфере углекислоты примерно до 95 °C, то сначала выделяется красновато-желтый осадок. Затем осадок исчезает, но при охлаждении выпадают крупные зеленые кристаллы четырехкарбонила [2]. В атмосфере углекислоты кристаллы девятикарбонила при 100 °C переходят в зеленую жидкость без увеличения давления в закрытом сосуде. Однако постепенно давление начинает возрастать с одновременным выпадением металлического железа. Жидкость при этом обесцвечивается. Разложение проходит в две стадии [2]:
2Fe2(CO)9 = 2Fe (CO)5 + [Fe (CO)4]3.

[Fe (CO)4]3 = Fe (CO)5 + Fe + 3CO.
Термическое разложение девятикарбонила заметно идет уже при 80−95°C. В токе водорода при 100—120° разложение идет по схеме [2]:
2Fe2(СO)9 = 3Fe (СO)5 + Fe + ЗСО.
Девятикарбонил слабо растворяется в карбониле никеля. Желтый раствор его при нагревании выделяет газ и металлическое железо. В эфире, петролейном эфире, четыреххлористом углероде, толуоле, бензоле девятикарбонил практически нерастворим; в метиловом, этиловом спиртах и в ацетоне слабо растворим; в пиридине растворяется легче, но с красным окрашиванием. [2].