Металлы и неметаллы

Все эти элементы образуют соединения с металлами — карбиды, силициды и бориды (CaC2, Al4C3, Fe3C, Mg2Si, TiB, TiB2). Некоторые из них обладают большей твердостью, например Fe3C, TiB. Карбид кальция используется для получения ацетилена. Если сравнить расположение электронов по орбиталям ф атомах фтора, хлора и других галогенов, то можно судить и об их отличительных свойствах. У атома фтора… Читать ещё >
Металлы и неметаллы (реферат, курсовая, диплом, контрольная)
Металлы — это элементы, проявляющие в своих соединениях только положительные степени окисления, и в простых веществах которые имеют металлические связи. Металлическая кристаллическая решетка — решетка, образованная нейтральными атомами и ионами металлов, связанными между собой свободными электронами. У металлов в узлах кристаллической решетки находятся атомы и положительные ионы.
Электроны, отданные атомами, находятся в общем владении атомов и положительных ионов. Такая связь называется металлической. Для металлов наиболее характерны следующие физические свойства: металлический блеск, твердость, пластичность, ковкость и хорошая проводимость тепла и электричества. Теплопроводность и электропроводность уменьшается в ряду металлов: Аg Сu Аu Аl Мg Zn Fе РЬ Hg.
Многие металлы широко распространены в природе. Так, содержание некоторых металлов в земной коре следующее:
- — алюминия — 8,2%;
- — железа — 4,1%;
- — кальция — 4,1%;
- — натрия — 2,3%;
- — магния — 2,3%;
- — калия — 2,1%;
- — титана — 0,56%.
С внешней стороны металлы, как известно, характеризуются прежде всего особым «металлическим» блеском, который обусловливается их способностью сильно отражать лучи света.
Однако этот блеск наблюдается обыкновенно только в том случае, когда металл образует сплошную компактную массу.
Правда, магний и алюминий сохраняют свой блеск, даже будучи превращенными в порошок, но большинство металлов в мелкораздробленном виде имеет черный или темно-серый цвет. Затем типичные металлы обладают высокой теплои электропроводностью, причем по способности проводить тепло и ток располагаются в одном и том же порядке: лучшие проводники — серебро и медь, худшие — свинец и ртуть. С повышением температуры электропроводность падает, при понижении температуры, наоборот, увеличивается.
Рисунок 1:
Очень важным свойством металлов является их сравнительно легкая механическая деформируемость. Металлы пластичны, они хорошо куются, вытягиваются в проволоку, прокатываются в листы и т. п.
Характерные физические свойства металлов находятся в связи с особенностями их внутренней структуры. Согласно современным воззрениям, кристаллы металлов состоят из положительно заряженных ионов и свободных электронов, отщепившихся от соответствующих атомов. Весь кристалл можно себе представить в виде пространственной решетки, узлы которой заняты ионами, а в промежутках между ионами находятся легкоподвижные электроны. Эти электроны постоянно переходят от одних атомов к другим и вращаются вокруг ядра то одного, то другого атома. Так как электроны не связаны с определенными ионами, то уже под влиянием небольшой разности потенциалов они начинают перемещаться в определенном направлении, т. е., возникает электрический ток.
Наличием свободных электронов обусловливается и высокая теплопроводность металлов. Находясь в непрерывном движении, электроны постоянно сталкиваются с ионами и обмениваются с ними энергией. Поэтому колебания ионов, усилившиеся в данной части металла вследствие нагревания, сейчас же передаются соседним ионам, от них — следующим и т. д., и тепловое состояние металла быстро выравнивается, вся масса металла принимает одинаковую температуру. По плотности металлы условно подразделяются на две большие группы: легкие металлы, плотность которых не больше 5 г/см. куб., и тяжелые металлы — все остальные. Частицы металлов, находящихся в твердом и жидком состоянии, связаны особым типом химической связи — так называемой металлической связью. Она определяется одновременным наличием обычных ковалентных связей между нейтральными атомами и кулоновским притяжением между ионами и свободными электронами. Таким образом, металлическая связь является свойством не отдельных частиц, а их агрегатов.
Наиболее активные металлы главных подгрупп являются сильными восстановителями, поэтому восстанавливают водород до степени окисления -1 и образуют гидриды.
Понятие о сплавах.
Характерной особенностью металлов является их способность образовывать друг с другом или с неметаллами сплавы.
Чтобы получить сплав, смесь металлов обычно подвергают плавлению, а затем охлаждают с различной скоростью, которая определяется природой компонентов и изменением характера их взаимодействия в зависимости от температуры.
Рисунок 2:
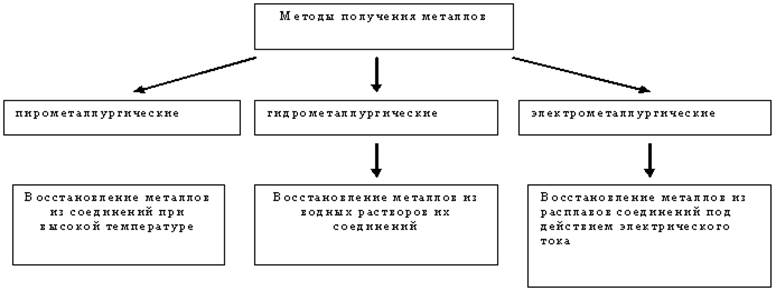
Иногда сплавы получают спеканием тонких порошков металлов, не прибегая к плавлению (порошковая металлургия). Итак сплавы — это продукты химического взаимодействия металлов.
Кристаллическая структура сплавов во многом подобна чистым металлам, которые, взаимодействуя друг с другом при плавлении и последующей кристаллизации, образуют:
- а) химические соединения, называемые интерметаллидами;
- б) твердые растворы;
- в) механическую смесь кристаллов компонентов.
Тот или иной тип взаимодействия определяется соотношением энергии взаимодействия разнородных и однородных частиц системы, то есть соотношением энергий взаимодействия атомов в чистых металлах и сплавах.
Современная техника использует огромное число сплавов, причем в подавляющем большинстве случаев они состоят не из двух, а из трех, четырех и большего числа металлов. Интересно, что свойства сплавов часто резко отличаются от свойств индивидуальных металлов, которыми они образованы. Так, сплав, содержащий 50% висмута, 25% свинца, 12,5% олова и 12,5% кадмия, плавится всего при 60,5 градусах Цельсия, в то время как компоненты сплава имеют соответственно температуры плавления 271, 327, 232 и 321 градус Цельсия. Твердость оловянной бронзы (90% меди и 10% олова) втрое больше, чем у чистой меди, а коэффициент линейного расширения сплавов железа и никеля в 10 раз меньше, чем у чистых компонентов. Однако некоторые примеси ухудшают качество металлов и сплавов. Известно, например, что чугун (сплав железа и углерода) не обладает той прочностью и твердостью, которые характерны для стали. Помимо углерода, на свойства стали влияют добавки серы и фосфора, увеличивающие ее хрупкость.
Среди свойств сплавов наиболее важными для практического применения являются жаропрочность, коррозионная стойкость, механическая прочность и др.
Для авиации большое значение имеют легкие сплавы на основе магния, титана или алюминия, для металлообрабатывающей промышленности — специальные сплавы, содержащие вольфрам, кобальт, никель. В электронной технике применяют сплавы, основным компонентом которых является медь. Сверхмощные магниты удалось получить, используя продукты взаимодействия кобальта, самария и других редкоземельных элементов, а сверхпроводящие при низких температурах сплавы — на основе интерметаллидов, образуемых ниобием с оловом и др.
Все многообразие окружающей нас природы состоит из сочетаний сравнительно небольшого числа химических элементов.
В различные исторические эпохи в понятие «элемент» вкладывался различный смысл. Древнегреческие философы в качестве «элементов» рассматривали четыре «стихии» — тепло, холод, сухость и влажность. Сочетаясь попарно, они образовывали четыре «начала» всех вещей — огонь, воздух, воду и землю. В средние века к этим началам добавились соль, сера и ртуть. В XVII веке Р. Бойль указал на то, что все элементы носят материальный характер и их число может быть достаточно велико.
В 1787 году французский химик А. Лавуазье создал «Таблицу простых тел». В нее вошли все известные к тому времени элементы. Под последними понимались простые тела, которые не удавалось разложить химическими методами на еще более простые. Впоследствии выяснилось, что в таблицу вошли и некоторые сложные вещества.
В настоящее время понятие «химический элемент» установлено точно.
Химический элемент — вил атомов с одинаковым положительным зарядом ядра. Последний равен порядковому номеру элемента в таблице Менделеева. В настоящее время известно 107 элементов. Около 90 из них существуют в природе. Остальные получены искусственно с помощью ядерных реакций. 104−107 элементы были синтезированы учеными-физиками в Объединенном институте ядерных исследований в городе Дубне. В настоящее время продолжаются работы по искусственному получению химических элементов с более высокими порядковыми элементами. Все элементы делятся на металлы и неметаллы. Из 107 элементов 85 относятся к металлам. К неметаллам относят следующие элементы: гелий, неон, аргон, криптон, ксенон, радон, фтор, хлор, бром, йод, астат, кислород, сера, селен, теллур, азот, фосфор, мышьяк, углерод, кремний, бор, водород. Однако это деление условное. При определенных условиях некоторые металлы могут проявлять неметаллические свойства, а некоторые неметаллы — металлические свойства.
Неметаллических элементов по сравнению к металлическими элементами относительно немного.
Все остальные неметаллы проявляют восстановительные свойства. Причем эти свойства постепенно возрастают от кислорода к кремнию: O, Cl, N, I, S, C, P, H, B, Si. Так, например, хлор непосредственно с кислородом не соединяется, но косвенным путем можно получить его оксиды (Cl2 O, ClO2, Cl2O2), в которых хлор проявляет положительную степень окисления. Азот при высокой температуре непосредственно соединяется с кислородом и, следовательно, проявляет восстановительные свойства. Еще легче с кислородом реагирует сера: она проявляет и окислительные свойства.
Неметаллы образуют как одноатомные, так и двухатомные молекулы.
К одноатомным неметаллам относятся инертные газы, практически не реагирующие даже с самыми активными веществами. Инертные газы расположены в VIII группе Периодической системы, а химические формулы соответствующих простых веществ следующие: He, Ne, Ar, Kr, Xe и Rn.
Некоторые неметаллы образуют двухатомные молекулы. Это H2, F2, Cl2, Br2, I2 (элементы VII группы Периодической системы), а также кислород O2 и азот N2. Из трехатомных молекул состоит газ озон (O3).
Для веществ неметаллов, находящихся в твердом состоянии, составить химическую формулу довольно сложно. Атомы углерода в графите соединены друг с другом различным образом. Выделить отдельную молекулу в приведенных структурах затруднительно. При написании химических формул таких веществ, как и в случае с металлами, вводится допущение, что такие вещества состоят только из атомов. Химические формулы, при этом, записываются без индексов — C, Si, S и т. д.
Такие простые вещества, как озон и кислород, имеющие одинаковый качественный состав (оба состоят из одного и того же элемента — кислорода), но различающиеся по числу атомов в молекуле, имеют различные свойства. Так, кислород запаха не имеет, в то время как озон обладает резким запахом, который мы ощущаем во время грозы. Свойства твердых неметаллов, графита и алмаза, имеющих также одинаковый качественный состав, но разное строение, резко отличаются (графит хрупкий, алмаз твердый). Таким образом, свойства вещества определяются не только его качественным составом, но и тем, сколько атомов содержится в молекуле вещества и как они связаны между собой.
Неметаллы в виде простых тел находятся в твердом или газообразном состоянии (исключая бром — жидкость). Они не имеют физических свойств, присущих металлам. Твердые неметаллы не обладают характерным для металлов блеском, они обычно хрупки, плохо проводят электрический ток и тепло (за исключением графита).
Оксиды неметаллов относят к кислотным оксидам, которым соответствуют кислоты. С водородом неметаллы образуют газообразные соединения (например HCl, H2S, NH3). Водные растворы некоторых из них (например, галогеноводородов) — сильные кислоты. С металлами типичные неметаллы дают соединения с ионной связью (например, NaCl). Неметаллы могут при определенных условиях между собой реагировать, образуя соединения с ковалентной полярной (H2O, HCl) и неполярной связями (CO2).
С водородом неметаллы образуют летучие соединения, как, например, фтороводород HF, сероводород H2S, аммиак NH3, метан CH4. При растворении в воде водородные соединения галогенов, серы, селена и теллура образуют кислоты той же формулы, что и сами водородные соединения: HF, HCl, HCl, HBr, HI, H2S, H2Se, H2Te.
При растворении в воде аммиака образуются аммиачная вода, обычно обозначаемая формулой NH4OH и называемая гидроксидом аммония. Ее также обозначают как NH3H2O и называют гидратом аммиака.
С кислородом неметаллы образуют кислотные оксиды. В одних оксидах они проявляют максимальную степень окисления, равную номеру группы (например, SO2, N2O5), а других — более низкую (например, SO2, N2O3). Кислотным оксидам соответствуют кислоты, причем из двух кислородных кислот одного неметалла сильнее та, в которой он проявляет более высокую степень окисления. Например, азотная кислота HNO3 сильнее азотистой HNO2, а серная кислотаH2SO4 сильнее сернистой H2SO3.
Самые типичные неметаллы имеют молекулярное строение, а менее типичные — немолекулярное. Этим и объясняется отличие их свойств.
Кристаллический бор В (как и кристаллический кремний) обладает очень высокой температурой плавления (2075°С) и большой твердостью. Электрическая проводимость бора с повышением температуры сильно увеличивается, что дает возможность широко применять его в полупроводниковой технике. Добавка бора к стали и к сплавам алюминия, меди, никеля и др. улучшает их механические свойства.
Бориды (соединения бора с некоторыми металлами, например с титаном: TiB, TiB2) необходимы при изготовлении деталей реактивных двигателей, лопаток газовых турбин.
Как видно из схемы № 2, углерод С, кремний Si, бор В имеют сходное строение и обладают некоторыми общими свойствами. Как простые вещества они встречаются в двух видоизменениях — в кристаллическом и аморфном. Кристаллические видоизменения этих элементов очень твердые, с высокими температурами плавления. Кристаллический кремний обладает полупроводниковыми свойствами.
Все эти элементы образуют соединения с металлами — карбиды, силициды и бориды (CaC2, Al4C3, Fe3C, Mg2Si, TiB, TiB2). Некоторые из них обладают большей твердостью, например Fe3C, TiB. Карбид кальция используется для получения ацетилена. Если сравнить расположение электронов по орбиталям ф атомах фтора, хлора и других галогенов, то можно судить и об их отличительных свойствах. У атома фтора свободных орбиталей нет. Поэтому атомы фтора могут проявить только валентность I и степень окисления — 1. В атомах других галогенов, например в атоме хлора, на том же энергетическом уровне имеются свободные d-орбитали. Благодаря этому распаривание электронов может произойти тремя разными путями.
В первом случае хлор может проявить степень окисления +3 и образовать хлористую кислоту HClO2, которой соответствуют соли — хлориты, например хлорит калия KClO2.
Во втором случае хлор может образовать соединения, в которых степень окисления хлора +5. К таким соединениям относятся хлороноватая кислота HClO3 и ее соли — хлораты, например хлорат калия КClO3 (бертолетова соль).
В третьем случае хлор проявляет степень окисления +7, например в хлорной кислоте HClO4 и в ее солях — перхлоратах, например в перхлорате калия КClO4.
Кислородные и водородные соединения неметаллов. Краткая характеристика их свойств.
С кислородом неметаллы образуют кислотные оксиды. В одних оксидах они проявляют максимальную степень окисления, равную номеру группы (например, SO2, N2O5), а других — более низкую (например, SO2, N2O3). Кислотным оксидам соответствуют кислоты, причем из двух кислородных кислот одного неметалла сильнее та, в которой он проявляет более высокую степень окисления. Например, азотная кислота HNO3 сильнее азотистой HNO2, а серная кислота H2SO4 сильнее сернистой H2SO3.
Характеристики кислородных соединений неметалов:
- 1. Свойства высших оксидов (т. е., оксидов, в состав которых входит элемент данной группы с высшей степенью окисления) в периодах слева направо постепенно изменяются от основных к кислотным;
- 2. В группах сверху вниз кислотные свойства высших оксидов постепенно ослабевают. Об этом можно судить по свойствам кислот, соответствующих этим оксидам;
- 3. Возрастание кислотных свойств высших оксидов соответствующих элементов в периодах слева направо объясняется постепенным возрастанием положительного заряда ионов этих элементов;
- 4. В главных подгруппах периодической системы химических элементов в направлении сверху вниз кислотные свойства высших оксидов неметаллов уменьшаются.
С металлами водород образует (за некоторым исключением) нелетучие соединения, которые являются твердыми веществами немолекулярного строения. Поэтому их температуры плавления сравнительно высоки.
С неметаллами водород образует летучие соединения молекулярного строения. В обычных условиях это газы или летучие жидкости.
В периодах слева направо кислотные свойства летучих водородных соединений неметаллов в водных растворах усиливается. Это объясняется тем, что ионы кислорода имеют свободные электронные пары, а ионы водорода — свободную орбиталь, то происходит процесс, котроый выглядит следующим образом:
H2O + HF > H3O + F.
Фтороводород в водном растворе отщепляет положительные ионы водорода, т. е., проявляет кислотные свойства. Этому процессу способствует и другое обстоятельство: ион кислорода имеет неподеленную электронную пару, а ион водорода — свободную орбиталь, благодаря чему образуется донорно-акцепторная связь.
При растворении аммиака в воде происходит противоположный процесс. А так как ионы азота имеют неподеленную электронную пару, а ионы водорода — свободную орбиталь, возникает дополнительная связь и образуются ионы аммония NH4+ и гидроксид-ионы ОН-. В результате раствор приобретает основные свойства. Этот процесс можно выразить формулой:
окисление металл молекулярный.
H2O + NH3 > NH4 + OH.
Молекулы аммиака в водном растворе присоединяют положительные ионы водорода, т. е., аммиак проявляет основные свойства.
Теперь рассмотрим, почему водородное соединение фтора — фтороводород HF — в водном растворе является кислотой, но более слабой, чем хлороводородная. Это объясняется тем, что радиусы ионов фтора значительно меньше, чем ионов хлора.
Поэтому ионы фтора гораздо сильнее притягивают к себе ионы водорода, чем ионы хлора. В связи с этим степень диссоциации фтороводородной кислоты значительно меньше, чем соляной кислоты, т. е., фтороводородная кислота слабее соляной кислоты.