Объем и состав продуктов полного сгорания

Если в состав горючего вещества входит кислород, то при горении он будет расходоваться на окисление горючих компонентов (углерода, водорода, серы, фосфора) и, поэтому из воздуха на горение будет израсходовано кислорода меньше на количество, которое содержалось в горючем веществе. Следовательно, в продуктах горения и азота будет меньше на количество, которое приходилось бы на кислород, если бы… Читать ещё >
Объем и состав продуктов полного сгорания (реферат, курсовая, диплом, контрольная)
Знание количества и состава продуктов горения позволяет вычислять такие характеристики процесса горения, как температуру горения, температуру взрыва и давление при взрыве. Продукты горения могут быть влажными и сухими. Во влажных продуктах объем водяных паров учитывается, а в сухих — нет. Объем продуктов горения выражается в метрах кубических на килограмм (м3/кг) или на метр кубический (м3/м3) горючего вещества, а состав — в объемных процентах.
Состав продуктов горения зависит от химической природы горючего материала и условий его горения. Практически всегда органические вещества горят с образованием продуктов полного и неполного горения.
К продуктам полного сгорания относятся: углекислый газ, образующийся при горении углерода, разложении карбонатов; водяной пар, образующийся при горении водорода и испарении влаги в исходном веществе; оксид серы (IV) SO2 и азот — продукты горения соединений, содержащих серу и азот.
Продукты неполного сгорания — это оксид углерода (II) — угарный газ СО, сажа С, продукты термоокислительного разложения — смолы.
Неорганические вещества сгорают, как правило, до соответствующих оксидов.
Выход продуктов неполного горения количественно установить невозможно из-за чрезвычайной сложности их состава, поэтому материальный баланс процесса горения рассчитывается из предположения, что вещество сгорает полностью до конечных продуктов. При этом в состав продуктов горения включают также азот воздуха, израсходованного на горение, и избыток воздуха при > 1.
Как и в случае расчета объема воздуха, необходимого для горения, свои особенности имеет расчет продуктов горения для индивидуальных веществ, смеси газов и веществ с известным элементным составом.
В случае, когда горючее — индивидуальное химическое соединение, расчет объема продуктов горения ведется по уравнению реакции горения:
м3.
где:
Vпг — объем продуктов горения;
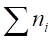
— общее число кмолей продуктов горения, которые выделяются при сгорании одного кмоля горючего вещества:
= n1(СО2) +n2(Н2O) +n3(SO2) +n4(HCl) + n5(N2) +.;
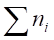
m — масса горючего вещества, кг;
VM — объем кмоля продуктов горения;
М — молярная масса горючего вещества, кг/м3.
Если горение протекает с избытком воздуха, то при расчете общего числа кмолей продуктов горения учитывается избыточное число кмолей кислорода и азота:
= (-1) — число кмолей кислорода в избытке вздуха (остаточного кислорода);
= 3,76· (-1) — число кмолей азота в избытке воздуха.
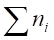
Процентный состав продуктов горения рассчитывается, исходя из общего числа кмолей продуктов горения. Общее число кмолей продуктов горения (= n1CO2) + n2(H2O) + n3(SO2) + n4(НСl) + n5(N2) + +) принимается за 100% и вычисляется процентное содержание каждого компонента продуктов горения.
ц (СО2) = n1(СО2)· 100/?ni; %; ц (Н2О) = n2(H2O) · 100/?ni; %;
ц (SО2) = n3(SО2)· 100/?ni; %; ц (НСl) = n4(HCl) · 100/?ni; %;
ц (N2) = [n5 (N2)+Дnазота]· 100/?ni; % ;
ц (O2) = Дnкисл · 100/?ni; % .
Если требуется рассчитать объем отдельного компонента продуктов горения, выделившегося при сгорании данного весового количества вещества, то такой расчет ведут по формуле:
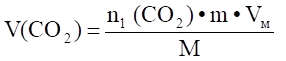
; м3 ;
Пример расчета объема и состава продуктов горения по уравнению химической реакции Условие: Определить объем и состав в объемных % продуктов горения, образовавшихся при сгорании 1 кг бензола С6Н6. Начальная температура окружающей среды 200С, давление 770 мм рт.ст., коэффициент избытка воздуха = 1.4, температура горения 1500 °C.
1. Записываем уравнение реакции горения С6Н6 + 7,5(О2 + 3,76N2) = 6СО2 + 3Н2О + 7,53,76N2.
2. По уравнению реакции горения определяем количество каждого из продуктов сгорания:
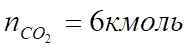
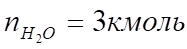
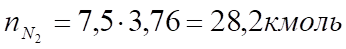
Поскольку в рассматриваемом случае горение протекает с избытоком воздуха (), необходимо учесть остаточный кислород в продуктах сгорания и азот в избытке воздуха:
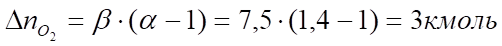
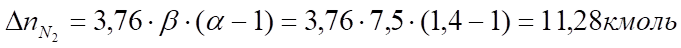
Таким образом, практический состав продуктов сгорания следующий:
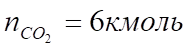
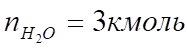
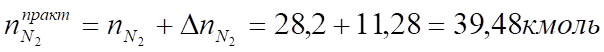
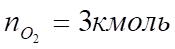
3. Определяем общее количество продуктов сгорания при сжигании 1 киломоля горючего:
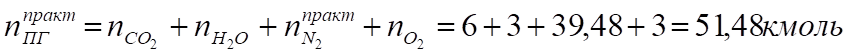
4. Определяем процентный состав продуктов горения:
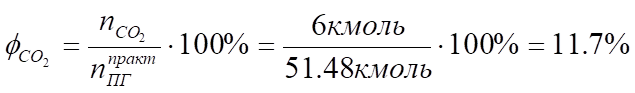
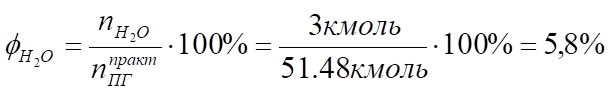
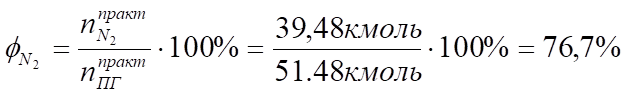
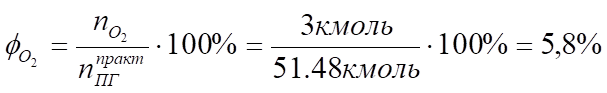
Производим проверку:
Поскольку известно, что 1 киломоль любого газа или пара при одинаковых условиях занимает одинаковый объем, то найденные концентрации также будут являться и объемными концентрациями продуктов сгорания.
5. Определяем общее количество продуктов сгорания при сжигании 1 кг горючего, для этого составляем пропорцию:
Отсюда:
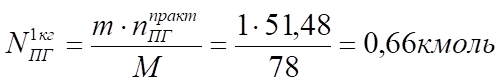
6. При определения общего объема продуктов сгорания, примем, что нагретые до высокой температуры продукты сгорания отдают свою теплоту в окружающее пространство и строительным конструкциям, поэтому температуру продуктов сгорания принимаем 20 °C (см. условие задачи).
Рассчитаем, какой объем занимает 1 кмоль газообразных веществ при заданных температуре и давлении.
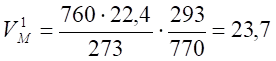
м3/кмоль Объем продуктов сгорания составит:
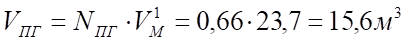
ОТВЕТ:
При сжигании 1 кг бензола при заданных условиях выделяется 15,6 м³ продуктов сгорания, из них: СО2 — 11,7%; Н2О — 5,8%; N2 — 76,7%; О2 — 5,8%.
Расчет по элементному составу вещества В этом случае теоретический выход продуктов горения определяется как сумма продуктов горения каждого элемента, входящего в состав вещества.
Рассчитаем, сколько киломолей и какой теоретический объем продуктов горения образуется при сгорании 1 кг каждого элемента при нормальных условиях.
Для углерода:
1 кг n1, х1 м3 n2, х2 м3.
С + (О2 + 3,76N2) = СО2 + 3,76N2.
М=12 кг/кмоль 1кмоль;22,4 м³ 3,76кмоль; 3,7622,4 м³.
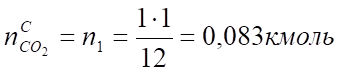
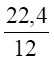
V (СО2) = х1 = = 1,87 м³.
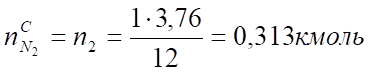
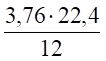
V (N2) = х2 = = 7,0 м³.
Для водорода:
1 кг n1, х1 м3 n2, х2 м3.
Н + 0,25(О2 + 3,76N2) = 0,5Н2О + 0,253,76N2.
М=1 кг/кмоль 0,5кмоль; 0,522,4 м³ 0,25· 3,76 кмоль; 0,253,7622,4 м³.

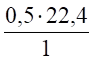
V (Н2О) = х1 = = 11,2 м³.
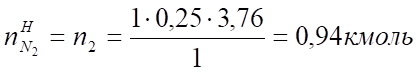
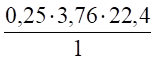
V (N2) = х2 = = 21,0 м³.
Для серы:
- 1 кг n1, х1 м3 n2, х2 м3
- S + (О2 + 3,76N2) = SО2 + 3,76N2
М=32 кг/моль 1кмоль;22,4 м³ 3,76 кмоль;3,7622,4 м³.
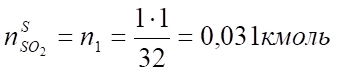
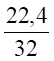
V (SО2) = х1 = = 0,7 м³.
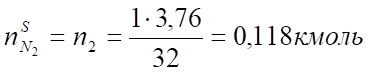
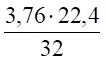
V (N2) = х2 = = 2,63 м³.
Для фосфора:
1 кг n1, х1 м3 n2, х2 м3.
Р + 1,25(О2 + 3,76N2) = 0,5Р2О5 + 1,253,76N2.
31 кг 0,5кмоль; 0,522,4 м³ 1,25· 3,76кмоль; 1,253,7622,4 м³.
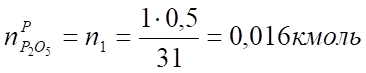
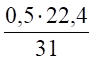
V (Р2О5) = х1 = = 0,36 м³.
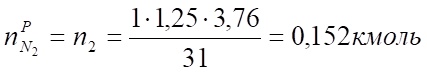
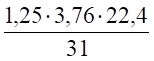
V (N2) = х2 = = 3,4 м³.
В состав горючего вещества может входить азот, влага, которые удаляются вместе с продуктами горения.
Объем 1 кг азота при нормальных условиях составит:
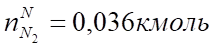
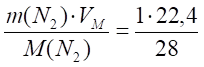
V (N2) = = 0,8 м³.
При нормальных условиях 1 кг паров воды займет объем:
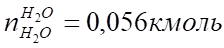
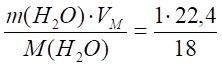
V (Н2О) = = 1,24 м³.
Если в состав горючего вещества входит кислород, то при горении он будет расходоваться на окисление горючих компонентов (углерода, водорода, серы, фосфора) и, поэтому из воздуха на горение будет израсходовано кислорода меньше на количество, которое содержалось в горючем веществе. Следовательно, в продуктах горения и азота будет меньше на количество, которое приходилось бы на кислород, если бы он находился не в горючем веществе, а в воздухе.
На 1 кг кислорода в воздухе будет приходиться объем азота, равный.
V (N2) = = 2,63 м³.
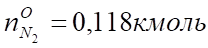
Полученные значения выходов продуктов горения элементов приведены в таблице 2.
Таблица 2. Теоретический выход продуктов горения элементов сложных веществ при нормальных условиях.
Элемент. | Объем продуктов горения (м3) на 1 кг вещества. | ||||||||
СО2. | Н2О. | SO2. | Р2О5. | N2. | |||||
кмоль. | м3. | кмоль. | м3. | кмоль. | м3. | кмоль. | м3. | кмоль. | м3. |
Углерод. | 0,083. | 1,86. | 0,313. | 7,0. | |||||
Водород. | 0,5. | 11,2. | 0,94. | 21,0. | |||||
Сера. | 0,031. | 0,7. | 0,118. | 2,63. | |||||
Фосфор | 0,016. | 0,36. | 0,152. | 3,4. | |||||
Азот в горючем. | 0,036. | 0,8. | |||||||
Азот за счет кислорода в горючем. | — 0,118. | 2,63. | |||||||
Влага в горючем. | 0,056. | 1,24. |
Используя данные таблицы можно определить количество и состав продуктов горения, а так же вычислить объем продуктов горения любого вещества с известным элементным составом при нормальных условиях.
Пусть ©, (Н), (S), (О), (N) — - массовые доли элементов в веществе, %; (W) — содержание влаги в веществе, %.
Тогда общие формулы для расчета каждого компонента продуктов горения при сгорании заданной массы (m) вещества будут иметь следующий вид:
Углекислый газ:
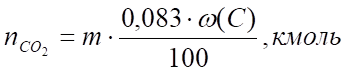
(10).
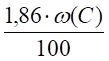
V (СО2) = m, м3(11).
Вода:
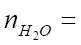
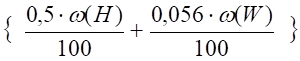
m, кмоль (12).
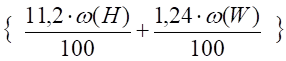
V (H2O) = m, м3(13).
Оксид серы:
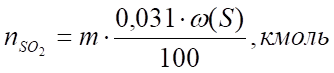
(14).
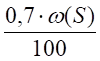
V (SО2) = m, м3(15).
Азот:
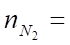
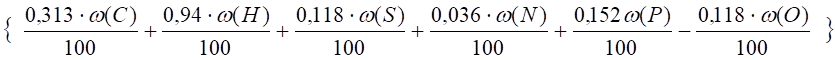
m (16).
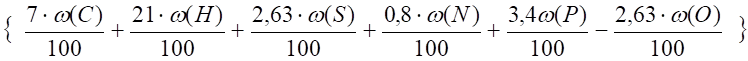
V (N2) = m, м3 (17).
В случае, когда горение происходит при избытке воздуха, т. е. коэффициент избытка воздуха, при расчетах необходимо учесть остаточное содержание кислорода и азот в избытке воздуха:
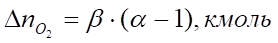
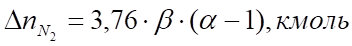
В случае, если условия окружающей среды, по условиям задачи, отличаются от нормальных, полученный объем следует привести к заданным условиям.
Далее задача решается аналогично как для индивидуального химического вещества.
Пример расчета по элементному составу Условие: Представить бутанол С4Н9ОН как вещество сложного элементного состава. Определить объем и состав в объемных % продуктов горения, образовавшихся при сгорании 1 кг этого вещества. Начальная температура окружающей среды 300С, давление 95 кПа, коэффициент избытка воздуха = 1,4.
Решение:
1. Вычислим массовые доли элементов в веществе:
Молярная масса бутанола составляет.
М (С4Н10О) = 124 + 10 + 16 = 74 кг/кмоль.
© = = 64,9%;
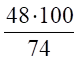
(Н) = = 13,5%;
(О) = = 21,6%.
2. Условия отличаются от нормальных, следовательно, необходимо определить, какой объем будет занимать 1 кмоль любого газообразного вещества при данных условиях (расчет VМ).
Для заданных в задаче условий:
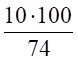
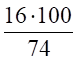
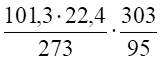
VМ = = 26,5 м3/кмоль.
3. Вычислим число киломолей каждого компонента продуктов горения.
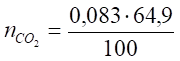
= 0,053 кмоль.
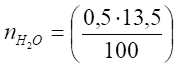
= 0,0675 кмоль.
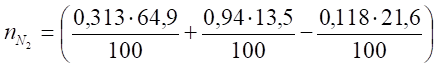
= 0,305 кмоль В состав продуктов горения входит избыточный воздух.
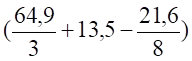
= 0,0119 (1,4 — 1) = 0,154 кмоль.
n (ПГ) = 0,053 + 0,0675 + 0,305 + 0,154 = 0,580 кмоль.
4. Суммарный объем продуктов горения составит:
V (ПГ) = n (ПГ) VМ = 0,580 26,5 = 15,4 м³.
5. Процентный состав продуктов горения.
(СО2) = = 9,2%;
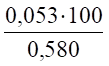
(Н2О) = = 11,6%;
(N2) = = 52,6%;
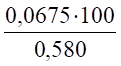
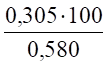
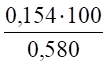
(возд) = = 26,6%.
Ответ: объем продуктов горения бутанола при заданных условиях составляет 15,4 м3/кг; объемные доли продуктов горения составляют:
(СО2) = 9,2%; (Н2О) = 11,6%; (N2) = 52,6%; (возд) = 26,6%.