Разработка системы дентальных имплантатов для реабилитации больных с полным отсутствием зубов

Основные материалы диссертации докладывались и обсуждались на: Международной научно-практической конференции «Актуальные проблемы стоматологической имплантации» (Минск, июль 1996 г.), специализированном научно-практическом семинаре «The Radix Dental Implant System: conception, hardware, clinical use» (Хайдарабад, Индия, апрель 1997 г.), Международной конференции «Workshop & Hands on Training… Читать ещё >
Разработка системы дентальных имплантатов для реабилитации больных с полным отсутствием зубов (реферат, курсовая, диплом, контрольная)
Общая характеристика работы
Актуальность исследования
По данным Всемирной Организации Здравоохранения полной адентией страдает около 15% взрослого населения планеты [NIH publication, no. 87−2868]. Более того, отмечается неуклонный рост числа больных с полной утратой зубов не только среди пожилых людей за счёт увеличения продолжительности жизни, но и среди лиц трудоспособного возраста [Ettinger R.L., 1993]. Согласно расчётам C. Douglas (1996) и A. Furino (1997), в ближайшие десятилетия около половины больных с полной утратой зубов одной или обеих челюстей будут составлять люди в возрасте от 30 до 50 лет.
Кроме нарушения функций жевания и речи, полная адентия приводит к изменениям анатомо-топографических пропорций лица и лицевого скелета, прогрессирующей атрофии и остеопорозу челюстей, атрофии жевательных и мимических мышц, дисфункции этих мышц и височно-нижнечелюстных суставов. В результате отсутствия полноценного питания, изменения внешнего вида, проблем в общении с людьми образуется целый комплекс психосоматических реакций больного, которые часто приводят к его социальной самоизоляции [Blau Z., 1995; Beck J., Hunt R., 1997].
Таким образом, лечение больных страдающих полной адентией является не только актуальной междисциплинарной проблемой ортопедической и хирургической стоматологии, но и социальной проблемой. Учитывая, что большое количество больных должны будут пользоваться зубными протезами более 20-ти лет, задачами реабилитации должны считаться:
- — восстановление функции жевания и речи;
- — профилактика атрофии и остеопороза челюстей;
- — максимально возможное сокращение сроков функциональной адаптации больных к зубным протезам;
- — создание условий для эффективной социальной адаптации больных полной адентией.
Решение этих задач может быть осуществлено только с учётом патогенеза морфологических и функциональных изменений зубочелюстной системы, являющихся следствием полной утраты зубов.
Основой профилактики прогрессирующей атрофии, остеопороза челюстей и предупреждения изменений топографо-анатомических пропорций челюстно-лицевой области при полной адентии является сохранение кровоснабжения, микроциркуляции и восстановление биоэлектрической активности костной ткани челюстей.
В настоящее время, для лечения больных с полным отсутствием зубов применяются ортопедическое лечение с помощью полных съёмных зубных протезов, а также комбинированное лечение, включающее хирургические методы коррекции топографо-анатомических условий для съёмного протезирования и эндопротезирование (имплантацию) для съёмного и несъёмного протезирования.
Использование внутрикостных имплантатов для фиксации съёмных зубных протезов повышает жевательную активность по сравнению с традиционным съёмным протезированием на 19 — 44%, а также позволяет почти полностью восстановить двигательную и тоническую активность жевательных мышц [Дудко А.С., 1993; Канатов В. А., 1991; Carlsson G., Haraldson T., 1985].
При несъёмном протезировании на внутрикостных имплантатах жевательные усилия могут достигать 412N, восстанавливаются миостатические, миодинамические рефлексы и нормализуется функция височно-нижнечелюстных суставов [Hobo S., Ichida E., Garcia L., 1990]. Внутрикостная имплантация обеспечивает биомеханические и активизирует близкие к естественным условиям обменные процессы в окружающих тканях [Дудко А.С., 1993; Канатов В. А., 1991; Олесова В. Н., 1997].
Таким образом, с точки зрения эффективности восстановления утраченных функций, профилактики атрофии и остеопороза челюстей, а также социальной адаптации, метод имплантации может рассматриваться как один из наиболее приемлемых способов реабилитации больных полной адентией.
Клинические наблюдения показали, что в 75−99% случаев различные по форме и конструкции имплантаты могут выполнять функцию опоры зубных протезов от 5 до 15 лет [Adell R., Lekholm U., Rockler B. A., 1981; Ganeles G., Rosenberg M., Holt R., 2001; Mich C., 2004; Fischer K., Stenberg T, 2006]. Однако разнообразие форм имплантатов и методик их применения при полной адентии свидетельствует об отсутствии на сегодняшний день единой стратегии имплантации для реабилитации больных полной адентией. Кроме того, до сих пор не сформулированы критерии выбора однои двухэтапной методик применения имплантатов и показания к их применению для восстановления анатомической целостности зубных рядов при полном их отсутствии.
Это обуславливает необходимость дальнейшей разработки конструкций имплантатов, алгоритма и методик их применения с учётом анатомо-топографических изменений, сопровождающих полную адентию.
Цель исследования:
Разработать, обосновать и внедрить в клиническую практику систему дентальных имплантатов и алгоритм их применения у больных с полным отсутствием зубов для эффективной реабилитации данной категории пациентов.
Задачи исследования:
- 1. Провести анализ условий для достижения интеграции имплантатов с костной тканью на основе экспериментальных и морфологических исследований.
- 2. Изучить биофизические и морфологические аспекты препарирования костной ткани для разработки инструментального обеспечения новой системы имплантатов и методики атравматичного препарирования костного ложа имплантатов.
- 3. Изучить морфологические особенности динамики интеграции имплантатов с костной тканью и на основе полученных результатов определить критерии сроков включения дентальных имплантатов в функциональную нагрузку.
- 4. Изучить зависимость силы интеграции имплантатов с костной тканью в зависимости от их макроконструкции и структуры поверхности.
- 5. Определить и систематизировать анатомо-топографические условия, оказывающие существенное влияние на выбор конструкции имплантатов и методики их применения у больных полной адентией.
- 6. Разработать оригинальную систему дентальных имплантатов и алгоритм их применения при различных анатомо-топографических условиях у больных с полным отсутствием зубов.
- 7. Провести доклинические исследования и решить процедурные вопросы сертификации и патентования разработанной системы имплантатов на территории стран СНГ.
- 8. Изучить клинические возможности и эффективность внедрения разработанной системы имплантатов при различных анатомо-топографических условиях для реабилитации больных с полным отсутствием зубов.
Научная новизна:
- 1. Изучена динамика интеграции имплантатов и проведена гистоморфометрическая характеристика остеоинтеграции, сила интеграции имплантатов с костной тканью, морфологические условия для достижения контактного остеогенеза.
- 2. Систематизированы анатомо-топографические условия для имплантации у больных с полным отсутствием зубов и выделены клинические их фенотипы.
- 3. Разработана система дентальных имплантатов, созданная с учётом анатомо-топографических изменений челюстно-лицевой области у больных с полным отсутствием зубов.
- 4. Разработан алгоритм выбора конструкции и формы имплантатов, методики имплантации и сроков функциональной нагрузки в зависимости от типа архитектоники челюстных костей.
- 5. Разработана клинически эффективная и социально адаптированная к условиям СНГ система имплантатов, позволяющая использовать единую ортопедическую платформу для изготовления различных видов зубных протезов больным с полным отсутствием зубов.
- 6. Создана база для продолжения научных и клинических исследований в стоматологической имплантологии, а также широкого применения метода имплантации в стоматологической практике.
Основные положения, выносимые на защиту:
- 1. Теоретические и экспериментальные исследования при создании новой системы дентальных имплантатов. Объективизация биофизических данных о процессе препарирования костной ткани ложа под имплантаты, изучение морфологии и динамики интеграции имплантатов с костной тканью.
- 2. Обоснование применения размеров и конфигураций внутрикостных дентальных имплантатов с точки зрения особенностей остеогенеза компактного и губчатого слоёв, а также фенотипов архитектоники костной ткани челюстей.
- 3. Характеристика типов имплантатов и их компонентов на основе морфологических и клинических исследований имплантационной системы. Алгоритм выбора типа, размеров, методики операции и сроков функциональной нагрузки на имплантаты. Рекомендации к практическому их использованию.
- 4. Результаты клинического внедрения разработанной системы дентальных имплантатов за период 1996;2007 гг. Применение имплантатов разработанной системы в различных клинических ситуациях.
Апробация работы
Основные материалы диссертации докладывались и обсуждались на: Международной научно-практической конференции «Актуальные проблемы стоматологической имплантации» (Минск, июль 1996 г.), специализированном научно-практическом семинаре «The Radix Dental Implant System: conception, hardware, clinical use» (Хайдарабад, Индия, апрель 1997 г.), Международной конференции «Workshop & Hands on Training on Oral Implantology» (Нью Дели, Индия, май 1997 г.), III Съезде Стоматологов Республики Беларусь (Минск, ноябрь 1997 г.), научно-практической конференции стоматологов «Янтарный край России — стоматология XXI век» (Калининград, апрель 1999 г.), V Съезде Стоматологической Ассоциации России (Москва, сентябрь 1999 г.), I Международном Конгрессе Итальянской Академии Стоматологической Имплантологии (Верона, октябрь 1999 г.), VIII Петербургском Международном Линков-Бюркель Симпозиуме «Клиническая имплантология и стоматология» (С.-Петербург, ноябрь 2000 г.), Международной научной конференции «Использование различных систем дентальных имплантатов в ортопедической стоматологии» (Минск, октябрь 2002 г.), IV Международном Конгрессе по стоматологии (Каунас, Литва, июнь 2002 г.), I Международном Конгрессе «Функциональная и эстетическая реабилитация в стоматологии» (С.-Петербург, ноябрь 2002 г.), научно-практическом семинаре «Система „Radix“: философия, инструментальное обеспечение и клиническое применение» (С.-Петербург, ноябрь 2004 г.), научно-практическом семинаре «Система дентальных имплантатов „Radix“. Биотехнические и клинические аспекты» (Смоленск, январь 2005 г.), V ежегодной, совместной с ICOI, конференции секции имплантологов БелСА «Современные проблемы дентальной имплантации и тканевой инженерии» (Минск, февраль 2005 г.), IV Международном Конгрессе «Функциональная и эстетическая реабилитация в стоматологии» (С.-Петербург, ноябрь 2005 г.), научно-практическом семинаре «Современные подходы и технологии в дентальной имплантологии и тканевой инженерии» (Тбилиси, Грузия, март 2006 г.), II Украинском Конгрессе «Стоматологическая имплантология. Остеоинтеграция» (Киев, май 2006 г.), научно-практическом семинаре «Система дентальных имплантатов Radix: биотехническая и клиническая концепция» (Алматы, Казахстан, май 2006 г.), III Восточноевропейской конференции по проблемам стоматологической имплантации (Львов, март, 2007 г.), межкафедральном заседании кафедр; госпитальной хирургической стоматологии и челюстно-лицевой хирургии, факультетской хирургической стоматологии и имплантологии стоматологического факультета, хирургической стоматологии и челюстно-лицевой хирургии ФПКС МГМСУ (ноябрь, 2007 г.).
Практическая значимость
Обосновано клиническое применение разработанной системы имплантатов у различных категорий пациентов с полным отсутствием зубов.
Предложен алгоритм выбора конфигурации, размеров и конструкций имплантатов, а также методики их применения у больных с полным отсутствием зубов.
Обоснованы сроки функциональной нагрузки на внутрикостные дентальные имплантаты и способы протезирования на имплантатах при полной адентии.
Доказана эффективность применения разработанной системы имплантатов для реабилитации пациентов с полной адентией.
Личное участие соискателя в разработке проблемы
Автором лично была проведена серия экспериментов на 21 трупной нижней челюсти людей и 30 беспородных собаках, включенных в исследование. В ходе сбора материала для диссертационной работы соискателем были освоены методики регистрации биофизических параметров препарирования костной ткани; моделирования динамики интеграции имплантатов с костной тканью и гистоморфометрических исследований. имплантат дентальный анатомия Автором лично проведено лечение 425 пациентов, включавшее как хирургические вмешательства, так и протезирование больных.
Внедрение результатов исследования. Результаты исследования внедрены в учебный процесс кафедры госпитальной хирургической стоматологии и челюстно-лицевой хирургии, кафедры факультетской хирургической стоматологии и имплантологии МГМСУ.
Публикации
По теме диссертации опубликовано 51 научная работа, из них 7 в журналах рекомендуемых ВАК РФ, 3 монографии, получено 2 патента на изобретения.
Объём и структура диссертации
Диссертация изложена на 213 страницах и состоит из введения, обзора литературы, шести глав собственных экспериментальных и клинических исследований, заключения, выводов, практических рекомендаций и списка литературы, который включает 215 работ. Работа иллюстрирована 10 таблицами и 50 рисунками.
Материалы и методы
Для решения поставленных задач были проведены экспериментальные и клинические исследования по изучению:
- — биофизических параметров препарирования кости, их влияния на процесс регенерации кости с целью разработки режущего инструмента для разрабатываемой системы имплантатов и для проведения корректных гистологических исследований по изучению морфологии и динамики биосовместимости титановых имплантатов;
- — морфологической картины интерфейса имплантат/костная ткань через 14, 30 и 60 дней после введения имплантатов из титана. Целью данного исследования явилось определение возможных сроков достижения интеграции имплантатов и условий для ранней функциональной нагрузки на имплантаты с точки зрения сроков репаративной регенерации на уровне интерфейса имплантат/костная ткань;
- — морфологической картины и гистоморфометрии интерфейса имплантат/костная ткань у функционировавших в течение 6 месяцев имплантатов. Целью данного исследования было изучение особенностей структурной перестройки (физиологической регенерации) костной ткани на уровне интерфейса имплантат/костная ткань для определения условий необходимых для адекватного функционирования разрабатываемых имплантатов;
- — влияния структуры поверхности имплантатов на силу их интеграции с костной тканью, с целью определения оптимальной технологии иготовления внутрикостных элементов разрабатываемых имплантатов;
- — влияния технологии изготовления на степень контаминации поверхности имплантатов с целью определения оптимальной технологии изготовления разрабатываемых имплантатов;
- — влияния технологии пластического деформирования титана на качество изготовления компонентов имплантатов.
Параллельно с экспериментальными исследованиями были проведены предварительные клинические исследования по изучению:
- — особенностей архитектоники беззубых отделов челюстей при частичной и полной адентии;
- — анатомических особенностей строения челюстей у пациентов с полным отсутствием зубов.
Данные предварительные исследования были положены в основу разработки конфигурации разрабатываемых имплантатов и алгоритма их применения.
Для изучения биофизических параметров препарирования кости, исследования процесса регенерации костной ткани вокруг имплантатов и их интеграции были проведены четыре эксперимента.
В первом эксперименте проведено изучение процесса нагревания кости при различных режимах препарирования. Эксперимент проводили in-vitro, на нативных препаратах трупных нижних челюстей человека. Для проведения эксперимента была собрана установка, состоящая из настольного сверлильного устройства с подвижным в вертикальном направлении предметным столиком, динамометра, тахометра, электронного термометра и секундомера. В процессе сверления измерялась температура кости на расстоянии 0,5 мм от зоны препарирования. Одновременно измеряли время от начала препарирования до завершения формирования канала глубиной 10,0 мм. Препарирование осуществляли шаровидным, фиссурным борами и сверлами скоростях вращения от 1000 до 7000 об/мин с давлением 5 и 10N, т. е. с давлением, соответствующим минимальному и среднему нажиму хирурга на инструмент при препарировании кости в клинических условиях. Всего было произведено 144 препарирования с измерением температуры кости и времени сверления.
Второй эксперимент включал изучение влияния формы инструмента и скорости его вращения на процесс регенерации костной ткани вокруг имплантатов и проводился in-vivo. Для эксперимента использовали собак, которым имплантировали в нижнюю челюсть титановые цилиндры. Костное ложе при этом препарировали шаровидным, фиссурным борами и свёрлами на различных скоростях вращения. Во время препарирования костного ложа соблюдали общепринятые принципы формирования ложа под цилиндрические имплантаты. Всего было имплантировано 140 титановых цилиндров. Животных выводили из эксперимента через 14 и 30 дней после операции. Проводили визуальное обследование и морфологическое исследование косной ткани стенки воспринимающего ложа имплантатов.
Для изучения динамики биосовместимости внутрикостных имплантатов были проведены ещё два экспериментальных исследования in-vivo на 10 собаках, которым в нижнюю челюсть было установлено 60 имплантатов из титана марки ВТ-1.00 цилиндрической формы. Изучали морфологическую картину через 14, 30 и 60 дней после имплантации (эксперимент № 3) и через 6 месяцев после приложения функциональной нагрузки на имплантаты (эксперимент № 4).
Дополнительно, для получения объёмно-пространственного представления о характере контакта между имплантатами и окружающими тканями, проводили исследования препаратов с помощью растрового электронного сканирующего микроскопа JSM-840 фирмы JEOL (Япония) при степенях увеличения х50, х250, х500, х1000.
Для качественного анализа интеграции имплантатов было проведено гистоморфометрическое исследование интерфейса недекальнированных препаратов. Для этой цели интерфейс имплантат/костная ткань на каждом препарате был условно разделён на 34 зоны в виде сетки с размерами ячеек 1×1 мм. Для оценки морфологии поверхности раздела имплантат/кость использовали 1000-кратное увеличение. Каждая ячейка вмещала в себя 25 снимков, каждый из которых показывал участок интерфейса размером 50×50 мкм. Измерялась протяжённость различных вариантов сопряжения тканей с поверхностью имплантатов.
Исследование биомеханической прочности интеграции имплантатов с костью было проведено на 10 взрослых беспородных собаках. Животным удаляли первый и второй премоляры. Имплантацию производили в этих зонах челюстей через 3 месяца после удаления зубов.
Устанавливали имплантаты, изготовленные из компактного титана марки ВТ.1−00, и имплантаты из сферических порошков титана той же марки. Диаметр всех имплантатов составлял 3,0 мм, высота — 5,0 мм, радиус закругления верхушки — 3,0 мм. Из компактного титана имплантаты имели винтовую форму и два варианта цилиндрической формы — один имел тестурированную поверхность, второй — гладкую. Пористые имплантаты были изготовлены из сферических порошков титана методом электроимпульсного спекания с последующим допеканием в вакууме. Использовали 3 варианта пористых имплантатов, изготовленных из различных фракций сферических порошков титана с размером частиц: 0,2−0,315 мм, 0,315−0,4 мм и 0,4−0,63 мм.
Животных выводили из эксперимента через 3 месяца путём введения летальной дозы тиопентала натрия и дитилина. После этого сразу вычленяли фрагменты нижних челюстей, содержащих имплантаты. Затем распиливали сегменты челюстей таким образом, чтобы каждый костный блок содержал один имплантат. Эти блоки помещали в стандартные формочки и фиксировали их в этих формочках эпоксидной смолой. При этом сошлифовывали костную ткань в области верхушки имплантата до её оголения. Таким образом, образцы были приготовлены к биомеханическим исследованиям при помощи «теста на выталкивание».
Тест на «выталкивание» имплантатов из кости производился на универсальной испытательной машине «Instron-1195» (Великобритания). В процессе испытаний записывалась диаграмма нагружения и фиксировалась максимальная нагрузка, при которой происходит сдвиг имплантата в кости.
Объёктом конструкторско-испытательных исследований служили опытные образцы выпущенных серийно разработанных имплантатов (торговая марка Radix). Предметом изучения были:
- 1) поверхность имплантата, которую исследовали на предмет контаминации инородными материалами по сравнению с исходным материалом для изготовления имплантатов (титан марки ВТ.1−00). Испытания химического состава поверхностей производили путём рентгеноспектрального анализа и ИК-спектроскопии. Исследования проводились на аттестованном сканирующем электронном микроскопе «Нанолаб-7» фирмы «Оптон» (Германия) с микрорентгеноспектральным анализатором AN 10 000 фирмы «Линк Аналитикл» (Англия) по программе количественного анализа ZAF4-FLS.
- 2) состояние поверхности имплантатов, кристаллической решётки титана имплантата и его соединения на уровне внутрикостный элемент/ опорная головка после обработки методом пластического деформирования. Данное исследование производилось при помощи сканирующего электронного микроскопа JSM-840 фирмы JEOL (Япония). В качестве сравнения для изучения точности соединения опорной головки с внутрикостной частью имплантата исследованию подвергали аналогичные соединения имплантатов Anthogir (Франция) и Straumann (Швейцария).
Для оценки структуры кристаллической решётки исходного материала (прутки титана марки ВТ.1−00) и изготовленных по технологии пластического деформирования имплантатов, а также качества соединения компонентов имплантатов производили шлифы имплантатов. Эти шлифы изучались под сканирующим электронным микроскопом в рабочих режимах: увеличение — х10 — х5000; ускоряющее напряжение электрического поля — 20 кэВ; величина тока пучка электронов на поверхности — от 6×109 до 6×1010А.
Материалом для предварительных клинических исследований послужили наблюдения, проведенные за 825 пациентами с различными формами адентии, которым проводили имплантацию и регистрировали качество костной ткани мануально, а также клиническое обследование 425 пациентов с полной адентией, которым проводилась компьютерная томография с верификацией типов архитектоники челюстных костей и их анатомических размеров.
После проведения экспериментальных, предварительных клинических и конструкторско-испытательных исследований проводилась клиническая апробация разработанной системы имплантатов, материалом для которой послужили клинические наблюдения за 425 пациентами с полным отсутствием зубов.
Результаты экспериментальных исследований
В результате проведенных экспериментов были получены следующие данные:
Эксперимент № 1. В результате проведенных исследований в эксперименте на трупном материале были получены различные значения нагревания кости. Температура кости во время сверления с давлением 10N при скорости вращения от 1000 до 7000 об/мин максимально доходила до 29,0 — 61,5оС в случаях, когда сверление проводили шаровидным бором. При сверлении с помощью фиссурного бора температура кости была зарегистрирована в пределах 27 — 52оС. При использовании сверла максимальная температура кости была зарегистрирована в пределах 23 — 37оС. Начальная температура кости при этом колебалась в пределах 20 — 25оС.
Нагревание кости выше 4оС на расстоянии 0,5 мм от зоны сверления, т. е. выше уровня безопасного нагревания, наблюдалось во всех случаях, когда сверление производили шаровидным и фиссурным борами. Превышение безопасного уровня нагревания наблюдалось также при использовании сверла со скоростями вращения 5000 — 7000 об/мин, а при снижении давления на инструмент до 5N и со скоростью вращения 3000 об/мин.
Таким образом, оптимальным с точки зрения снижения нагревания кости и давления на инструмент, является использование сверла со скоростью вращения 1000 об/мин.
Эксперимент № 2. В случах, когда костное ложе препарировали свёрлами при 1000 об/мин, на 14-й день после имплантации костная ткань, образующая стенку ложа имплантата в 7 из 12 случаев была представлена на уровне компактного и губчатого слоёв кости очень узкой и плотной полоской грубоволокнистой ткани. У остальных 5 препаратов аналогичная полоска грубоволокнистой ткани наблюдалась только на уровне губчатого слоя, а на уровне компактного слоя была еле заметна или не выявлялась и стенка ложа была представлена неизменённой костной тканью. На всех препаратах в ограниченных участках стенки ложа отмечались отёк, расширение или полнокровие немногочисленных сосудов, имбибиция эритроцитами, но без воспаления. В пограничной со стенкой ложа зоне единичные трабекулы находились в состоянии субтотального или лакунарного рассасывания с умеренно выраженной пролиферацией остеобластов по их периферии. Местами наблюдался отёк волокнистой ткани межтрабекулярных пространств и полнокровие сосудов. Микроскопическая структура костной ткани в этих зонах была обычного строения.
На 30-й день во всех случаях на уровне компактного слоя кости стенка ложа была представлена костной тканью обычного строения. Край стенки ложа гладкий. Местами, прослеживалось врастание узкой полоски грубоволокнистой ткани с полнокровными капиллярами в участках, соответствующих канавкам на поверхности имплантатов. На уровне губчатого слоя, стенка ложа представлена тонким слоем рыхлой волокнистой ткани с обилием в её толще полнокровных тонкостенных сосудов. Часть её, непосредственно контактировавшая с имплантатом, имеет вид узкой полоски уплотнённых волокон. В пограничной зоне наблюдается лакунарное рассасывание единичных костных балок с умеренной пролиферацией остеобластов по их периферии.
В случаях, когда применялись другие режимы препарирования костного ложа во всех случаях на 14 и 30 день после операции наблюдалось выраженное воспаление в зоне стенки костного ложа с образованием грануляционной или фиброзной ткани с явным замедлением репаративных процессов костных структур в пограничной зоне.
Эксперимент № 3. Через два месяца после установки имплантатов, микроскопическое изучение шлифов кости с имплантатами выявило следующую морфологическую картину.
На уровне компактного слоя пластинчатая кость плотно окружает имплантаты. Остеоны по линии контакта с имплантатом и в пограничных участках обычного строения. Местами по линии контакта выявляются мелкие узуры в кости, окаймлённые по костному краю полоской гомогенной набухшей соединительной ткани. Узуры соответствуют по расположению и структуре фрагменту остеонного канала, оставшегося по месту распила остеонов.
В области губчатого слоя кости, имплантаты местами окаймлены относительно широкой полосой набухшей соединительной ткани, в которой отмечается концентрическое расположение волокон, появление остеобластов, набухание, гомогенизация и интенсивное прокрашивание в розовый цвет основного вещества, отмечается формирование остеоноподобных структур. Трабекулы на всём протяжении обычного строения, плотно примыкают к поверхности имплантата.
С помощью растровой электронной микроскопии, при 500- и 1000-кратном увеличении было установлено, что в местах плотного контакта между поверхностью имплантатов и окружающих структурных единиц кости, который был верифицирован на уровне светового микроскопа, имплантат и окружающую костную ткань в некоторых местах разделяет очень тонкий, толщиной всего 3−5 мкм, слой соединительной ткани.
Эксперимент № 4. После шестимесячного периода функционирования имплантатов в качестве опор мостовидных протезов визуальный осмотр показал, что у двух собак целостность протезов не нарушена, подвижности имплантатов и фиксированных на них протезов не наблюдалось. У одной собаки, с левой стороны имелся перелом протеза. При этом на одном имплантате образовалась консоль. Наблюдалась небольшая подвижность этого имплантата.
Микроскопическое исследование шлифов кости в данном эксперименте выявило следующую морфологическую картину.
На уровне компактного слоя кости имплантат окружён зрелой пластинчатой костной тканью. Кость почти на всём протяжении плотно прилежит к поверхности имплантатов и как бы спаяна с ними. Местами по линии контакта имплантатов с костью имеются короткие щелевидные пространства или мелкие узуры, которые располагаются в зоне распила остеонов по сосудистому каналу остеона.
В губчатом слое кости, костные балки плотно прилежат к поверхности имплантатов, и костная ткань повторяет рельеф поверхности имплантатов. В участках межтрабекулярных пространств, поверхность имплантата окружена узкой полоской рыхлой волокнистой ткани и непосредственного контакта с костными структурами не имеет. В некоторых шлифах нижняя часть имплантата полностью расположена в костномозговых полостях и не имеет контакта с костной тканью. В таких участках имплантаты со всех сторон окружены слоем толщиной 500−700 мкм плотной соединительной ткани, тесно прилежащей к имплантату.
Отверстия и поры имплантатов выполнены тканью слоистого строения. А именно: за слоем пластинчатой кости, прилежащей к граням отверстий или пор, следует остеогенная клеточно-волокнистая ткань в виде довольно широкой полосы, а следующая за ней более широкая полоса рыхлой волокнистой ткани имеет в своей толще сформированные, относительно толстые сосуды (сосудистые каналы).
Костная и соединительная ткань в зонах контакта с имплантатами имеет обычное строение, без патологических изменений.
Результаты гистоморфометрии. Как показали исследования, в секторах, где имплантаты находились в компактном слое кости, 79 — 81,5% их поверхности имели оссеоинтегрированный контакт; 13,3−14% поверхности — фиброзно-костную интеграцию (ширина волокнисто-тканной прослойки примерно 50 мкм); к 3,9 — 4,5% поверхности имплантата примыкает слой мягкой ткани шириной 250 мкм и более; 1,3 — 1,5% поверхности имплантата приходятся на костные полости. В секторах приходящихся на губчатый слой кости оссеоинтегрированный контакт составил 46,7 — 49% поверхности имплантата, фиброзно-костная интеграция — 32,4 — 34% и 20,9% - 22% поверхности имплантата контактируют с мягкой тканью. В секторах, приходящихся на отверстие в апикальной части имплантатов, оссеоинтегрированный контакт наблюдали на 34,5 — 36% поверхности, фиброзно-костный — на 47,3 — 49% и фиброзный — на 18,2 — 19% поверхности имплантата. Оссеоинтегрированный контакт в секторах приходящихся на компактный слой и частично на уровне губчатого слоя был представлен непосредственной связью костного матрикса с 75,3% поверхности имплантата; аморфной зоной с 23,1%; волокнистыми структурами с 1,6% поверхности имплантата. В остальных секторах на уровне губчатого слоя преобладала связь в виде аморфного слоя (68% поверхности имплантата). Непосредственный контакт костного матрикса трабекул регистрировали на 24,6% поверхности; волокнистую организацию интерфейса наблюдали на 7,4% поверхности имплантата.
Таким образом, гистоморфометрический анализ показал, что интерфейс 17 из 18 функционировавших имплантатов был представлен на уровне компактного слоя костной интеграцией (в среднем 82% площади), фиброзно-костной интеграцией (в среднем 14% площади) и контактом с фиброзной тканью (около 4% площади). На уровне губчатого слоя кости морфология интерфейса этих имплантатов выглядела иначе. Костная интеграция составила 47% площади, фиброзно-костная — 32%, контакт с мягкими тканями был зарегистрирован на 21% площади сопряжения поверхности имплантата.
Как показало исследование силы интеграции имплантатов с костной тканью (тест на выталкивание), сила приложения, необходимая для сдвига исследуемых образцов имплантатов по отношению к окружающей кости, составляла от 116 до 1097 Н. Перерасчёт полученных данных на удельное давление сдвига (усилие на единицу площади поверхности имплантата, приводящее к отрыву интегрированного имплантата от костной ткани) позволил определить, что для имплантатов диаметром 4 м и высотой 13 мм усилие сдвига может составлять у цилиндрических имплантатов с гладкой поверхностью — 698 Н; у цилиндрических имплантатов с текстурированной поверхностью — 1956 Н, у винтовых имплантатов — 3260 Н и у пористых имплантатов — от 2282 до 3586 Н.
Таким образом проведенный тест на выталкивание имплантатов показал очевидную разницу силы интеграции имплантатов в зависимости от макрорельефа и модификации их поверхности.
На основании результатов проведенных экспериментов было сделано следующее заключение.
Определение сроков протезирования на имплантатах должно быть дифференцированным, и исходить из типа архитектоники кости в зоне имплантации.
Если в области установленного имплантата костная ткань челюсти представлена гомогенным компактным слоем, к протезированию можно приступать непосредственно после операции или спустя 2−3 недели после имплантации.
В случаях, когда внутрикостная часть имплантата находится преимущественно в губчатом слое кости, оптимальным является протезирование через 2−3 месяца после имплантации.
Оптимальными с точки зрения биомеханических и остеокондуктивных свойств являются имплантаты из титана винтовой формы с тектурированной (шероховатой) поверхностью.
Результаты конструкторско-испытательных исследований. Исходя из проведенного анализа химического состава исходного материала (титан марки ВТ.1−00) и изготовленных имплантатов следует, что технология изготовления имплантатов путём пластического деформирования с последующей пескоструйной обработкой гранулами алюмооксидной керамики поверхности имплантата с целью её текстурирования не приводят к изменениям химического состава технически чистого титана и контаминации поверхности имплантатов.
Результаты проведенных санитарно-химической и токсиколого-гигиенической экспертиз подтвердили данные, проведенные при помощи рентгеноспектрального анализа и ИК-спектроскопии, конструкторско-испытательных исследований.
Как показали исследования кристаллической решётки шлифов изготовленных методом пластического деформирования имплантатов, наблюдаемое при помощи электронного сканирующего микроскопа, очевидное уплотнение кристаллической решётки технически чистого титана должно давать двойной эффект. Первое — это увеличение поверхностной энергии изделия. Второе — это увеличение прочности изделия.
Результаты предварительных клинических исследований
Результаты определения качества костной ткани челюстей
Результаты проведенного исследования позволили определить, что снижение плотности костной ткани челюстей является следствием адентии и развивается, как правило, в боковых отделах челюстей более чем у 33% больных.
Анализ полученных результатов позволил установить ряд факторов, способствующих снижению плотности костной ткани челюстей. Установлено, что сочетание 3−4 этих факторов является основанием для постановки предварительного диагноза регионарного остеопороза челюстей. Данный предварительный диагноз при адентии верхней челюсти может быть установлен у больных, страдающих адентией более двух лет, пользовавшихся съёмными протезами, имеющих значительную атрофию альвеолярного отростка и его толщину более 8 мм, а также имеющих брахицефалический тип строения лицевого отдела скелета. Исключением могут быть случаи, когда у больного с мезоили долихоцефалическим типом формы лицевого скелета срок адентии составляет менее двух лет, отсутствуют признаки атрофии кости и альвеолярный отросток полностью сохранён.
При адентии нижней челюсти регионарный остеопороз предполагается у больных, страдающих адентией более двух лет, пользовавшихся съёмными протезами со значительной атрофией альвеолярного отростка и его толщиной более 8 мм. У больных с долихоцефалическим типом строения черепа, практически во всех случаях, даже при отсутствии вышеперечисленных признаков, регионарный остеопороз может сопровождать адентию в боковых отделах нижней челюсти.
Результаты исследований по определению объёма и архитектоники костной ткани челюстей при полной адентии
Из 425 обследованных пациентов с полной адентией у 114 высота кости в боковых отделах челюстей (h), т. е расстояние от гребня альвеолярного отростка до нижнечелюстного канала или дна верхнечелюстной пазухи составляла более 10 мм. У большинства пациентов (225 человек) данное расстояние составляло 8 — 10 мм и, таким образом, отсутствовали анатомические условия для проведения имплантации в боковых отделах челюстей (табл.1). В то же время у всех этих пациентов (339 человек) высота кости во фронтальных отделах челюстей (H) составляла более 12 — 15 мм. У 56 пациентов высота в боковых отделах челюстей составляла менее 8 мм, а во фронтальных отделах всего — от 8 до 10 мм.
Таблица 1. Данные измерений объёма челюстных костей пациентов с полным отсутствием зубов
Анатомический тип. | Кол-во пациентов. | Толщина. | Межкортикальное расстояние. | Возраст. | ||
в/челюсти. | н/челюсти. | |||||
А. h > 10,0 mm. H > 15,0 mm. | 114 (27%). | < 7 мм ;
> 4 мм ; 4 (3,5%). | < 7 мм ;
> 4 мм ; 2 (1,5%). |
|
После 60 лет — 42%. | |
Б. h 8 — 10 mm. H > 12,0 mm. | 255 (60%). | < 7 мм ;
> 4 мм ; 7 (3%). | < 7 мм ;
> 4 мм ; 9 (3,5%). |
|
После 60 лет — 31%. | |
В. h < 8,0 mm. H 8 — 10 mm. | 56 (13%). | < 7 мм ;
> 4 мм ; 2 (3,5%). | < 7 мм ;
> 4 мм ; 2 (3,5%). |
|
После 60 лет — 41%. | |
Измерения челюстей по данным компьютерной томографии показало, что у большинства пациентов вне зависимости от выраженности атрофии и высоты кости толщина кости составляет 7 и более мм, а межкортикальное расстояние от 3 до 7 мм. У 67 пациентов толщина нижних челюстей составляла 4 — 6 мм, а у 93 аналогичная толщина наблюдалась у верхних челюстей. Толщина челюстей менее 4 мм была у 13 пациентов. Межкортикальное расстояние у пациентов с толщиной челюстей менее 6 мм составляло от 0 мм (полностью отсутствовал губчатый слой кости) до 4 мм.
Анализ компьютерных томограмм позволил выявить визуально различимые варианты строения губчатого слоя костной ткани челюстей, а также его плотность по шкале Хаунсфилда (рентгеноденситометрия). Визуально различимых было выявлено 6 вариантов архитектоники костной ткани челюстей (рис.1):
I тип — костная ткань челюсти представлена практически полностью компактным слоем. Наблюдали у 29 пациентов. Такой тип архитектоники чаще регистрировали во фронтальном отделе нижней челюсти (у 21 из 29 пациентов), реже в боковых её отделах и во фронтальном отделе верхней челюсти. Данный тип архитектоники наблюдали при различной степени атрофии и остаточном объёме кости.
II тип — соотношение компактного и губчатого слоёв составляет 1:1. Губчатый слой представлен немногочисленными, но очень толстыми трабекулами; толщина компактного слоя — 3−5 мм и более. Наблюдали у 98 пациентов. Такой тип архитектоники чаще регистрировали в области премоляров нижней челюсти, во фронтальном отделе и в области премоляров верхней челюсти (79 пациентов), реже — в области моляров верхней челюсти и во фронтальном отделе нижней челюсти (19 пациентов).
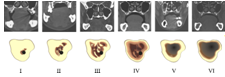
Рисунок 1. Шесть типов архитектоники костной ткани челюстей при полной адентии, верифицированных по изображениям, полученным с помощью компьютерной томографии.
III тип — соотношение компактного и губчатого слоёв составляет 1:3. Наблюдали у 224 пациентов. Толщина компактного слоя при таком типе архитектоники составляет 2−3 мм. Губчатый слой представлен равномерной, хорошо развитой сетью трабекул, однако они тонкие и не формируют чётко ориентированные устои. Такой тип архитектоники чаще встречали в области моляров нижней и верхней челюстей (157 пациентов), реже во фронтальном отделе и в области бугров верхней челюсти (65 пациентов), очень редко — во фронтальном отделе нижней челюсти (2 пациента).
IV тип — соотношение компактного и губчатого слоёв составляет 1:4 и более. Толщина компактного слоя — 1−2 мм. Губчатый слой представлен рыхлой сетью тонких трабекул. Наблюдали у 61 пациента в зоне бугров и альвеолярного отростка верхней челюсти в области моляров (32 пациента) и области моляров нижней челюсти (29 пациентов).
V тип — толщина компактного слоя составляет 2−4 мм. Губчатый слой практически отсутствует. Наблюдали у 9 пациентов с выраженной атрофией челюстей и только в боковых отделах (зона жевательной группы зубов).
VI тип — толщина компактного слоя составляет не более 0,5−1,5 мм. Губчатый слой отсутствует. Наблюдали у 4 пациентов с умеренно выраженной атрофией в боковых отделах челюстей.
Каждый из выделенных типов архитектоники верифицировался и по шкале Хаунфилда (рис.1): I тип — от 600 до 1000 HU, II — тип — от 400 до 600 HU, III тип — от 300 до 400 HU, IV тип — от 200 до 300 HU, V и VI типы — менее 200 HU.
Измерения остаточной высоты кости беззубых челюстей показали, что у 27% пациентов были удовлетворительные анатомические условия для проведения имплантации. 42% из этих пациентов были в возрасте после 60 лет, 38% в возрасте от 40 до 60 лет и 20% - 27- 40 лет. При наличии достаточной для проведения имплантации высоты костной ткани у 1,5 — 3,5% пациентов имел место дефицит толщины альвеолярных отростков. Причём, толщину кости менее 4 мм регистрировали у пациентов в возрасте от 27 до 40 лет, в большинстве случаев у женщин. У половины пациентов (56 человек) с достаточным для имплантации объёмом костной ткани регистрировали IV тип архитектоники костной ткани челюстей, у 29 (25%) — III тип архитектоники, у 28 (24%) — I — II тип архитектоники и у 1 пациента (1%) — V тип архитектоники.
У большинства пациентов (60%) наблюдали снижение высоты костной ткани в зоне жевательной группы зубов и премоляров до 8 — 9 мм, но с сохранением достаточной высоты кости (более 12 мм) во фронтальных отделах челюстей. У 3−3,5% этих пациентов регистрировали толщину кости менее 4 мм, также преимущественно у лиц в молодом возрасте (от 27 до 40 лет). В данной группе пациентов чаще, чем в предыдущей регистрировали V — VI тип архитектоники (21 пациент или 8%), заметно также было снижение количества пациентов с I и IV типом архитектоники и увеличение количества пациентов с III типом архитектоники.
У 18% пациентов (56 человек) наблюдали выраженную атрофию челюстей, при которой высота кости в боковых отделах не превышала 4 — 5 мм, а во фронтальных отделах — 8 — 10 мм. У 24 (43%) пациентов данной группы регистрировали IV тип архитектоники, у 15 (27%) — III тип, у 7 (12%) наблюдали выраженный остеопороз, и только у 10 (18%) — I и II тип архитектоники.
На основании проведенных исследований для систематизации анатомо-топографических условий и разработки схем лечения были определены 3 фенотипа пациентов с полным отсутствием зубов:
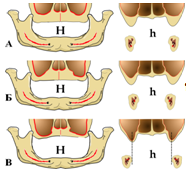
Рисунок 2. Схема трёх фенотипов анатомо-топографического состояния челюстных костей у пациентов с полным отсутствием зубов.
А — остаточная высота альвеолярных отростков в передних отделах челюстей (H) составляет 15 и более мм, в боковых (h) — более 10 мм (рис.2). Архитектоника костной ткани IIII типа, но примерно у половины пациентов, в основном у тех из них, кто пользовался съёмными зубными протезами 5 и более лет — IV тип архитектоники. В данной группе толщина альвеолярных отростков менее 6 мм наблюдается примерно у 20% человек. Данный фенотип характерен для лиц в возрасте от 40 до 60 и более лет.
Таким образом, для данного фенотипа характерно наличие удовлетворительных анатомо-топографических условий, как для ретенции полных съёмных зубных протезов, так и для проведения имплантации и несъёмного протезирования;
Б — остаточная высота в боковых отделах челюстей 8 — 10 мм, в передних отделах — 12−15 мм (рис.2). Архитектоника кости представлена I-III типом в передних отделах челюстей, в боковых отделах у большинства пациентов — IV — VI типом. Примерно у 25% пациентов толщина альвеолярных отростков составляет менее 6 мм. Примерно 70% пациентов с данным фенотипом — это лица в трудоспособном возрасте. При полной адентии одной из челюстей наблюдается смещение осей альвеолярных отростков.
Характерным для этого фенотипа является отсутствие удовлетворительных условий для ретенции полных съёмных зубных протезов и отсутствие анатомо-топографических условий для стандартных методик имплантации в боковых отделах челюстей.
В — остаточная высота в боковых отделах челюстей — менее 8 мм, в передних отделах — от 8 до 10 мм (рис.2). Отсутствует преддверие полости рта, изменена высота прикрепления уздечек губ и языка. Более чем у половины пациентов имеет место остеопороз (IV-VI тип архитектоники). Примерно у 45% архитектоника кости во фронтальных отделах челюстей представлена I-III типом архитектоники. Примерно у 25% пациентов толщина альвеолярных отростков составляет менее 6 мм. Примерно 60% пациентов с данным фенотипом — это лица в трудоспособном возрасте. Во всех случаях имеет место смещение осей альвеолярных отростков верхней и нижней челюстей.
Характерным для этого фенотипа является отсутствие условий для ретенции полных съёмных зубных протезов и анатомо-топографических условий для стандартных методик имплантации в боковых и фронтальных отделах челюстей.
Биотехническая характеристика разработанной системы имплантатов
При разработке конструкций системы имплантатов (торговая марка «Radix») для реабилитации пациентов с полным отсутствием зубов учитывались следующие результаты и наблюдения, полученные при выполнении экспериментальной и клинической частей работы:
- 1. Диаметр внутрикостных элементов имплантатов должен соответствовать вариантам объёма и межкортикального расстояния челюстей.
- 2. Конфигурация и размер имплантатов должны давать возможность их установки бии межкортикально для достижения хорошей первичной фиксации и создания условий для контактного остеогенеза.
- 3. Конструкция имплантатов должна обеспечивать возможность несъёмного и условно-съёмного протезирования.
- 4. Учитывая достаточно большое количество имплантатов, устанавливаемых пациентам с полным отсутствием зубов, конструкция имплантатов должна быть достаточно простой и иметь совместимые (унифицированные) между собой компоненты и инструменты.
- 5. Инструменты для препарирования костного ложа должны обеспечивать условия для атравматичного сверления кости, а инструменты для установки имплантатов — условия при которых можно предупредить контаминацию поверхности имплантатов.
Исходя из вышеперечисленных положений, была разработана система имплантатов, имеющих 3 типа конфигурации внутрикостных элементов и унифицированные, совместимые со всеми типами внутрикостных элементов ортопедические компоненты (рис.3).
Системообразующим (базовым) является разборный имплантат с внутрикостным элементом винтовой формы с «пассивным» профилем резьбы (торговая марка Radix-IIS). Внутрикостные элементы имеют диаметр 3,5; 4,0; 4,5 и 5,0 мм и высоту: 8, 10, 12, 15 и 18 мм (рис.3А).
Вторым (торговая марка Radix-DM), дополнительным, является неразборный имплантат винтовой формы с «агрессивным» профилем резьбы диаметром 2,8 мм. Внутрикостная его часть имеет переменное сечение: в нижней части — трёхгранной формы, постепенно переходящей в круглую форму на уровне верхней 1/3 (рис.3Б). Данная конструкция является эффективным антиротационным «замком» (Евразийский патент № 196 от 27.10.1997 г.). Внутрикостная часть этих имплантатов, которая имеет высоту 13, 15, 18 и 24 мм, переходит в «шейку» имплантата и затем в головку. Головка имплантата имеет два варианта ортопедической платформы конической формы — 10 и 20 градусов диаметром 3,8 мм. В верхней части головки снабжены резьбовым каналом для установки фиксирующего зубной протез винта.

Рисунок 3. Образцы разработанных имплантатов: А — имплантат серии Radix-IIS; Б — имплантаты серии Radix-DM; В — имплантаты серии Radix-Combi.
Третьим, входящим в систему, является имплантат, конструкция которого представляет комбинацию цилиндрической и пластиночной форм (торговая марка Radix-Combi). Внутрикостный элемент имеет цилиндрическую часть и отходящую с обеих или одной из сторон «лопасти» (рис.3В). Цилиндр внутрикостного элемента диаметром 4 мм имеет высоту 8, 10 и 12 мм. Толщина «лопастей» составляет 1,4 мм, длина — 4 мм.
Разборные имплантаты Radix-IIS и — Combi имеют однотипный модуль для соединения с компонентами имплантатов. Модуль выполнен в форме конического резьбового канала (Евразийский патент № 2 187 от 17.05.1999 г.). Как показали стендовые технические испытания, проведенные в процессе сертификации, такое соединение обеспечивает надёжное герметичное соединение под воздействием циклических нагрузок. Дополнительными компонентами данных имплантатов являются винт-заглушка и формирователь десневой манжетки, а также ортопедические компоненты: головки, колпачки, фиксирующие протезы винты и зуботехнические компоненты: аналоги головок, выжигаемые колпачки, винты технические. Головки имплантатов снабжены резьбовыми каналами для фиксирующих протез винтов, имеют два варианта конической платформы — 10 и 20 градусов, два варианта её диаметров — 3,8 и 4,5 мм, а также различную высоту чрездесневой части — от 1 до 7 мм. Головки с 10-градусной платформой являются универсальными, рассчитаны как на фиксацию протеза при помощи винтов (условно-съёмное протезирование), так и при помощи цемента (несъёмное протезирование). Головки с 20-градусной платформой рассчитаны только на условно-съёмное протезирование (рис.4).
Все имплантаты и их компоненты изготовлены из титанового сплава марки ВТ1−00, который является одним из наиболее изученных биосовместимых материалов, отвечает стандарту, принятому ИСО/ТК № 5832/11 «Имплантационные материалы для хирургии» и соответствует международному стандарту ASTM F67−89 Grade 4. Все компоненты изготавливаются методом пластического деформирования, что позволяет увеличить усталостную прочность изделий, чистоту обработки поверхностей (не ниже 10-го класса) и точность соединений.
Для препарирования костного ложа имплантатов скомплектован набор инструментов, при разработке которого учитывали биофизические параметры сверления кости и данные, полученные при экспериментальном исследовании.
Кроме инструментов для препарирования костного ложа в комплект инструментов разработанной системы входят инструменты для установки имплантатов и всех их компонентов.
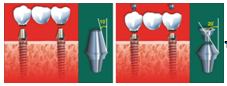
Рисунок 4. Конструкция и назначение головок в системе имплантатов «Radix»: А — универсальная головка с 10-градусной опорной платформой, рассчитанная на фиксацию протезов, как при помощи цемента, так и при помощи винтов; Б — головка с 20-градусной платформой, рассчитанная только на условно-съёмное протезирование.
Клиническая характеристика разработанной системы имплантатов
Конструкции разработанных имплантатов поддерживают все известные на сегодняшний день методики имплантации: двухэтапную стандартную («классическую»), двухэтапную «закрытую» (или «бескровную»), одноэтапную, а также методики имплантации сопровождающиеся реконструкцией костной ткани челюстей.
Конструкция, размеры и конфигурация системы имплантатов разработаны с таким расчётом, чтобы обеспечивать бии межкортикальное расположение внутрикостных элементов, а также при развившемся остеопорозе вовлекать в процесс остеогенеза и структурной перестройки кости максимально возможное количество структурных единиц губчатого слоя кости (рис.5).
Алгоритм клинического применения и выбора разработанных имплантатов можно сформулировать следующим образом:
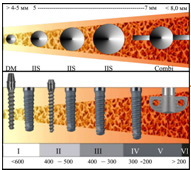
Рисунок 5. Схема алгоритма выбора конструкции и размеров имплантатов в зависимости от объёма кости и типа её архитектоники.
1. В качестве базового для всех пациентов с полным отсутствием зубов, вне зависимости от анатомо-топографических условий (фенотипы А, Б и В) первоначально рассматривается применение имплантатов серии «Radix-IIS».
Размер, диаметр, количество и место их расположения определяется исходя из высоты и межкортикального расстояния костной ткани челюстей. Выбор диаметра имплантата при этом должен совпадать с величиной межкортикального расстояния (рис.5);
- 2. Если толщина альвеолярных отростков составляет 4−5 мм и межкортикальное расстояние — 2−3 мм соответственно, в качестве оптимального выбора имплантатов рассматриваются имплантаты серии «Radix-DM» с соответствующей высотой их внутрикостной части (рис.5).
- 3. Если толщина альвеолярных отростков превышает 7−8 мм и диагностирован региональный остеопороз (в подавляющем большинстве случаев такая картина наблюдается в области жевательной группы зубов) в качестве адекватной конструкции рассматривается применение имплантатов серии «Radix-Combi» (рис.5).
Ортопедические компоненты разработанной системы имплантатов позволяют выполнить условно-съёмное и несъёмное протезирование на имплантатах.
Основная идея протезирования при использовании данной системы имплантатов заключается в унификации ортопедической платформы (рис.6). При использовании имплантатов различных серий, что обусловлено различиями анатомо-топографических условий, ортопедические процедуры и зуботехнические работы производятся при помощи унифицированных компонентов и стандартных процедур, что должно обеспечить оптимальный и упрощённый технологический процесс изготовления зубных протезов. При этом ряд компонентов имеют двойное назначение.
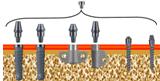
Рисунок 6. Унификация ортопедических компонентов системы Radix.
Так, для «закрытой» методики снятия оттисков могут использоваться фиксирующие винты и пластиковые колпачки. А для «открытой» методики — титановые, пластиковые колпачки и зуботехнические винты. Таким образом, в данной системе имплантатов реализован принцип унификации и совместимости ортопедических компонентов для различных внутрикостных элементов имплантатов, что весьма актуально для протезирования на достаточно большом количестве имплантатов и позволяет стандартизировать работу зуботехнических лабораторий.
Сертификация
На основании проведенных санитарно-химических, токсиколого-гигиенических, функциональных и клинических испытаний разработанных имплантатов и инструментов к ним были выданы сертификаты соответствия и регистрационные удостоверения соответствующими государственными органами здравоохранения России, Белоруссии, Украины, Казахстана, Азербайджана, Таджикистана и Киргизии, разрешающие клиническое применение имплантатов системы «Radix».
Внедрение в клиническую практику разработанной системы имплантатов
На этапе клинического внедрения разработанной новой системы дентальных имплантатов «Radix» и концепции их применения за 10 лет (1997;2007 гг.) было проведено лечение 425 пациентов (302 женщины и 123 мужчины в возрасте от 27 до 75 лет) с полным отсутствием зубов. У 278 из них была полная адентия обеих челюстей, у остальных 147 — одной из челюстей (109 с полной адентией нижней челюсти, 38 — верхней челюсти). Всего было установлено 3685 имплантатов.
Глубина наблюдений за результатами лечения составила от 1 до 10 лет (табл.3).
Раздельно оценивали уровень успеха имплантации и уровень успешного лечения пациентов с различными анатомо-топографическими условиями (фенотипами А, Б и В).
Результаты реабилитации пациентов с фенотипом группы А
Провели лечение и дальнейшие наблюдения за 114 пациентами, у которых были удовлетворительные анатомические условия для имплантации. Вместе с тем, несмотря на наличие анатомических условий, у половины пациентов (57 человек) данной группы имел место выраженный остеопороз в боковых отделах челюстей, при наличии нормальной архитектоники (I-III тип) во фронтальных отделах.
За основу клинической концепции реабилитации данной группы пациентов были приняты следующие положения:
- — установка 6−8 и более имплантатов на каждой из челюстей на основе разработанного алгоритма для применения имплантатов системы «Radix» (рис. 7);
- — условно-съёмное или несъёмное протезирование на имплантатах, подразумевающее создание полноценных по протяжённости зубных рядов;
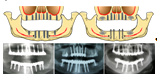
Рисунок 7. Схема и рентгенограммы демонстрирующие расположение имплантатов при различной толщине и типе архитектоники альвеолярных отростков у пациентов группы А.
Количество имплантатов и места их расположения определялись на основании расчётного количества единиц зубного ряда и анатомических особенностей строения верхнечелюстных пазух.
В зависимости от анатомических условий (толщины альвеолярных отростков) и типа архитектоники челюстных костей выбирали не только вариант конструкции имплантатов, но и вариант методики имплантации, а также сроки функциональной нагрузки на имплантаты.
В большинстве случаев, у пациентов с III-IV типом архитектоники (74 человека) применяли классическую двухэтапную методику имплантации с отсроченной функциональной нагрузкой. У пациентов с III типом архитектоники (29 человек) второй этап имплантации и протезирование осуществляли через 2 месяца после установки внутрикостных элементов. У пациентов с IV типом архитектоники второй этап имплантации и протезирование осуществляли через 3−4 месяца после имплантации.
В 12 случаях у пациентов с полной адентией нижней челюсти, имевшим толщину альвеолярных отростков 8 — 10 мм и III-IV тип архитектоники была применена «бескровная» двухэтапная методика имплантации.
В качестве временных протезов часть пациентов (в основном это были пациенты с полной адентией верхней челюсти) пользовались полными съёмными зубными протезами.
Примерно половине пациентов (41 человек) с адентией нижней челюсти устанавливали дополнительно имплантаты для временного протезирования. Установку этих имплантатов производили обязательно бикортикально. В качестве временных протезов в этих случаях изготавливали металлоакриловые конструкции.
У пациентов с I-II типом архитектоники (28 человек) применялась одноэтапная методика имплантации. К протезированию при этом приступали через 10−14 дней после имплантации.
Зубные протезы изготавливали на цельнолитой основе с облицовкой керамикой (40 человек) или с расстановкой стандартных гарнитуров зубов на акриловом базисе (74 человека). В большинстве случаев изготавливали условно-съёмные протезы (89 пациентов), реже — несъёмные конструкции, которые фиксировали на имплантатах при помощи цемента (25 пациентов).
Всего в данной группе было установлено 1984 имплантата. В послеоперационном периоде в результате различных осложнений (периимплантита, отсутствия интеграции, остеита) было удалено 35 имплантатов, 28 из них были удалены по причине отсутствия интеграции в зонах, где имел место остеопороз. В 27 случаях удаления имплантатов была произведена реимплантация, которая в 24 случаях была успешной. После протезирования было удалено 10 имплантатов вследствие их дезинтеграции и периимплантита. В 5 случаях было проведено повторное лечение — реимплантация и повторное протезирование. В остальных случаях, когда было установлено по 8 и более имплантатов, и количество оставшихся имплантатов было достаточно для выполнения функции опоры зубных протезов, дополнительного лечения (имплантации) не производилось.
Таким образом, уровень успеха имплантации в данной группе пациентов составил 97,7−98,9%. Уровень успеха реабилитации пациентов составил 99,1% (только у одного пациента из-за неудачной имплантации был полностью изменён план лечения, и оставшиеся 2 имплантата были использованы для дополнительной фиксации съёмного протеза).
Результаты реабилитации пациентов с фенотипом группы Б
Лечение и дальнейшие наблюдения осуществляли за 255 пациентами, у которых были удовлетворительные анатомические условия для имплантации только во фронтальном отделе челюстей. У 129 пациентов данной группы имел место остеопороз не только в боковых, но и во фронтальных отделах челюстей. У второй половины пациентов при наличии остеопороза в боковых отделах, во фронтальных отделах регистрировали I-III тип архитектоники.
За основу клинической концепции реабилитации данной группы пациентов были приняты следующие положения:
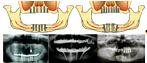
Рисунок 8. Схема и рентгенограммы демонстрирующие расположение имплантатов при различной толщине и типе архитектоники альвеолярных отростков у пациентов группы Б.
- — установка 4−6 имплантатов (только серий Radix-IIS иDM, высотой внутрикостного элемента 12−18 мм) во фронтальном отделе нижней и 6−8 аналогичных имплантатов во фронтальном отделе верхней челюстей.
- — условно-съёмное протезирование с дистальным вытяжением по первые моляры (консольной конструкцией) на имплантатах (рис.8).
Выбор конструкции имплантатов в данной группе зависел от толщины альвеолярного отростка, а в зависимости от типа архитектоники выбирали методику их применения и сроки функциональной нагрузки.
У пациентов с III-V типом архитектоники (204 пациента) применяли двухэтапную методику имплантации с отсроченной функциональной нагрузкой. Внутрикостные элементы имплантатов при этом устанавливали только бикортикально. У пациентов с I-II типом архитектоники применяли одноэтапную методику имплантации. В случаях, когда на верхней челюсти также была полная адентия и осуществлялось протезирование с изготовлением полных съёмных зубных протезов, — применяли раннюю функциональную нагрузку на имплантаты, т. е. проводили протезирование через 10−14 дней после имплантации.
Условно-съёмные зубные протезы изготавливали по принятой для данной конструкции расчётной схеме, на цельнолитой металлической основе с расстановкой стандартных гарнитуров зубов в акриловом базисе.
Всего в данной группе было установлено 1320 имплантатов. В послеоперационном периоде в результате различных осложнений (периимплантита, отсутствия интеграции, остеита) был удалён 21 имплантат, 18 из них были удалены по причине отсутствия интеграции. В 5 случаях удаления имплантатов была произведена реимплантация, которая в 4 случаях была успешной. После протезирования было удалено 2 имплантата вследствие их дезинтеграции и периимплантита. В этих случаях было проведено повторное протезирование на меньшем количестве имплантатов. Таким образом, уровень успеха имплантации в данной группе пациентов составил 98,4−98,7%. Уровень успеха реабилитации пациентов составил 98,8% (у трёх пациентов из-за неудач имплантации был изменён план лечения, и оставшиеся имплантаты были использованы для дополнительной фиксации съёмных протезов).
Результаты реабилитации пациентов с фенотипом группы В
Лечение и дальнейшие наблюдения осуществляли за 56 пациентами, у которых были неудовлетворительные анатомические условия для имплантации во всех отделах челюстей. Кроме того, у 31 пациента имел место остеопороз не только в боковых, но и во фронтальных отделах челюстей. У остальных 25 пациентов при наличии остеопороза в боковых отделах, во фронтальных отделах челюстей регистрировали I-III тип архитектоники. У 6 пациентов данной группы была первичная полная адентия вследствие гипогидротической эктодермальной дисплазии.
За основу клинической концепции реабилитации данной группы пациентов были приняты 2 подхода.
1. Тотальная реконструкция утраченного вследствие атрофии объёма костной ткани челюстей или проведение реконструкции в субантральной зоне (при полной адентии верхней челюсти) и установкой 8 и более имплантатов с последующим условно-съёмным или несъёмным протезированием на имплантатах, подразумевающее создание полноценных по протяжённости зубных рядов (рис. 9А). По сути, данный подход подразумевает создание условий для реализации клинической концепции применённой в группе А.
Данный подход был реализован у 24 пациентов трудоспособного возраста, в случаях, когда зубы отсутствовали только на одной из челюстей, при этом антагонирующий зубной ряд был восстановлен при помощи несъёмного протезирования.
У 3 пациентов была произведена тотальная реконструкция альвеолярных отростков верхней челюсти при помощи монокортикальных костных аутотрансплантатов. Производилась реконструкция как фронтальных, так и боковых отделов.
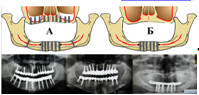
Рисунок 9. Схема и рентгенограммы демонстрирующие расположение имплантатов при различной толщине и типе архитектоники альвеолярных отростков у пациентов группы В.
У 21 пациента, у которых высота остаточного объёма верхней челюсти во фронтальных отделах составляла 8 — 10 мм, а в боковых отделах дефицит костной ткани был обусловлен как атрофией костной ткани, так и значительным объёмом верхнечелюстных пазух (пневматический и смешанный тип их строения), производили наращивание высоты боковых отделов при помощи субантральной аугментации («синус-лифтинга»). При этом имплантацию производили как в передних отделах, устанавливая минимальные по высоте имплантаты (Radix-IIS с высотой внутрикостных элементов 8 или 10 мм), так и в зоне произведенного «синус-лифтинга». Всего по альвеолярной дуге устанавливали 8 — 10 имплантатов.
В большинстве случаев (15 пациентов) операцию «синус-лифтинг» производили с применением монокортикальных костных аутотрансплантатов из различных донорских мест (симфиза, тела, ретромолярной зоны нижней челюсти, бугристости большеберцовой кости) с одномоментной имплантацией. В качестве вспомогательных для реконструкции материалов использовали обогащённую тромбоцитами плазму крови пациента и остеокондуктивные материалы.
У 6 пациентов, когда сохранялась возможность для удовлетворительной первичной фиксации внутрикостных элементов, операцию «синус-лифтинг» производили без аутотрансплантации кости, с использованием только остеокондуктивных материалов и обогащённой тромбоцитами плазмы крови.
Эффективность данного подхода определяется не только уровнем успеха имплантации, но и результатами необходимых реконструктивных операций по наращиванию объёма челюстей для создания условий к имплантации.
У пациентов, которым проводили тотальную реконструкцию верхней челюсти, уровень успеха имплантации составил 92,8% (3 из 28 имплантатов были удалены из-за отсутствия интеграции). Однако, удаление этих имплантатов не привело к пересмотру изначально выбранной концепции лечения и протезирование в полном объёме было реализовано на оставшихся имплантатах.
У пациентов, которым производили субантральную аугментацию, уровень успеха имплантации составил 95,7%. Из 189 установленных имплантатов, 8 были удалены из-за отсутствия интеграции и воспалительных осложнений. 2 из них были удалены у пациента через 3 года после протезирования (один имплантат мигрировал в верхнечелюстную пазуху, второй — стал подвижен из-за неадекватной нагрузки). Было произведено удаление имплантатов, реимплантация и повторное протезирование.
2. Второй подход заключался в бикортикальной установке 4−6 имплантатов (только серий Radix-IIS иDM, высотой внутрикостного элемента 8−12 мм) во фронтальном отделе нижней и 6−8 аналогичных имплантатов во фронтальном отделе верхней челюстей с последующим условно-съёмным протезированием с дистальным вытяжением (рис.4Б).
В качестве исходных условий для реализации этого подхода рассматривали случаи полной адентии обеих челюстей, когда для верхней челюсти изготавливались полные съёмные зубные протезы.
Всего при данном подходе было установлено 164 имплантата. В послеоперационном периоде в результате различных осложнений (периимплантита, отсутствия интеграции, остеита) было удалено 2 имплантата. В 1 случае была произведена успешная реимплантация. После протезирования были удалены ещё 2 имплантата вследствие их дезинтеграции и периимплантита. У этих двух пациентов было проведено съёмное протезирование с использованием оставшихся имплантатов. Таким образом, уровень успеха имплантации в данной группе составил 97,5 — 98,1%. Уровень успеха реабилитации пациентов этой группы составил 98,7%.
Обобщение и анализ результатов клинических наблюдений В период с 1997 по 2002 гг. было установлено 1742 имплантата. Из них 24 были удалены. Таким образом, 98,6% установленных имплантатов продолжают успешно выполнять функцию опоры зубных протезов 5 и более лет.
Анализ рентгенологических обследований показал, что в зоне 1651 (94,7%) функционирующих более 5 лет имплантатов, достоверных признаков снижения высоты кости, более чем на 0,5−1 мм, а также горизонтальной и вертикальной резорбции выявлено не было. В области 70 имплантатов (4,0%) имела место вертикальная резорбция с образованием костных карманов глубиной около 1−1,5 мм. В зоне 21 имплантата (1,3%) наблюдали горизонтальную резорбцию костной ткани более 1 мм.
Анализ применения однои двухэтапной методик имплантации, подразумевающих соответственно раннюю и отсроченную функциональную нагрузку на имплантаты, показал, что одноэтапная методика более эффективна (табл. 2 и 3). Однако, следует учесть, что одноэтапную методику и раннюю функциональную нагрузку применяли только в случаях, когда имел место нормальный тип архитектоники и была реальная возможность для установки имплантатов не только бикортикально, но и панкортикально. Кроме того, данную методику не применяли в группе пациентов со значительной атрофией костной ткани (группа В). Калькуляция результатов имплантации при различных типах архитектоники челюстных костей показала, что при остеопорозе (IV-VI тип) эффективность имплантации меньше на 1−3%, чем в случаях нормального типа архитектоники (табл. 4). Вместе с тем, результаты имплантации у пациентов с регионарным остеопорозом челюстных костей в настоящем исследовании на уровне 95−97% показывают, что предлагаемый алгоритм выбора конструкции разработанных имплантатов и методик их применения явились достаточно эффективными. Для сравнения, описываемый в литературе уровень успеха применения стандартных методик имплантации в аналогичных анатомо-топографических ситуациях составляет 66−92%.
Таблица 2. Результаты лечения пациентов в группах исследования
Фенотип. | челюсть. | методика. | |||
нижняя. | верхняя. | двухэтапная. | одноэтапная. | ||
Группа А. | 99,6%. | 98,1%. | 97,9%. | 99,7%. | |
Группа Б. | 99,7%. | 98,5%. | 98,6%. | 99,7%. | |
Группа В. | 99,3%. | 98,1%. | 97,5%. | не применялась. | |
Как показали клинические наблюдения применения новой системы имплантатов и алгоритма их применения, эффективность реабилитации пациентов с полным отсутствием зубов составила 99 — 100% (табл.2). Не удалось достичь искомого результата у 6 пациентов, которым вместо условно-съёмного протезирования, из-за удаления части имплантатов, пришлось изготавливать полные съёмные зубные протезы. Таким образом, общий уровень успеха лечения пациентов составил 98,5%.
Таблица 3. Результаты имплантации при различных типах архитектоники костной ткани челюстей
Архитектоника. | челюсть. | методика. | |||
нижняя. | верхняя. | двухэтапная. | одноэтапная. | ||
Тип I-II. | 98,5%. | 99,1%. | 97,8%. | 99,8%. | |
Тип III. | 99,4%. | 99,3%. | 98,6%. | 99,1%. | |
Тип IV. | 97,8%. | 93,1%. | 97,6%. | не применялась. | |
Тип V-VI. | 95,4%. | ; | 95,4%. | не применялась. |
4. Результаты имплантации в группах исследования
Фенотип. | Эффективность лечения. | ||
двухэтапная методика. (отсроченная нагрузка на имплантаты). | одноэтапная методика. (ранняя функциональная нагрузка). | ||
Группа А. | 99,1%. | 100%. | |
Группа Б. | 98,8%. | 100%. | |
Группа В. | 98,7%. | не применялась. | |
Обобщение и анализ клинических результатов показали высокую эффективность разработанной системы дентальных имплантатов и алгоритма их применения у пациентов с полным отсутствием зубов.
Выводы
- 1. Реабилитация пациентов с полным отсутствием зубов — актуальная междисциплинарная проблема стоматологии, задачами которой являются: восстановление функции жевания и речи, профилактика атрофии и остеопороза челюстей, максимальное сокращение сроков функциональной адаптации больных к зубным протезам и создание условий для эффективной социальной адаптации больных.
- 2. С точки зрения эффективности восстановления утраченных функций, профилактики атрофии и остеопороза челюстей, а также социальной адаптации, метод имплантации может рассматриваться как один из наиболее приемлемых способов реабилитации больных полной адентией. Этот метод может расцениваться как патогенетическое лечение данной патологии.
- 3. В основе биосовместимости внутрикостных имплантатов лежит биологическое свойство заживления кости первичным и вторичным натяжением (контактный и дистантный остеогенез), а также способность костной ткани к модификации собственной архитектоники в результате структурной перестройки.
- 4. Достижение интеграции имплантатов возможно при сохранении способности костной ткани воспринимающего ложа имплантата к остеоиндукции и остеокондукции, обеспечении остеокондуктивных свойств поверхности имплантатов и своевременном включении имплантата в функциональную нагрузку.
- 5. Степень термического и механического повреждения кости во время препарирования ложа определяет способность костной ткани воспринимающего ложа к остеоиндукции и остеокондукции и достижению интеграции дентальных имплантатов.
- 6. Препарирование костного ложа с использованием шаровидных и фиссурных фрез со скоростью вращения от 1000 до 7000 об/мин, а также сверлом при 3000 — 7000 об/мин приводит к нагреванию кости, превышающему допустимый уровень, что нарушает процесс регенерации костной ткани, приводит к образованию мягкотканой капсулы вокруг имплантатов и может приводить к секвестрации фрагментов кости вместе с имплантатами.
- 7. Препарирование костного ложа сверлом с помощью ручной дрели (скорость вращения 15−30 об/мин) приводит к грубому механическому повреждению костной ткани воспринимающего ложа и замедляет процесс регенерации кости вокруг имплантатов.
- 8. Препарирование ложа имплантатов сверлом (угол заточки — менее 45є, угол отводящей канавки — более 120є) со скоростью вращения 1000 об/мин не вызывает чрезмерного нагревания кости, позволяет существенно сократить время препарирования при минимальном давлении на инструмент, что создаёт оптимальные условия для регенерации костной ткани и контактного остеогенеза на поверхности имплантатов.
- 9. Остеогенез в зоне интерфейса имплантат/костная ткань имеет существенные различия на уровне компактного и губчатого слоёв кости.
- 10. Отсутствие резорбции большинства остеонов при сохранении их неизменённой структуры через 14, 30 дней и 2 месяца после установки имплантатов свидетельствует о достижении контактного сотеогенеза и интеграции имплантатов на уровне компактного слоя в срок около 14 дней.
- 11. На уровне губчатого слоя кости регенерация костной ткани в прилегающих к поверхности имплантата зонах происходит преимущественно по типу дистантного остеогенеза, о чём свидетельствует образование грубоволокнистой костной ткани через 1−2 месяца после установки имплантатов.
- 12. Гистоморфометрический анализ показал, что интерфейс функционировавших in-vivo имплантатов был представлен на уровне компактного слоя костной интеграцией на 82% их площади, фиброзно-костной интеграцией в среднем на 14% площади и контактом с фиброзной тканью на 4% площади. На уровне губчатого слоя кости морфология интерфейса этих имплантатов выглядела иначе. Костная интеграция составила 47% площади, фиброзно-костная — 32%, контакт с мягкими тканями был зарегистрирован на 21% площади сопряжения поверхности имплантата с окружающими тканями.
- 13. Регионарный остеопороз костной ткани челюстей является следствием утраты зубов. Развивается, как правило, в боковых отделах челюстей примерно у 33 — 50% больных, страдающих адентией более двух лет, пользовавшихся съёмными зубными протезами, имеющих выраженную атрофию альвеолярных отростков при сохранении значительной их толщины (более 8 мм) и имеющих брахицефалический тип строения лицевого отдела скелета.
- 14. У большинства пациентов (73%) с полным отсутствием зубов отсутствуют анатомические условия для проведения имплантации в боковых отделах челюстей, т.к. расстояние от гребня альвеолярного отростка до нижнечелюстного канала или дна верхнечелюстной пазухи составляет менее 10 мм. Только у 27% таких пациентов высота кости в боковых отделах челюстей составляет более 10 -12 мм.
- 15. У большинства пациентов (80%) с полным отсутствием зубов вне зависимости от выраженности атрофии и высоты кости толщина альвеолярных отростков составляет более 7 мм, у 17% - от 4 до 6 мм, и только у 3% пациентов толщина альвеолярных отростков составляла менее 4 мм.
- 16. Межкортикальное расстояние (или толщина губчатого слоя) альвеолярных отростков у пациентов с толщиной челюстных костей более 7 мм составляет от 3 до 7 мм, у пациентов с толщиной альвеолярных отростков менее 7 мм, межкортикальное расстояние составляет от 0 до 4 мм.
- 17. При компьютерной томографии и рентгеноденситометрии выявлены 6 визуально различимых и верифицированных по шкале Хаунсфилда вариантов архитектоники костной ткани челюстей, из которых I-III типы (от 300 до 1000 HU) являются нормальными вариантами архитектоники для проведения имплантации, в то время, как IV-VI типы (менее 300HU) представляют собой разной степени выраженности регионарный остеопороз и могут расцениваться как неблагоприятные условия для проведения стандартных методик имплантации.
- 18. На основании проведенных экспериментальных и предварительных клинических исследований разработана система дентальных имплантатов (торговая марка «Радикс»). Систему составляют 3 типа внутрикостных элементов винтовой и комбинированной форм, унифицированные инструменты для атравматичного препарирования костного ложа имплантатов и совместимые со всеми типами внутрикостных элементов ортопедические компоненты.
- 19. Конструкция, размеры и конфигурация имплантатов, составляющих разработанную систему, обеспечивают бии межкортикальное расположение внутрикостных элементов, что позволяет обеспечить условия для контактного сотеогенеза, а также оптимизировать условия для интеграции имплантатов при регионарном остеопорозе челюстей.
- 20. Разработанный алгоритм выбора имплантатов системы «Радикс» и методик их применения, учитывающий анатомо-топографические условия для имплантации, позволяет обеспечить достаточно высокий уровень успеха имплантации, как при удовлетворительных анатомо-топографических условиях (97,8−99,85), так и при регионарном остеопорозе (93,1−97,8%) и обеспечить у 98,5% пациентов с полным отсутствием зубов эффективную функциональную и социальную реабилитацию в течение 5 и более лет.
Практические рекомендации
- 1. Для клинического применения разработанных дентальных имплантатов системы «Радикс» у пациентов с полным отсутствием зубов необходимо использовать следующий алгоритм выбора типа имплантата:
- 1)в качестве базового для всех пациентов с полным отсутствием зубов, вне зависимости от анатомо-топографических условий (фенотипы А, Б и В) первоначально рассматривается применение имплантатов серии «Radix-IIS». Размер, диаметр, количество и место их расположения определяется исходя из высоты и межкортикального расстояния костной ткани челюстей. Выбор диаметра имплантата при этом должен совпадать с величиной межкортикального расстояния;
- 2)если толщина альвеолярных отростков составляет 4−5 мм и межкортикальное расстояние — 2−3 мм соответственно, в качестве оптимального выбора рассматриваются имплантаты серии «Radix-DM» с соответствующей высотой их внутрикостной части;
- 3)если толщина альвеолярных отростков превышает 7−8 мм и диагностирован региональный остеопороз (в подавляющем большинстве случаев такая картина наблюдается в области жевательной группы зубов) в качестве адекватной конструкции рассматривается применение имплантатов серии «Radix-Combi».
- 2. Для реабилитации пациентов с удовлетворительными для имплантации анатомическими условиями (фенотип А) рекомендуется следующая схема лечения:
- — установка 6−8 и более имплантатов на каждой из челюстей на основе разработанного алгоритма;
- — условно-съёмное или несъёмное протезирование на имплантатах, подразумевающее создание полноценных по протяжённости зубных рядов.
У пациентов с I-II типом архитектоники, а также с III типом архитектоники, если имплантаты установлены биили межкортикально, целесообразно применять одноэтапную методику имплантации и раннюю функциональную нагрузку на имплантаты. К протезированию при этом можно приступать через 7−10 дней после имплантации. При стандартной установке имплантатов у пациентов с III типом архитектоники целесообразно проведение двухэтапной методики имплантации с отсроченной функциональной нагрузкой на имплантаты и протезированием через 2 месяца после имплантации.
У пациентов с IV-VI типами архитектоники необходимо применять двухэтапную методику имплантации и приступать к протезированию через 2−3 месяца после имплантации.
- 3. Для реабилитации пациентов с удовлетворительными для имплантации анатомическими условиями только во фронтальном отделе и отсутствием таковых в боковых отделах челюстей (фенотип Б) рекомендуется следующая схема лечения:
- — установка 4−6 имплантатов (только серий Radix-IIS иDM, высотой внутрикостного элемента 12−18 мм) во фронтальном отделе нижней и 6−8 аналогичных имплантатов во фронтальном отделе верхней челюстей;
- — условно-съёмное протезирование с дистальным вытяжением по первые моляры (консольной конструкцией) на имплантатах по принятой для данной конструкции расчётной схеме, на цельнолитой металлической основе с расстановкой стандартных гарнитуров зубов в акриловом базисе.
У пациентов с I-II типом архитектоники может применяться одноэтапная методика имплантации с протезированием через 7−10 дней после имплантации.
У пациентов с III-VI типом архитектоники следует применять двухэтапную методику имплантации с отсроченной функциональной нагрузкой и протезированием через 2−3месяца после имплантации.
- 4. Для реабилитации пациентов со значительной атрофией костной ткани челюстей (фенотип В) могут применяться 2 подхода:
- 1) тотальная реконструкция утраченного вследствие атрофии объёма костной ткани челюстей или проведение реконструкции в субантральной зоне (при полной адентии верхней челюсти) и установка 8 и более имплантатов с последующим условно-съёмным или несъёмным протезированием на имплантатах, подразумевающее создание полноценных по протяжённости зубных рядов. По сути, данный подход подразумевает создание условий для реализации клинической концепции применяемой у пациентов фенотипа А.
- 2) бикортикальная установка 4−6 имплантатов (только серий Radix-IIS иDM, высотой внутрикостного элемента 8−12 мм) во фронтальном отделе нижней и 6−8 аналогичных имплантатов во фронтальном отделе верхней челюстей с последующим условно-съёмным протезированием с дистальным вытяжением.
В качестве исходных условий для реализации этого подхода рассматриваются случаи полной адентии обеих челюстей, когда имплантация проводится на обеих челюстях или в качестве антагониста будет изготавливаться полный съёмный зубной протез.
5. Данные рекомендации и алгоритм выбора конструкций и размеров имплантатов, а также методик их применения могут использоваться при использовании любых других систем дентальных имплантатов, конструкции которых позволяют выполнять условно-съёмное протезирование.
Список опубликованных работ по теме диссертации.
- 1. Дудко А. С., Параскевич В. Л., Максименко Л. Л. Влияние структуры поверхности цилиндрических зубных имплантатов на прочность их интеграции в костной ткани // Здравоохранение Белоруссии, 1992, № 10, стр. 19−21.
- 2. Параскевич В. Л. Эндоссальная имплантация при атрофии альвеолярного отростка верхней челюсти // Новое в стоматологии, 1992, № 3, стр. 21−23.
- 3. Параскевич В. Л. Возможности реконструктивной хирургии и имплантации для реабилитации больных с полной адентией. Материалы международного семинара «Новые методики и технологии в стоматологии», 1996, Львов, стр.7−8.
- 4. Параскевич В. Л. Основные направления реконструктивной хирургии полости рта при полной адентии // Материалы I международной конференции «Актуальные вопросы стоматологической имплантации», Минск, 1996, стр. 6−21.
- 5. Параскевич В. Л., Смирнов С. А., Максименко Л. Л. Медицинская и технологическая концепция системы дентальных имплантатов «Radix» // Материалы I международной конференции «Актуальные вопросы стоматологической имплантации», Минск, 1996, стр. 75−81.
- 6. Paraskevich V. The Radix Implant System — conception, hardware, clinical use. (Система имплантатов «Radix»: концепция, инструментальное обеспечение, клиническое применение), New Delhi, Appolo Publ. Gr., 1997. 55 p.
- 7. Параскевич В. Л. Анализ основных клинических концепций дентальной имплантации // Клиническая имплантология и стоматология. 1997, № 1, стр.60−64.
- 8. Параскевич В. Л. Сравнительная оценка двух типов внутрикостных имплантатов для восстановления концевых дефектов зубных рядов верхней челюсти // Новое в стоматологии. 1997, № 4 стр. 28−30.
- 9. Параскевич В. Л. Основные концепции дентальной имплантации и возможности их применения в Беларуси // Материалы 3-го съезда стоматологов Белоруссии, 1997, стр.229−231.
- 10. Параскевич В. Л. Усовершенствованный метод вестибулопластики // Новое в стоматологии, 1997, № 9, стр.39−42.
- 11. Максименко Л. Л., Параскевич В. Л Внутрикостный челюстной имплантат. Евразийский патент № 196 от 27.10.1997 г.
- 12. Параскевич В. Л. Методика выбора типа и размеров внутрикостных имплантатов при планировании лечения // Новое в стоматологии, 1998,№ 3, стр.45−52.
- 13. Параскевич В. Л. Возможности применения внутрикостной имплантации при значительной атрофии челюстей // Материалы I международной конференции «Актуальные вопросы стоматологической имплантации», Минск, 1998, стр. 15−23.
- 14. Параскевич В. Л., Следков М. С. Клинико-лабораторные этапы изготовления условно-съёмных протезов на имплантатах // Материалы II международной конференции «Актуальные вопросы стоматологической имплантации», Минск, 1998, стр. 35−39.
- 15. Параскевич В. Л., Максименко Л. Л. Винтовые внутрикостные имплантаты с антиротационной защитой // Материалы II международной конференции «Актуальные вопросы стоматологической имплантации», Минск, 1998, стр. 79−81.
- 16. Параскевич В. Л. Модифицированный метод вестибулопластики по EdlanMejchar // Новини стоматологii (Украина), 1999, № 1, стр.18−19.
- 17. Параскевич В. Л. Эндопротезирование в комплексной реабилитации больных полной адентией // Материалы научно-практической конференции «Янтарный край России — стоматология — XXI век». Калининград, 1999, стр.33−34.
- 18. Параскевич В. Л. Современные проблемы реабилитации больных полной адентией. Часть I: Сравнительный анализ методов лечения // Проблемы стоматологии и нейростоматологии. 1999, № 3, стр. 42−46.
- 19. Параскевич В. Л. Современные проблемы реабилитации больных полной адентией. Часть II: Клинические концепции дентальной имплантации // Проблемы стоматологии и нейростоматологии, 1999, № 4, стр. 36−40.
- 20. Веранчик Е. А., Максименко Л. Л., Параскевич В. Л. Внутрикостный зубной имплантат. Евразийский патент № 2 187 от 17.05.1999 г.
- 21. Параскевич В. Л. Диагностика регионарного остеопороза челюстей при планировании имплантации // Российский стоматологический журнал, 2000, № 2, стр.33−36.
- 22. Параскевич В. Л., Дудко А. С., Швед И. А. Динамика биосовместимости внутрикостных имплантатов.// Новое в стоматологии, 2000, № 8, стр. 16−24.
- 23. Параскевич В. Л., Максименко Л. Л. Одноэтапные винтовые имплантаты. Преимущества и недостатки // Новое в стоматологии, 2000, № 8. стр. 38−45.
- 24. Параскевич В. Л. Усовершенствованный хирургический подход для внутрикостной имплантации при значительной атрофии нижней челюсти.// Новое в стоматологии, 2000, № 8, стр.60−67.
- 25. Параскевич В. Л. Дентальная имплантация.
Введение
в специальность // Стоматологический журнал (Беларусь), 2000. № 1(октябрь), стр.8−21.
- 26. Параскевич В. Л. Усовершенствованный хирургический подход для внутрикостной имплантации в области сильно атрофированных боковых отделов нижней челюсти// Современная стоматология (Беларусь), 2000, № 2, стр. 58−64.
- 27. Параскевич В. Л. Бикортикальная установка имплантатов // Клиническая имплантология и стоматология, 2000, № 3−4, стр. 58−60.
- 28. Параскевич В. Л. Использование монокортикальных аутотрансплантатов для наращивания высоты костной ткани в области дна верхнечелюстной пазухи // Институт стоматологии, 2001, № 3, стр. 35−40.
- 29. Параскевич В. Л. Остеоиндуктивные и остеокондуктивные материалы в стоматологической практике // Современная стоматология (Беларусь), 2001, № 3, стр. 7−12.
- 30. Параскевич В. Л. Дентальная имплантология. Основы теории и практики (научно-практическое издание). Минск, Юнипресс, 2002, 368 с.
- 31. Параскевич В. Л. Конструкция «Toronto bridge» в комплексной реабилитации больных с полной адентией нижней челюсти // Стоматологический журнал (Беларусь), 2002, № 1, стр. 27−29.
- 32. Параскевич В. Л. Использование аутотрансплантатов из симфиза нижней челюсти при операции синус-лифт // Современная стоматология (Беларусь), 2002, № 1, стр. 22−26.
- 33. Параскевич В. Л., Булат А. В. «Бескровные» методики имплантации // Стоматологический журнал (Беларусь), 2002, № 1, стр. 30−32.
- 34. Параскевич В. Л. Использование костных аутотрансплантатов при операции синус-лифт // Материалы первой Восточноевропейской конференции по проблемам стоматологической имплантации. Львов, 15−16 марта 2002, стр. 40−41.
- 35. Параскевич В. Л. Методика использования монокортикальных костных аутотрансплантатов при операции синус-лифт // Новини стоматологii (Украина), 2002, № 2, стр. 4−9.
- 36. Параскевич В. Л. Протезирование на имплантатах. Сообщение 1: Базовые конструкции зубных протезов // Современная стоматология (Беларусь), 2002, № 2, стр. 8−10.
- 37. Параскевич В. Л. Протезирование на имплантатах. Сообщение 2: Клинико-лабораторные этапы изготовления несъёмных протезов // Современная стоматология (Беларусь), 2002, № 3, стр. 37−40.
- 38. Параскевич В. Л. Протезирование на имплантатах. Сообщение 3: Клинико-лабораторные этапы изготовления условно-съёмных зубных протезов // Современная стоматология (Беларусь), 2002, № 4, стр.9−15.
- 39. Параскевич В. Л. Протезирование на имплантатах. Сообщение 4: Клинико-лабораторные этапы изготовления комбинированных зубных протезов // Современная стоматология (Беларусь), 2002, № 5, стр.9−15.
- 40. Параскевич В. Л., Артюшкевич А. С., Яцкевич О. С. Методика применения монокортикальных костных аутотрансплантатов из гребешка подвздошной кости для тотальной реконструкции атрофированной верхней челюсти // Стоматологический журнал (Беларусь), 2005, № 1, стр. 56−60
- 41. Параскевич В. Л. Использование монокортикальных костных блоков из бугра верхней челюсти при операции синус-лифтинг // Институт стоматологии, 2005, № 1, стр.32−33
- 42. Параскевич В. Л., Иванов С. Ю. Полная адентия. Проблемы реабилитации // Стоматологический журнал, 2005 (Беларусь), № 2, стр.9−15
- 43. Галиновская Т. В., Параскевич В. Л. Окклюзионная реабилитация больных с гипогидротической эктодермальной дисплазией // Стоматологический журнал (Беларусь), 2005, № 3, стр.50−53.
- 44. Параскевич В. Л., Артюшкевич А. С., Яцкевич О. С. Методика тотальной реконструкции альвеолярного отростка верхней челюсти // Институт стоматологии, 2005, № 2, стр.18−21.
- 45. Параскевич В. Л. Дентальная имплантология. 2-е издание. Москва, Медицинское информационное агентство (научно-практическое издание), 2006, 399 с.
- 46. Параскевич В. Л. Условно-съёмные протезы с дистальным вытяжением в комплексной реабилитации больных с полной адентией и значительной атрофией нижней челюсти // Проблемы стоматологии (Казахстан), 2006, № 1, стр. 48−49.
- 47. Параскевич В. Л. Немедленная имплантация в лунки удалённых зубов (обобщение 10-летнего клинического опыта 2325 имплантаций) // Стоматологический журнал (Беларусь), 2006, № 2, стр. 108−119.
- 48. Параскевич В. Л., Иванов С. Ю. Модифицированная методика синус-лифтинга // Стоматологический журнал, 2006 (Беларусь), № 4, стр. 251−253.
- 49. Опанасюк И. В., Параскевич В. Л., Каленчук В. В., Сюма А. З. Синус-лифтинг // Стоматологический журнал (Беларусь), 2007, № 1, стр. 44−55
- 50. Параскевич В. Л. Негайна iмплантацiя у лунки видалених зубiв (Немедленная имплантация в лунки удалённых зубов) // Iмплантологiя. Пародонтологiя. Остеологiя (Украина), 2007, № 2, стр. 28−42
- 51. Параскевич В. Л., Иванов С. Ю. Методика синус-лифтинга с использованием современных технологий // Институт стоматологии, 2007, № 1, стр. 30