Коррозия металлов и защита от коррозии

Пример 5. Определите возможность электрохимической коррозии с водородной деполяризацией гальванической пары СuZn, погруженной в 0.01М раствор ZnSO4 при 25 oC. Как изменится ЭДС коррозионного элемента в результате концентрационной поляризации анода, если концентрация раствора возросла до 0.05 моль/л? Задача 3. Железо покрыто хромом. Какой из металлов будет корродировать в случае нарушения… Читать ещё >
Коррозия металлов и защита от коррозии (реферат, курсовая, диплом, контрольная)
Коррозия — это разрушение металла в результате его физикохимического взаимодействия с окружающей средой. По механизму протекания коррозионного процесса различают химическую и электрохимическую коррозию.
Химическая коррозия представляет собой самопроизвольное разрушение металлов в среде окислительного газа (например, кислорода, галогенов) при повышенных температурах или в жидких неэлектролитах.
Уравнение реакции окисления металлов кислородом (пример газовой коррозии) можно записать в общем виде:
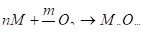
.
Электрохимическая коррозия протекает при контакте металла с растворами электролитов. Например, наиболее распространённая атмосферная коррозия протекает в тонких плёнках электролитов, которые возникают на поверхности металла в результате адсорбции, конденсации или прямого попадания воды и растворения в ней коррозионноактивных газов и солей (O2, SO2, CO2, NO2, NaCl и др.). Учитывая, что поверхность металла всегда энергетически неоднородна (изза наличия примесей в металле, различий по химическому и фазовому составу сплава и др.), на участках металла, имеющих более отрицательное значение потенциала, пойдёт процесс окисления этого металла. Таким образом, при электрохимической коррозии разрушение металла происходит в результате работы огромного количества коррозионных микроэлементов. При этом на корродирующем металле протекает анодная реакция:
АНОД M > Mn+ + ne,.
а на участках металла с более положительным потенциалом — катодное восстановление окислителя (Ox):
КАТОД Ox + ne > Red.
Наиболее распространёнными окислителями при электрохимической коррозии являются молекулы кислорода О2, воздуха и ионы водорода Н+ электролита.
Коррозия с участием кислорода называется коррозией с поглощением кислорода (с кислородной деполяризацией). В зависимости от рН среды возможны два механизма ионизации (восстановления) кислорода:
в щелочной или нейтральной среде.
O2 + 2H2O + 4e > 4OH (pH?7),.
в кислой среде.
O2 + 4H+ + 4e > 2H2O (pH<7).
При коррозии с выделением водорода (с водородной деполяризацией) реакции выделения водорода имеют вид:
в щелочной или нейтральной среде.
2H2O + 2e > H2 + 2OH (pH?7),.
в кислой среде.
2H+ + 2e > H2 (pH<7).
Если в качестве окислителя одновременно выступают О2 и Н+, то такая коррозия называется коррозией со смешанной деполяризацией.
Возможность протекания электрохимической коррозии может быть определена по знаку ЭДС элемента: если ЭДС элемента имеет положительное значение, то коррозия возможна. Так как ЭДС равна разности потенциалов окислителя и восстановителя Еэ=ЕокЕвосст или разности потенциалов катода и анода Еэ=ЕкЕа, то коррозия возможна при условии, что потенциал окислителя (или катода) положительнее потенциала металла:
Еок > E (Mn+/M) или Ек > E (Mn+/M).
Равновесный потенциал кислородного электрода при 298 К описывается уравнением:
E (О2/ОН) = 1.227 0.059?pH + 0.0147?lg p (О2),.
а потенциал водородного электрода уравнением:
E (H+/H2) = 0.0295?lg p (H2) 0.059?pH.
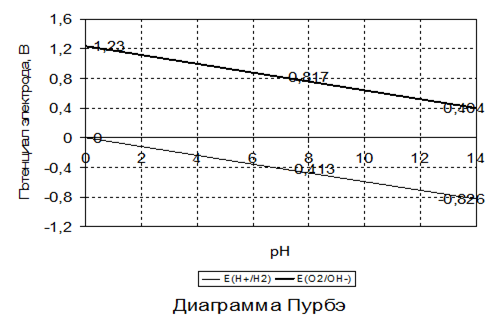
Для оценки возможности или невозможности протекания электрохимических процессов обычно используют диаграммы Пурбэ. Анализ диаграмм Пурбэ для разных металлов показывает, что в водных средах, содержащих О2 и Н+, металлы корродируют поразному, в зависимости от рН:
- а) если потенциал металла положительнее потенциала кислородного электрода (верхняя зона диаграммы), то коррозия металла невозможна (например потенциал золота);
- б) если потенциал металла положительнее потенциала водородного электрода и отрицательнее потенциала кислородного электрода (средняя зона диаграммы), коррозия возможна с поглощением кислорода и невозможна с выделением водорода;
- в) если потенциал металла отрицательнее потенциала водородного электрода (нижняя зона диаграммы), то возможна коррозия как с поглощением кислорода, так и с выделением водорода (щелочные и щелочноземельные металлы, магний, алюминий, цинк и др.).
Примеры решения задач Пример 1. Во сколько раз возрастает толщина плёнки при увеличении продолжительности равномерной газовой коррозии титана от 8 до 100 ч при 300 оС.
Решение:
На алюминии, хроме (при t<350 oC) и некоторых других металлах плёнка оксида растёт во времени ф по логарифмическому закону:
д = k lnф, где д — толщина плёнки.
Соответственно д1 = k ln8,.
д2 = k ln100.
Отсюда следует, что толщина плёнки (д2/д1) увеличится в 2.53 раза (ln (100/8)=2.53).
Пример 2. Определите скорость равномерной коррозии железа в (мм/год) и в [г/(м2?год)], если плотность коррозионного тока составляет 0.02 А/м2.
Решение:
Скорость равномерной коррозии, выраженная в г/(м2?с), равна.
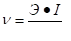
где Э — молярная масса эквивалента металла (г/моль);
I — плотность тока коррозии, А/м2;
F — число Фарадея, F = 96 500 Кл/моль.
Умножая эту величину на число секунд в сутки (3600?24) и число дней в году (365), получим скорость коррозии в году н = 170 г/(м2?год). Для перевода этой размерности в мм/год используем плотность железа с=7.87 г/см3. После преобразования единиц получим н = 0.022 мм/год.
Пример 3. Возможна ли электрохимическая коррозия олова (Sn) в водном растворе при рН=6 при контакте с воздухом, если относительные парциальные давления газов равны p (H2) = 1, p (O2) = 0.21? Напишите уравнения реакций анодного и катодного процессов. При каких значениях рН возможна коррозия с выделением кислорода?
Решение:
Найдём стандартный электродный потенциал олова (E0(Sn2+/Sn0=0.136 В). По уравнению Нернста определим равновесные потенциалы вероятных окислителей (H+ и O2) при 25 оС, p (H2) = 1, p (O2) = 0.21.
E (H+/H2) = 0.059?pH = 0.059?6 = 0.354 В,.
E (О2/ОН) = 1.227 0.059?pH + 0.0147?lg0.21= 1.227 0.059?6 — 0.01 = 0.873 В.
Рассчитаем ЭДС предполагаемых коррозионных микроэлементов:
е1 = Ек (Н2) — Еа = 0.354 В — (0.136 В) = 0.218 В < 0 — коррозия с выделением водорода невозможна.
е2 = Ек (О2) — Еа = 0.873 В — (0.136 В) = 1.009 В > 0 — коррозия с поглощением кислорода возможна.
Таким образом, уравнения реакций анодного и катодного процессов выглядят следующим образом:
- (анод) Sn — 2e > Sn2+
- (катод) ½ O2 + 2H+ + 2e > H2O.
Для выяснения диапазона значений рН, при которых возможна коррозия с водородной деполяризацией, решим неравенство:
е1 = Ек (Н2) — Еа > 0.
После подстановки значений электродных потенциалов получим.
0.059 ?pH — (0.136 В) > 0,.
Откуда следует, что при значениях рН < 0.136/0.059 = 2.26 идёт процесс с выделением водорода.
Пример 4. Определите, будет ли корродировать медь (Cu) в деаэрированном (без содержания кислорода) растворе CuSO4 в кислом растворе с рН=0 и выделением водорода при его относительном парциальном давлении p (H2) = 0.1.
Решение:
Стандартный потенциал меди составляет E0(Сu2+/Cu0)=+0.337 В, а потенциал водорода рассчитаем по уравнению Нернста:
E (H+/H2) = 0.0295?lg p (H2) 0.059?pH = 0.0295?lg0.1 0.059?0 = +0.0295 В.
ЭДС коррозионного микроэлемента:
е = Ек (Н2) — Еа = +0.0295 В — 0.337 В < 0 — коррозия протекать не будет.
Пример 5. Определите возможность электрохимической коррозии с водородной деполяризацией гальванической пары СuZn, погруженной в 0.01М раствор ZnSO4 при 25 oC. Как изменится ЭДС коррозионного элемента в результате концентрационной поляризации анода, если концентрация раствора возросла до 0.05 моль/л?
Решение:
С учётом гидролиза соли, образованной слабым основанием и сильной кислотой, рассчитываем рН раствора:
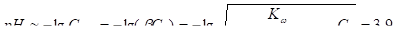
Равновесный потенциал водорода в предположении, что его относительное давление равно 1:
E (H+/H2) = 0.059?pH = 0.230 В.
Для выбора корродирующего металла воспользуемся их стандартными потенциалами (E0(Сu2+/Cu0=+0.337 В, E0(Zn2+/Zn0=0.763 В). Потенциал меди значительно положительнее потенциала предполагаемого катода, и электрохимическая коррозия идёт с участием цинка. Запишем процессы в коррозионном элементе:
- (анод) Zn — 2e > Zn2+
- (катод) 2H+ + 2e > H2.
Для расчёта ЭДС указанного микроэлемента уточним равновесный потенциал цинка, используя уравнение Нернста для 25 oC:
E1(Zn2+/Zn0) = 0.763 + (0.059/2)?lg102.
При увеличении концентрации ZnSO4 его потенциал изменяется:
E2(Zn2+/Zn0) = 0.763 + (0.059/2)?lg (5?102) = E1(Zn2+/Zn0) + (0.059/2)?lg5.
Таким образом, учитывая, что е = Ек — Еа, значение ЭДС уменьшится на величину Де = (0.059/2)?lg5 = 0.02 В.
Пример 6. Определите возможность электрохимической коррозии стального изделия (железа) в 0.1М растворе FeCl2, комнатной температуре (T=298 K) при следующих относительных парциальных давлениях водорода и кислорода: p (H2) = 0.1, p (O2) = 0.9.
Решение:
Указанная соль подвергается гидролизу. Учитывая первую ступень гидролиза:
Fe2+ + H2O — H+ + FeOH+, можно определить значение рН, величина которого, как видно из реакции меньше 7, т. е. коррозия идёт в подкисленной среде. Найдём рН раствора, принимая активность ионов равной их концентрации:
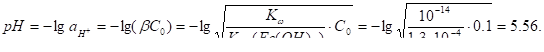
Теперь можно определить равновесные электродные потенциалы вероятных окислителей (H+ и O2):
E (H+/H2) = 0.0295?lg p (H2) 0.059?pH = 0.0295?lg0.1 0.059?5.56 = 0.3 В,.
E (О2/ОН) = 1.227 0.059?pH + 0.0147?lg p (О2) = 0.9 В.
Равновесный потенциал предполагаемого анода при 25 oC:
E (Fe2+/Fe0) = E (Fe2+/Fe0) + (0.0592/2))?lg a (Fe2+) = 0.44 (0.0592/2)?1 = 0.47 В.
Учитывая, что е1 = Ек (Н+) — Еа = 0.3 В — (0.47 В) = +0.17 В > 0 — коррозия с выделением водорода возможна.
е2 = Ек (О2) — Еа = 0.9 В — (0.47 В) = +1.37 В > 0 — коррозия с поглощением кислорода также возможна.
Таким образом, возможна коррозия железа с протеканием на катоде двух реакций:
- 2H+ + 2e > H2
- ½ O2 + 2H+ + 2e > H2O.
Пример 7. Стальное изделие имеет цинковое покрытие. Какой из металлов будет окисляться при коррозии, если эта пара металлов попадёт в нейтральную среду с рН=7? Подсчитайте ЭДС коррозионного элемента для стандартных условий. При каких рН прекратится процесс выделения водорода?
Решение:
Стандартный потенциал цинка составляет E0(Zn2+/Zn0)= 0.763 В, а потенциал железа E0(Fe2+/Fe0)= 0.44 В. Учитывая, что потенциал цинка более отрицателен, цинк является анодным покрытием. При этом железо не будет принимать участие в анодном процессе, т. е. не будет корродировать.
Равновесные потенциалы водорода и кислорода, при их парциальных давлениях, равных 1, определяем по уравнениям.
E (H+/H2) = 0.059?pH = 0.059?7 = 0.413 В,.
E (О2/ОН) = 1.227 0.059?pH = +0.814 В.
ЭДС коррозионных микроэлементов равны:
е1 = Ек (Н+) — Еа = 0.413 В — (0.763 В) = +0.35 В > 0 — коррозия с выделением водорода возможна;
е2 = Ек (О2) — Еа = 0.814 В — (0.763 В) = +1.577 В > 0 — коррозия с поглощением кислорода также возможна.
Катодные процессы:
- 2H2O + 2e > 2OH + H2
- ½ O2 + H2O + 2e > 2OH.
Процесс выделения водорода прекратится, если е1<0,т.е. 0.059?рН — (0.763) <0, откуда следует, что рН<12.9 е1<0, при этом процесс коррозии цинка с поглощением кислорода будет иметь место при любых значениях рН.
Контрольное задание Многовариантные задачи Задача 1. Гальваническая пара, состоящая из двух различных металлов, помещена в раствор электролита (см. таблицу). Какой металл и почему будет корродировать? Написать уравнения соответствующих электрохимических процессов (образование пассивирующих плёнок не учитывать).
Номер варианта. | Гальваническая пара, электролит. | Номер варианта. | Гальваническая пара, электролит. | Номер варианта. | Гальваническая пара, электролит. | |
Pb | H+ | Cu. | Fe | H2O+O2 | Pd. | Sn | H+ | Cu. | ||||
Cr | H+ | Bi. | Sn | H+ | Ag. | Mn | OH | Fe. | ||||
Co | OH | Bi. | Ni | H2O + O2 | Cu. | Al | H2O + O2 | Ni. | ||||
V | H2O + O2 | Cu. | Al | H2O + O2 | Zn. | Zn | OH | Ni. | ||||
Zn | H+ | Fe. | Cu | OH | Co. | Al | H+ | Fe. | ||||
Задача 2. Для пары металлов:
- 1) определите, возможна ли коррозия металла из данной пары в среде с заданным рН при контакте с воздухом;
- 2) напишите уравнения анодного и катодного процессов;
- 3) предложите для данной пары анодное и катодное покрытие. Изменятся ли и если изменятся, то как коррозионные процессы при нарушении сплошности покрытий. Запишите уравнения реакций.
- 4)
Номер варианта. | Пары металлов. | рН. | Номер варианта. | Пары металлов. | рН. | Номер варианта. | Пары металлов. | рН. | |
Pb — Sn. | Sn — Cd. | Fe — Pb. | |||||||
Sn — Cu. | Cd — Cu. | Sn — Ag. | |||||||
Fe — Co. | Zn — Ag. | Zn — Ni. | |||||||
Cu — Co. | Cd — Pb. | Mg — Ni. | |||||||
Fe Ni. | Fe — Cu. | Zn Sn. | |||||||
Предлагаемые варианты заданий для индивидуальной работы Вариант № 1 Задача 3. Определите скорость равномерной коррозии алюминия в (мм/год) и в [г/(м2?сут)], если плотность коррозионного тока составляет 0.062 А/м2.
Задача 4. В чём сущность протекторной защиты металлов от коррозии? Приведите пример протекторной защиты железа в электролите, содержащем растворённый кислород. Составьте уравнения анодного и катодного процессов.
Вариант № 2.
Задача 3. Магний равномерно корродирует в морской воде со скоростью 1,45 г/(м2?сут). Каково значение скорости коррозии, выраженное в мм/год? Если с такой же скоростью корродирует свинец, то каково соответствующее значение скорости коррозии в мм/год?
Задача 4. Как проходит атмосферная коррозия луженого железа и луженой меди при нарушении покрытия? Составьте уравнения анодной и катодной реакций.
Вариант № 3.
Задача 3. Во сколько раз возрастает толщина плёнки при увеличении продолжительности равномерной газовой коррозии ванадия от 0 до 200 ч при 900 оС?
Задача 4. Какой металл может служить протектором при защите железа от коррозии в одном растворе с рН = 10 в контакте с воздухом? Напишите уравнения протекающих реакций.
Вариант № 4.
Задача 3. Объясните, почему в атмосферных условиях цинк корродирует, а золото нет? Ответ подтвердите расчётами.
Задача 4. Будет ли протекать электрохимическая коррозия изделия пары NiCu в растворе NiSO4, имеющего концентрацию 0.03 моль/л при 35 оС? Как изменится ЭДС коррозионного элемента, если концентрация ионов Ni2+ возросла до 0.05 моль/л?
Вариант № 5.
Задача 3. Возможна ли коррозия олова в водном растворе с рН = 6 при контакте с воздухом? При каких значениях рН возможна коррозия с выделением водорода?
Задача 4. Изделие из цинка погрузили в 0.04М раствор ZnSO4 при 60 оС. Будет ли цинк корродировать?
Вариант № 6.
Задача 3. Возможна ли электрохимическая коррозия свинца (Pb) в водном растворе при рН = 6 при контакте с воздухом? Напишите уравнения реакций анодного и катодного процессов. При каких значениях рН возможна коррозия с выделением водорода?
Задача 4. Определите возможность электрохимической коррозии изделия пары FeCd, погруженной в 0.005М раствор FeCl2 при комнатной температуре, принимая коррозию избирательной. Как изменится ЭДС коррозионного элемента, если концентрация раствора возросла до 0.015 моль/л?
Вариант № 7.
Задача 3. Определите, будет ли корродировать медь (Cu) в деаэрированном (без содержания кислорода) растворе при рН = 0?
Задача 4. Железное изделие покрыли свинцом. Какое это покрытие — анодное или катодное? Составьте уравнения анодного и катодного процессов коррозии этого изделия при нарушении цельности покрытий во волажном воздухе и в растворе соляной кислоты.
Вариант № 8.
Задача 3. Магний (Mg) корродирует в морской воде (рН = 8) при контакте с воздухом. Напишите уравнения реакций анодного и катодного процессов.
Задача 4. Как протекает атмосферная коррозия луженого железа и луженой меди, если покрытие нарушено? Составьте электродные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
Вариант № 9.
Задача 3. Изделие из цинка погрузили в 0.03М раствор ZnSO4 при 70 оС. Будет ли цинк корродировать?
Задача 4. Если пластинку из чистого цинка опустить в разбавленную кислоту, то начинающееся выделение водорода вскоре почти прекратится. Однако при прикосновении к цинку медной палочкой на последней начинается бурное выделение водорода. Дайте этому объяснение, составив электродные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции.
Вариант № 10.
Задача 3. Будет ли протекать электрохимическая коррозия изделия пары NiCu в растворе NiSO4, имеющего концентрацию 0.04 моль/л при 25 оС? Как изменится ЭДС коррозионного элемента, если концентрация ионов Ni2+ возросла до 0.06 моль/л?
Задача 4. Цинковую и железную пластины опустили в раствор сульфата меди (II). Составьте электродные и ионные уравнения реакций, происходящих на каждой из пластин. Какие процессы будут проходить на пластинах, если их наружные концы соединить проводником?
Вариант № 11.
Задача 3. Определите возможность электрохимической коррозии изделия пары FeCd, погруженной в 0.01М раствор FeCl2 при комнатной температуре, принимая коррозию избирательной. Как изменится ЭДС коррозионного элемента, если концентрация раствора возросла до 0.02 моль/л?
Задача 4. Железное изделие покрыли кадмием. Какое это покрытие — анодное или катодное? Составьте уравнения анодного и катодного процессов коррозии этого изделия при нарушении цельности покрытий во волажном воздухе и в растворе соляной кислоты.
Вариант № 12.
Задача 3. Изделие из железа с алюминиевым покрытием погрузили в 0.01М раствор AlCl3. Будет ли протекать коррозия этого изделия при комнатной температуре? Будет ли изменяться ЭДС и как, если концентрация раствора возрастёт до 0.03 моль/л?
Задача 4. Магний равномерно корродирует в морской воде со скоростью 1,55 г/(м2?сут). Каково значение скорости коррозии, выраженное в мм/год? Если с такой же скоростью корродирует свинец, то каково соответствующее значение в мм/год?
Вариант № 13.
Задача 3. Олово спаяно с серебром. Какой из металлов будет окисляться при коррозии, если эта пара находится в щелочной среде? Подсчитайте ЭДС этого элемента для стандартных условий.
Задача 4. Определите скорость равномерной коррозии алюминия в (мм/год) и в [г/(м2?сут)], если плотность коррозионного тока составляет 0.06 А/м2.
Вариант № 14.
Задача 3. Алюминий склёпан медью. Какой из металлов будет подвергаться коррозии, если эти металлы попадут в кислую среду? Составьте схему гальванического элемента, образующегося при этом. Подсчитаёте ЭДС этого элемента для стандартных условий.
Задача 4. Будет ли протекать электрохимическая коррозия изделия пары NiCu в растворе NiSO4, имеющего концентрацию 0.03 моль/л при 45 оС? Как изменится ЭДС коррозионного элемента, если концентрация ионов Ni2+ возросла до 0.07 моль/л?
Вариант № 15.
Задача 3. Железо покрыто хромом. Какой из металлов будет корродировать в случае нарушения поверхностного слоя покрытия в атмосфере промышленного района (влажный воздух содержит CO2, H2S, SO2 и др.)? Составьте схему процессов, происходящих на электродах образующегося гальванического элемента.
Задача 4. Изделие из железа с алюминиевым покрытием погрузили в 0.005М раствор AlCl3. Будет ли протекать коррозия этого изделия при комнатной температуре? Будет ли изменяться ЭДС и как, если концентрация раствора возрастёт до 0.04 моль/л?