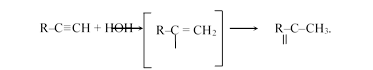Карбонильные соединения, номенклатура и изомерия.
Строение и химические свойства, качественные реакции на карбонильные соединения

В молекуле любого альдегида или кетона в связи с большей электроотрицательностью атома кислорода по сравнению с углеродным атомом подвижные электроны р-связи в карбонильной группе сдвинуты в сторону атома кислорода. Этот сдвиг вызывает появление избыточной электронной плотности на атоме кислорода (-) и соответственное уменьшение электронной плотности на карбонильном, атоме углерода (+), что… Читать ещё >
Карбонильные соединения, номенклатура и изомерия. Строение и химические свойства, качественные реакции на карбонильные соединения (реферат, курсовая, диплом, контрольная)
Карбонильные соединения являются производными углеводородов, в молекулах которых два водородных атома, находящихся у одного атома углерода, замещены атомом кислорода. Таким образом получается группа С=О, называемая карбонильной группой или оксогруппой.
В молекуле любого альдегида или кетона в связи с большей электроотрицательностью атома кислорода по сравнению с углеродным атомом подвижные электроны р-связи в карбонильной группе сдвинуты в сторону атома кислорода. Этот сдвиг вызывает появление избыточной электронной плотности на атоме кислорода (-) и соответственное уменьшение электронной плотности на карбонильном, атоме углерода (+), что вызывает, в свою очередь, смещениеэлектронов соседних углеродуглеродных связей:
Тривиальные названия альдегидов очень распространены, они связаны с тривиальными наименованиями кислот с тем же углеродным скелетом, в которые альдегиды легко переходят при окислении.
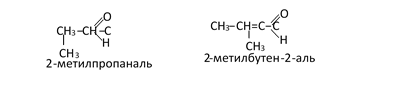
По номенклатуре ИЮПАК наличие альдегидной группы обозначается суффиксом — аль:
Названия простых кетонов обычно составляются из названий радикалов, связанных с карбонильной группой, и слова кетон:
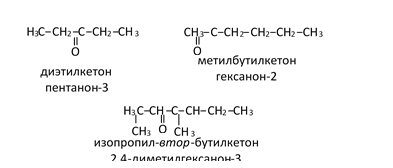
Для названий более сложных кетонов используют суффикс —он:
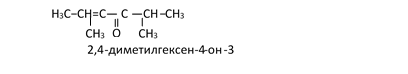
Изомерия альдегидов обусловлена изомерией цепи радикала, кетонов — положения карбонильной группы, а также изомерией радикалов и метамерией. Альдегиды и кетоны с одинаковым числом атомов углерода являются изомерами.
Химические свойства:
— присоединение водорода (восстановление):
— присоединение спиртов:
В присутствии каталитических количеств безводных сильных кислот к альдегидам легко присоединяются спирты с образованием полуацеталей и ацеталей:
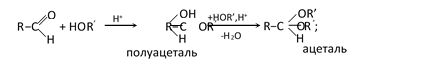
— присоединение синильной кислоты:
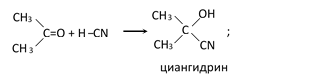
Альдегиды и кетоны присоединяют HCN в присутствии следов щелочей с образованием оксинитрилов (циангидринов):
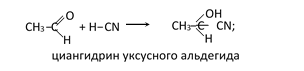
— присоединение металлоорганических соединений:
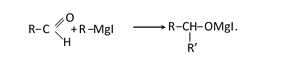
При разложении полученных соединений водой получаются спирты.
— образование бисульфитных соединений:
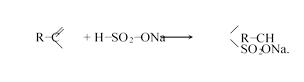
— с пятигалогенидами фосфора
Получаются галогенопроизводные углеводородов с двумя атомами галогена при одном атоме углерода (геминальные производные):
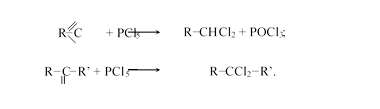
— галогенирование:
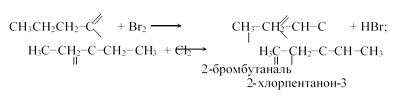
— реакции конденсации:
При действии на холоде слабых растворов щелочей на уксусный альдегид и его гомологи происходит реакция альдольной конденсации:
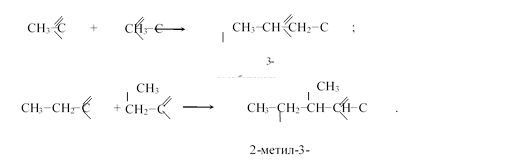
Альдоли (альдегидалкоголи) — малоустойчивые соединения. Они легко отщепляют воду и образуют ,-непредельные карбонильные соединения:

Конденсация альдегидов, протекающая с отщеплением воды, называется кротоновой (характерна только для альдегидов, имеющих атом Н в б-положении).
— окисление альдегидов:
Альдегиды легко окисляются до карбоновых кислот с тем же числом углеродных атомов. Они могут окисляться даже кислородом воздуха и такими слабыми окислителями, как аммиачный раствор гидроксида серебра (реактив Б. Толленса) или реактив Г. Фелинга [смесь растворов CuSO4, КОН и тартрата (соли винной кислоты) щелочных металлов].
реакция с аммиачным раствором гидроксида серебра (реакция «серебряного зеркала»)
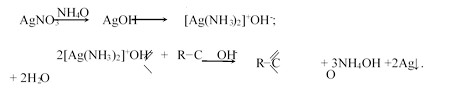
Иногда эту реакцию записывают в сокращенном виде:
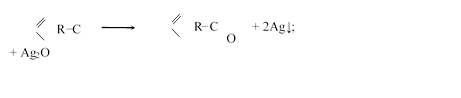

окисление гидроксидом меди (II).
Если к жидкости со светло-голубым осадком гидроксида меди (II) прибавить жидкость, содержащую альдегид, и нагреть смесь, то голубой осадок превращается в желтый осадок гидроксида меди (I) CuOH, а затем — в красный осадок оксида меди (I) Cu2O. Альдегид при этом превращается в кислоту: атом кислород бисульфитный кетон.
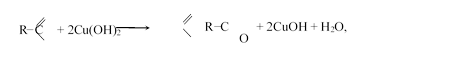
а желтый гидроксид меди (I) превращается в красный оксид:
2СuОН Сu2Оv+ Н2О.
Часто, чтобы сделать реакцию более отчетливой, гидроксид меди (II) предварительно растворяют при помощи солей виннокаменной кислоты. Если получающуюся при этом синюю жидкость (фелингов раствор) нагреть с альдегидом, то он окисляется в кислоту содержащейся в ней двухвалентной медью, а последняя восстанавливается и выпадает в осадок в виде красного оксида меди (I).
— окисление кетонов:
Кетоны устойчивы к действию окислителей и окисляются только сильными окислителями при нагревании (например, раствором марганцевокислого калия), причем окисление происходит иначе, чем окисление альдегидов. При окислении молекула кетона расщепляется с образованием молекул кислот или кислоты и кетона с меньшим числом углеродных атомов, чем первоначальный. Разрыв цепи углеродных атомов происходит рядом с карбонильным атомом углерода:
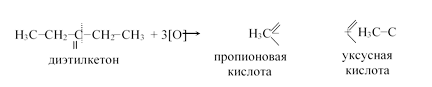
— качественные реакции на альдегиды:
Для открытия альдегидов используют реакции «серебряного зеркала», с реактивом Фелинга, а также очень чувствительные цветные реакции. Наиболее употребительным реактивом на альдегиды является «фуксинсернистая кислота» (раствор фуксина (NH2-С6Н4)2С (ОН)СбН3(СН3)NН2, обесцвеченный прибавлением сернистой кислоты), дающая даже с небольшим количеством альдегидов красное или фиолетовое окрашивание.
Получение карбонильных соединений:
— окисление спиртов:
При окислении первичных спиртов получаются альдегиды, а вторичных — кетоны. Окислителями служат «хромовая смесь» (смесь К2Сr2О7 или Na2Cr2О7 с серной кислотой), перманганаты различных металлов или перекись марганца и серная кислота.
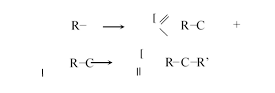
— дегидрирование спиртов:
При пропускании паров спирта над накаленными металлами (Ni, Fe, Zn и др.) спирты распадаются на альдегид (или кетон) и водород.
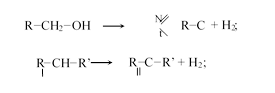
— cухая перегонка (термическое разложение) кальциевых и бариевых солей одноосновных кислот:
Для всех кислот, кроме муравьиной, реакция идет следующим образом:
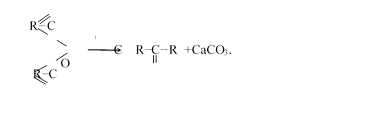
Если взять смесь солей двух кислот или смешанную соль, то наряду с предыдущей происходит также реакция между молекулами разных солей:
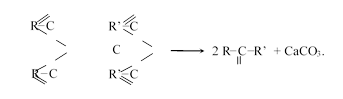
Если же взять смесь солей, одна из которых — соль муравьиной кислоты, то получается альдегид:
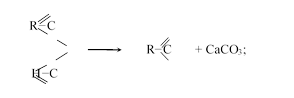
— действие воды на дигалогенопроизводные соединения, содержащие оба атома галогена при одном углеродном атоме:

— действие воды на алкины (реакция М. Кучерова):
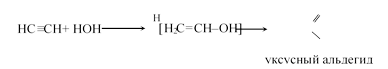
При действии воды в тех же условиях гомологи ацетилена дают кетоны: