Элементы группы vа — группа азота

Азот можно считать наиболее легко доступным химическим элементом после кислорода, так как он составляет более ¾ массы земной атмосферы. Но в земной коре его содержание во много раз меньше, чем содержание кислорода. Фосфор по распространенности несколько превосходит серу. Как азот, так и фосфор являются биогенными элементами, и их значение в химической технологии связано прежде всего… Читать ещё >
Элементы группы vа — группа азота (реферат, курсовая, диплом, контрольная)
Изучив содержание главы 20, студенты должны:
знат
- • положение азота и фосфора в таблице Менделеева, нахождение в природе и практическое применение;
- • строение атомов, валентность, степени окисления азота и фосфора;
- • способы получения и свойства простых веществ — азота и красного и белого фосфора;
- • основные типы соединений азота и фосфора;
- • особенности элементов подгруппы мышьяка;
уметь
- • составлять уравнения реакций получения азота и красного и белого фосфора и реакций, характеризующих химические свойства этих веществ;
- • проводить сопоставление свойств элементов в группе азота;
- • характеризовать практически важные соединения азота и фосфора;
- • проводить расчеты по уравнениям реакций, в которых участвуют азот и фосфор;
владеть
• навыками прогнозирования протекания реакций с участием азота, фосфора и их соединений.
Строение атомов. Распространенность в природе
Группа УА таблицы Менделеева состоит из пяти элементов с нечетными атомными номерами: азот N. фосфор Р, мышьяк Аб, сурьма БЬ и висмут В1 (табл. 20.1). Фосфор, мышьяк и висмут имеют по одному устойчивому изотопу. Висмут является последним устойчивым элементом в таблице Менделеева. У азота два изотопа, причем составляет 99,63% и лишь 0,37% — изотоп У N. Сурьма представлена приблизительно поровну двумя устойчивыми изотопами ,||5Ь (57,3%) и (42,7%).
Таблица 20.1
Характеристика элементов группы УА.
Свойство. | Элемент. | ||||
N. | Р. | А.8. | БЬ. | В1. | |
Порядковый номер | |||||
Радиус г атома (ковалентный), нм. | |||||
Содержание в земной коре со, %. | 2.5−10 3 | 0,1. | 1.5• 10″ 4 | 2 10 5 | 4.8• 10-6 |
Окончание табл. 20.1
Свойство. | Элемент. | ||||
N. | Р. | А*. | БЬ. | В1. | |
Содержание в орга; | 2,6*. | 1,1*. | 2,6• 105 | 4,1 Ю" 4 | 3,3• 1 о-7 |
низме человека <�о, % Электроотрицатель; | 3,0. | 2,3. | 2,2. | 2,1. | 2,0. |
ность, х Тип структуры прос; | Молеку; | Молекуляр; | Ковалент; | Метал; | Метал; |
того вещества. | лярная. | ная и кова; | ная и моле; | лическая. | лическая. |
лентная. | кулярная. | ||||
* Биогенный элемент.
Азот можно считать наиболее легко доступным химическим элементом после кислорода, так как он составляет более ¾ массы земной атмосферы. Но в земной коре его содержание во много раз меньше, чем содержание кислорода. Фосфор по распространенности несколько превосходит серу. Как азот, так и фосфор являются биогенными элементами, и их значение в химической технологии связано прежде всего с биогенностью. Ежегодно производятся сотни миллионов тонн азотных и фосфорных удобрений для сельскохозяйственных растений. Соответственно, как азот, так и фосфор являются составляющими продукции сельского хозяйства и пищевой промышленности.
Открытие азота официально приписывается Д. Резерфорду (1772) в период быстрого развития пневматической химии. Почти одновременно с ним азот получили Г. Кавендиш, Д. Пристли и К. Шееле. Фосфор открыл гамбургский алхимик-любитель X. Бранд в 1669 г. В последующие годы секрет получения фосфора разгадали и другие химики.
Оставшиеся три элемента группы — мышьяк, сурьму и висмут — рассматривают в качестве подгруппы мышьяка. Эти элементы несколько более распространены в природе, чем находящиеся справа от них элементы подгруппы селена. Мышьяк описывается в трудах Альберта Великого (1250). Его элементарная природа установлена Г. Брандтом (1733). Металлическая сурьма известна с третьего тысячелетия до нашей эры. Висмут упоминается в работах Василия Валентина (1450). Его принимали за разновидность свинца. Латинское название ему дал Г. Агрикола в 1530 г.
В подгруппе мышьяка заметно усиливается металличность по сравнению с подгруппой селена. По химическим свойствам мышьяк можно отнести к неметаллам, но в виде простого вещества он обладает высокой электрической проводимостью, превышающей проводимость следующих элементов группы — сурьмы и висмута. Все три элемента применяются главным образом как добавки в сплавы различного назначения. Мышьяк применяется также в полупроводниковой технике, так как некоторые его соединения с металлами оказываются полупроводниками.
Внешние энергетические уровни атомов группы УА далеки от максимальной заселенности электронами. На внешнем р-подуровне все их электроны неспаренные:
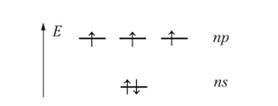
Электронные формулы атомов:

Очевидно, что в основном состоянии элементы группы азота трехвалентны. У всех элементов группы, кроме азота, на внешнем уровне имеется незаполненный ^/-подуровень. В возбужденном состоянии эти элементы становятся пятивалентными. Особенно устойчиво пятивалентное состояние у фосфора. Из электронных формул очевидно, что элементы подгруппы мышьяка имеют 18-электронную подоболочку, подобно элементам подгруппы селена. Этим обусловлен характер изменения свойств и значительное различие между элементами подгрупп (в данном случае подгруппы мышьяка) и элементами 2-го и 3-го периодов — азотом и фосфором.
Элементы группы азота менее электроотрицательны, чем халькогены и галогены. Но азот с относительной электроотрицательностью х = 3,0 все же стоит на третьем месте после фтора и кислорода. Электроотрицательность фосфора значительно ниже (х = 2,3) и лишь незначительно превышает электроотрицательность водорода.
Табличное значение элсктроотрицательности хлора такое же, как и азота. Однако из рассмотрения реакции.

можно заключить, что х (М) > х (С1). При этом условии на азоте имеется отрицательный заряд (-5), и при гидролизе с ним соединяется водород с положительным зарядом. Атом хлора с зарядом +6 соединяется с гидроксогруппой.