Радий.
Радиоэкология и экологическая радиохимия

В отдаленные сроки после поражения Ra развиваются злокачественные новообразования. Остеосаркомы наблюдались при дозах 94−440 Гр, а карциномы при дозах 64−260 Гр. 22"Ra практически всю энергию распада отдаёт на костные структуры. При инкорпорации 226Ra значительные количества проникают в минеральные структуры костной ткани, где отсутствуют эндостальные клетки, вследствие чего основная доля энергии… Читать ещё >
Радий. Радиоэкология и экологическая радиохимия (реферат, курсовая, диплом, контрольная)
Радий Ra — щелочноземельный металл главной подгруппы и группы периодической системы, Z- 88.
В природе как члены естественных радиоактивных рядов встречаются 4 изотопа: 226Ra (1600 л, ряд 238U), 224Ra (ThX, 3,66 дн, ряд 232Th), 228Ra (MsThI, мезоторий-i, 5,76 л), 223Ra (АсХ, 11,43 дн, РЯД 235U). Непосредственный продукт распада Ra — радиоактивный газ Rn, конечные продукты распада — изотопы РЬ и Bi. 226Ra вместе с продуктами своего распада излучает все три вида радиации — а-, ри у-лучи, 228Ra — достаточно мощный природный р-излучатель.
Радий-224 (ThX) 224Ra — член радиоактивного семейства 2з2ТЬ, а, 3,6319 дн, энергия распада 5,78 885 МэВ, средняя энергия а-излучения 5,78 МэВ, дочерний нуклид 22°Rn (55,6 с) — торон. Активность 1 г 224Ra.
— 5,89 210"5 Бк. Материнский изотоп 228Th (а-распад, 1,9116 л), кроме того, 224Ra образуется при p-распаде 22<*Fr (3,33 мин, энергия распада 2,83 МэВ) и р+-распаде 22«Ас (2,78 ч, энергия распада 1,408 МэВ).
Радий-226 принадлежит к радиоактивному семейству 238U. Активность 1 г этого нуклида 3,657 710ю Бк (~1 Ки). Г,/2= 1600 л, а-распад, энергия распада 4,87 062 МэВ, энергия испускаемых а-частиц 4,7843 МэВ (в 94,45% случаев) и 4,601 МэВ (в 5,55% случаев), при этом часть энергии выделяется в виде у-кванта (в 3,59 % случаев происходит испускание у-кванта с энергией 186,21 кэВ) дочерний нуклид 222Rn (3,8235 дн). 226Ra образуется в результате распада 2з°ТЬ (а, 75 380 л), кроме того, 226Ra образуется при р~- распаде 226Fr (49 с, энергия распада 3,7 МэВ) и осуществлении электронного захвата нуклидом 22бАс (энергия распада 1,113 МэВ). Период полураспада по спонтанному делению 226Ra составляетю1'" л, что соответствует 0,6 акту деления на 1 г 226Ra в 1 с. 226Ra образуется в результате распада 23°Th (а, 75 380 л), кроме того, 226Ra возникает при р—распаде 226Fr (49 с, Ерat«= 3,7 МэВ) и осуществлении электронного захвата нуклидом 22бАс СЕрасн= 1,113 МэВ). За счёт радиоактивного распада ядер 226Ra и дочерних продуктов распада 1 г Ra выделяет 550 Дж/ч теплоты. При распаде 226Ra превращается в 222Rn. За 1 сутки из 1 г «6Ra образуется ~1 ммз Rn.
Распад 226Ra приводит к образованию радиоактивной цепочки:

Соль Ra является чистым а-излучателем. При накоплении в ней продуктов распада препарат становится источником ри у-излучения. Равновесная соль Ra — мощный постоянный источник у-излучения.
Радий-228 (мезоторий I, MsTh I, 5,75 л) — член радиоактивного семейства 23'2Th. Образуется при а-распадеTh (1,405-ю10 л, энергия распада.
4,0816 МэВ). 228Ra претерпевает р-распад (5,75 л, энергия распада 0,0458 МэВ), продукт распада 228Ас (р—распад, 6,15 ч, энергия распада 2,1238 МэВ). Активность 1 г 228RaljOMO18 Бк.
С химической точки зрения Ra — щёлочноземельный металл, похож на Ва, но химически более активен. В соединениях проявляет степень окисления +2.
Определение Ra проводят аи у-спектрометрическими методами, эманационным, радиометрическим, авторадиографическим, а также методами изотопного разбавления и активационного анализа. Удельная активность 226Ra определяется линии 186,0 кэВ в у-спектре, за вычетом вклада 235U (185,7 кэВ). При определении Ra методом изотопного разбавления в качестве носителя используется РЬ. Для обнаружения 226Ra в различных объектах используются аи у-спектрометры, с помощью которых можно определять до 10^% Ra без его предварительного выделения.
Характерной особенностью a-активных изотопов Ra является существование у них газообразного продукта распада — Rn. Радон регистрируется достаточно надёжно, а по нему можно обнаружить его предшественника — Ra и идентифицировать его изотоп.
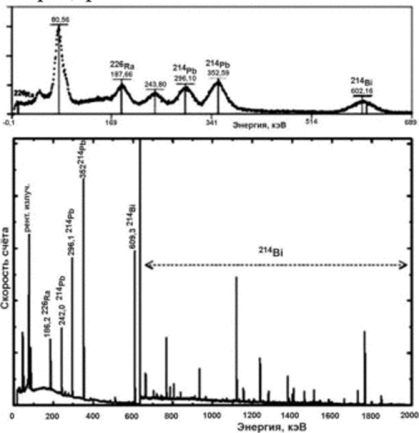
Рис. 4. у-Спектр 226Ra и продуктов его распада: сцинтилляционный детектор (вверху) и полупроводниковый детектор (внизу).
В тех случаях, когда анализируемая проба содержит смесь изотопов Ra, их идентификацию производят, наблюдая за изменением активности газовой компоненты, выделенной из образца, с последующим разложением полученной кривой на её составляющие в соответствии с постоянными радиоактивного распада л. По форме кривой изменения активности выделенной порции газа можно идентифицировать изотопы радона.
При интерпретации у-спектров Ra следует учитывать, что спектры Ra и Rn аналогичны; исключение составляет только линия 186 кэВ в спектре Ra, которая отсутствует в спектре Rn.
Несколько сложнее обстоит дело с идентификацией 228Ra, когда он находится в смеси с другими изотопами Ra, ввиду того что у-спектр препаратов 228Ra, полностью относящийся к дочернему 228Ас (6,13 ч), почти совпадает со спектрами продуктов распада 226Ra и 22^Ra. В таких случаях получающийся с помощью германиевого детектора спектр смеси расшифровывают методом разложения, с вычитанием спектра 22*Ra, нормированного к пику 2о8Т1 с энергией 2,62 МэВ, и затем спектра 226Ra, нормированного к пику 2,4Bi с Е./= 1,76 МэВ. В некоторых случаях 224Ra предварительно осаждают, например, на Mn-волоконных адсорбентах, и определяют его эманационным сцинтилляционным методом (по 22°Rn).
Классический метод определения 228Ra в природных водах основан на у-спектрометрии (по 228Ас). В нём сначала осуществляется выделение и очистка 228Ra, после чего происходит накопление дочернего 228Ас в течение 36 час. В экспресс-анализе 228Ас выделяется из воды быстрым осаждением с карбонатом кальция при малом количестве фосфата и очищается от Са, Pb, Bi, U, Th и Ра пропусканием анализируемой пробы воды через колонку с катионитом. Результат анализа выдаётся через 6 час.
Для выделения Ra используются методы соосаждения с сульфатом бария из растворов ЭДТА, или соосаждения с ВаС12 из концентрированных растворов НС1. При определении 226Ra, 224Ra, и 22^Ra регистрируется изменение a-активности во времени. Обработка подобной кривой методом наименьших квадратов позволяет определить содержание изотопов Ra в смеси. Наблюдение за p-активностью радиевых препаратов не является столь эффективным способом идентификации, поскольку наличие небольших количеств р-излучающих примесей сильно искажает форму начальной части кривой накопления.
Изотопы Ra обнаруживают по у-активности продуктов его распада. В цепочке 226Ra у-кванты с энергиями 1,76 и 0,609 МэВ являются наиболее характерными, так как они менее всего перекрываются излучением других у-активных веществ. у-Кванты с энергией 2,62 МэВ, испускаемые 2о8Т1, относящимся к генетической цепочке 224Ra, наиболее жёсткие среди всех уизлучений естественных радиоэлементов и потому являются надежным индикатором присутствия Rn. Для идентификации 223Ra может быть использовано у-излучение 211РЬ с энергиями 0,404, 0,425 и 0,829 МэВ.
Изотопы Ra часто идентифицируют по энергетическому спектру испускаемых ими и продуктами их распада а-частиц. Однако получение аспектра представляет по сравнению с у-спектроскопией более сложную задачу. а-Спектр может быть получен с помощью импульсной ионизационной сеточной камеры, пропорционального счётчика, а также с помощью полупроводниковых детекторов высокого разрешения.
Определение 226Ra в почве, растительности и пищевых продуктах проводят эманационным или радиометрическим методом, основанном на выделении суммы изотопов радия в виде сульфата Ra/Ba и непосредственном измерении a-активности препарата 226Ra после полного распада 224Ra. Определение 228Ra основано на осаждении дочернего 228Ас и измерения (3- активности выделенного препарата на малофоновой установке. В организме радий регистрируется по у-излучению от тела, по выдыхаемому радону, а также по, а и p-излучению от крови.
Радий и его соединения широко распространены в природе и являются одним из основных источников естественного радиационного фона. Существуют геохимические провинции с повышенным содержанием радия. Он обнаружен в травянистых и цветочных растениях, кофе, древесине, морских водорослях и т. д. Поведение Ra в природе обусловлено его химическими свойствами: соли Ra изоструктурны солям Ва, Ra обладает более основными свойствами, чем Ва. Соли Ra хуже растворимы, чем соли Ва.
Изотопы Ra отличаются очень низкими концентрациями в природе. Так, среднее содержание 226Ra в земной коре ~мою%, а в природных водах — Ю'14-г10'12 г/л. Низкие концентрации в природных водах определяют поведение атомов Ra, характерное для радионуклидов в разбавленных растворах. В присутствии носителя (Ва) Ra ведёт себя в соответствии с его геохимическими особенностями. Если концентрация Ва в природных водах мала, атомы Ra ведут себя как типичные радиоколлоиды. Они способны адсорбироваться на любых отрицательно заряженных поверхностях твёрдой фазы либо соосаждаться с гидроксидами металлов.
В большинстве пород концентрации изотопов Ra определяются концентрациями U и Th. Исключение составляют молодые вулканические породы, для которых отмечается обогащение 226Ra относительно 238U, либо 228Ra относительно 232Th. Как член семейства *з8и, изотоп Ra 226Ra содержится во всех рудах U. В рудах U содержится также 223Ra, а в рудах Th — 224Ra и 228Ra. Благодаря наличию Th в урановых рудах, 226Ra часто смешан с 228Ra. В урановых рудах на l т U приходится -0,34 г Ra (содержание, устанавливающееся при радиоактивном равновесии в ряду 238U, но многие руды не являются равновесными). В верхнем слое земной коры толщиной 1,6 км содержится 1,8-Ю7 т 226Ra. В результате вымывания Ra из руд U он содержится в растворённом состоянии в воде и образует вторичные руды, например, чёрные глины. Вымытый из урановых минералов Ra обычно концентрируется на глинах, причём, чем старше горные породы по возрасту происхождения, тем больше в них содержится 266Ra и 232Th, но меньше 4°К. Радий подвергается выщелачиванию водой из горных пород и потому урановые минералы теряют значительную часть Ra (иногда до 85%). Затем Ra мигрирует с подпочвенными водами.
Радий поступает в организм человека через органы дыхания (в том числе — при курении), желудочно-кишечный тракт (пища, питьё) и неповрежденную кожу (например, с грязных рук). Поступление Ra в организм человека с воздухом составляет ю13 г-сут1. Поступление с пищей более значительно (90% Ra поступает в организм с пищей и ю% с водой), особенно с пищей, взращенной в регионах с повышенным его содержанием. Довольно много Ra послушает в организм человека с водой.Ra обнаружен в большинстве проб питьевой воды. Его содержание составляет (о, 3+8,о) пг-лм в разных районах мира, за исключением небольшого числа районов с высоким содержанием Ra в воде.
Поступление с пищей в районах, Бк/сут. | |
с нормальным радиационным фоном. | (1,48+6,3)-Ю'2 |
с повышенным радиационным фоном. | >12,2−10'2 |
Концентрация, Бк/кг. | |
в костях. | 7,4-Ю‘2+2,8. |
в мягких тканях. | 2,7-Ю'3 |
Общее содержание в теле, Бк. | 0,55−51,8. |
Табл. 3. Поступление Ra в организм человека_.
Суточное поступление в организм человека 226Ra с пищей и водой составляет 2,3-ю12 Ки (2,3 пг-дн1), а потери с мочой и калом о, 8-ю-13 и 2,2*10'12 Ки. Независимо от химической формы соединения Ra при поступлении, 8о% поступившего в организм Ra накапливается в костной ткани человека. Довольно активно он накапливается в мозгу. Содержание Ra в организме человека зависит от района проживания и характера питания. Данные по условному человек}7 (в пг): содержание Ra в организме человека — 31, в скелете — 27; суточное поступление — 2,3. Радий быстро покидает кровеносное русло, но небольшие количества его длительно циркулируют в крови: через 14 лет после поступления Ra в крови циркулирует ~о, оз% элемента, содержащегося в организме.
В ранние сроки после введения заметные количества Ra находятся в мягких тканях. Однако уже через 1 сут концентрация Ra в костях на 1−2 порядка выше, чем в мягких тканях. При поступлении Ra в организм он отлагается на поверхности костей и в областях костной ткани с интенсивным обменом веществ. 226Ra и 228Ra распределяются по всем)' объём)7 минеральной кости, a 223Ra, —"Ra,Ra и 22?Ra — по поверхности кости во все периоды времени после отложения их в скелете. Выявлено два типа распределения Ra: образование участков интенсивного отложения — «горячих пятен» и сравнительно равномерное диффузное распределение. «Горячие пятна» содержат в 164−218 раз больше Ra на единиц)' костной массы, чем участки диффузного распределения.
226Ra выводится из скелета человека с Гб=17 л, из лёгких — 180 дн. Выведение Ra из организма происходит через ЖКТ. В течение 244−48 ч большая часть принятого с пищей Ra выводится с калом, с мочой (5%). Выведение Ra через почки ограничено из-за реабсорбции его в канальцах.
Радий не играет никакой биологической роли. Он опасен только в некоторых лабораториях, производствах и медицинских учреждениях. Его радиотоксичностоть намного сильнее химической, которая аналогична бариевой. Большие концентрации 226Ra в организме вредно действуют на животных и человека, вызывая болезненные изменения в виде остеопороза, самопроизвольных переломов, опухолей. Радиотоксическое действие Ra, попадающего в организм, имеет специфические особенности, связанные с сильно ионизирующим действием короткопробежных а-частиц, большим периодом полураспада, ярко выраженной органотропностью и длительной задержкой в организме. Максимально допустимое количество 226Ra, фиксированного в человеческом организме, *о, 1 мкг.
Радий — остеотропное вещество, с высокой токсичностью из-за своего свойства накапливаться в костной ткани (704−90%), которая обладает высокой радиочувствительностью, следствием чего являются лейкозы, лучевые остеосаркомы. Кроме того, Ra накапливается в лёгких и печени.
Характерным для поражения Ra является патология костного мозга. Отмечены случаи поражения кожи, ломкости ногтей, выпадения волос у людей, проработавших в контакте с Ra ~2 года. Наряду с жалобами на общую слабость, головную боль, головокружение, боли в сердце у лиц, контактирующих с Ra, возникают специфические боли в костях рук и ног, грудине, ребрах, иногда позвоночнике.
В отдаленные сроки после поражения Ra развиваются злокачественные новообразования. Остеосаркомы наблюдались при дозах 94−440 Гр, а карциномы при дозах 64−260 Гр. 22«Ra практически всю энергию распада отдаёт на костные структуры. При инкорпорации 226Ra значительные количества проникают в минеральные структуры костной ткани, где отсутствуют эндостальные клетки, вследствие чего основная доля энергии аизлучения из-за малого пробега а-частиц в тканях (40 мкм) не реализуется. Доза 22*Ra на эндостальные клетки в 9 раз больше, чем средняя доза на всю кость, в то время как при инкорпорации она составляет 2/3 среднего значения. При инкорпорации 226Ra остеосаркомы отсутствовали у людей, в скелете которых дозы были ниже 7 Гр. Минимальный период развития остеосарком при инкорпорации 226Ra при средних кумулятивных дозах 9 Гр для женщин и мужчин составляет 7 и 4 года соответственно Радий разрушает не только здоровые ткани, но убивает и злокачественные новообразования, излечивая рак кожи.
Для 223Ra, 224Ra группа радиационной опасности Б, МЗА = 3,7−104 Бк; для 226Ra, 228Ra группа радиационной опасности А, МЗА=з, 7*юз Бк. Допустимая концентрация Ra в воздухе не более ю мг/кмз или ю-11 г/мз. При такой концентрации в 1 мз происходит ~2 расп/с.
Изотоп. | Предельный уровень поступления, Бк/год. | Уровень вмешательства, Бк/л. |
226Ra. | 6.7-ю2 | 0.5. |
228 Ra. | 1.9*10*. | 0.2. |
В НРБ установлены следующие ограничения по содержанию изотопов радия в воде: __.
Работа с препаратами Ra требует принятия особых мер предосторожности. Она проводится в герметичных перчаточных боксах, исключающих утечку Rn. Неотложная помощь включает дезактивацию открытых участков кожи водой с мылом, каолиновой пастой с 20% цитратом натрия. Внутрь адсорбар или сернокислый барий 25:200.