Простые эфиры фенолов

Некоторые производные сложных органических оснований, содержащие остатки фосфорной и пирофосфорной кислот, играют исключительно важную роль в биохимии (см. гл. 25). Дело в том, что связь —Р—О—Р— очень реакционноспособна, при переносе каждой молекулы фосфорной кислоты, например от аденозинтрифосфата на другую молекулу, выделяется значительное количество энергии: около 42 кДж/моль. В биохимии такие… Читать ещё >
Простые эфиры фенолов (реферат, курсовая, диплом, контрольная)
Простые эфиры фенолов.
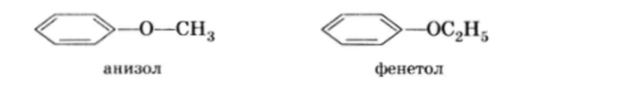
могут быть получены обычной реакцией алкилирования фенолята йодистым алкилом:

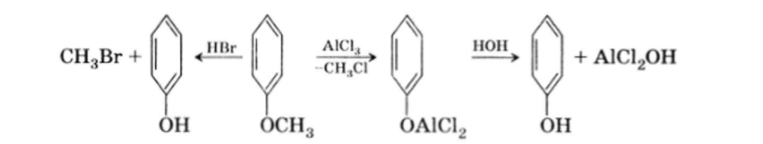
Простые эфиры фенолов, как и простые эфиры спиртов, мало реакционноспособные соединения, но разрыв связи С—О в них происходит все же несколько легче. Отщепление алкильной группы можно осуществить действием А1С1а или концентрированной НВг, расщепление проходит всегда с образованием фенола и ал кил галоген и да:
Этиленоксид
Формально этиленоксид Ы2С—СН2 представляет собой О.
внутренний эфир этиленгликоля НОСН2—СН2ОН. Получают его двумя способами:
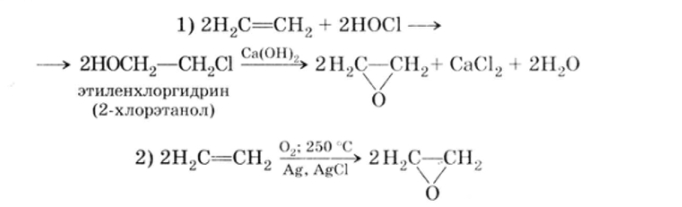
Этиленоксид — низкокипящее вещество (т. кип. +11 °С) с эфирным запахом. В отличие от ациклических простых эфиров он очень реакционноспособен. Это объясняется большой напряженностью цикла (как в циклопропане). Атака как нуклеофильных, так и электрофильных агентов приводит к разрыву связи С—О:

Другие циклические эфиры с ненапряженными циклами обладают очень малой реакционной способностью, как обычные простые эфиры.
Эфиры борной кислоты
Эфиры борной кислоты — триалкилбораты — получаются при нагревании борной кислоты и спиртов в присутствии серной кислоты:
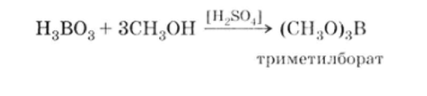
Как элемент III группы, бор имеет три валентных электрона, и, следовательно, в (К (){)В у бора не октет, а секстет электронов. Поэтому (R03)B легко присоединяют алкоксид-анион с образованием устойчивых солей:

Тем же объясняется и образование так называемых боратных комплексов с этиленгликолем, глицерином и другими полигидроксилсодержащими соединениями, у которых два соседних гидроксила находятся в цисположении:
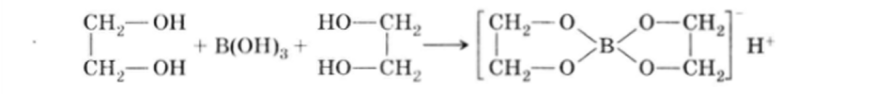
Образующийся эфир (боратный комплекс) ведет себя как сильная кислота. Эта реакция очень важна для установления конфигурации сахаров.
Эфиры борной кислоты, как, впрочем, и эфиры всех других неорганических кислот, гидролизуются под действием водных растворов щелочей:
(СНаО)3В + 3NaOH —* ЗСН8ОН + Na3B03
Эфиры серной кислоты
При взаимодействии концентрированной серной кислоты и спиртов можно получить кислые и полные эфиры:
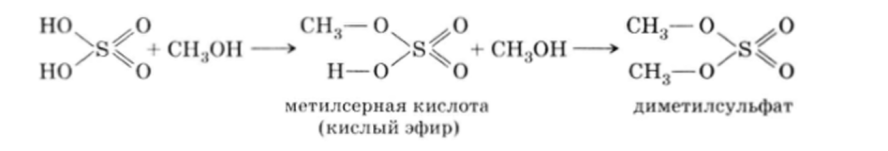
Одна из связей Н3С—О в диметилсульфате очень лабильна (реакционноспособна) к действию нуклеофильных агентов, и поэтому диметилсульфат широко применяется в качестве метилирующего агента:
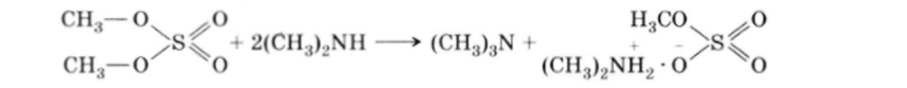
Диметилсульфат очень ядовит, и при работе с ним надо соблюдать крайнюю осторожность, особенно избегая попадания его на кожу.
Эфиры азотной и азотистой кислот
При действии на спирты смеси азотной и серной кислот легко образуются эфиры азотной кислоты, носящие общее название нитратов:
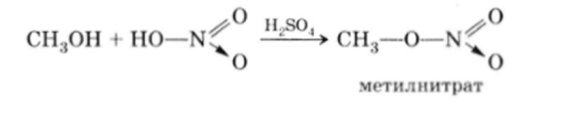
Сам нитроглицерин очень легко взрывается, поэтому применяется не в чистом виле, а в смеси с кизельгуром (пористый Si02) или другими пористыми веществами, такие смеси называются динамитами (открытие свойств динамитов принадлежит шведскому инженеру Нобелю, 1866).
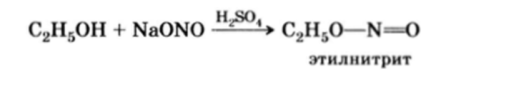
Эфиры азотистой кислоты называются нитритами, они способны понижать кровяное давление:
Все эфиры азотной кислоты сильно взрывчаты, особенно это относится к эфирам многоатомных спиртов:
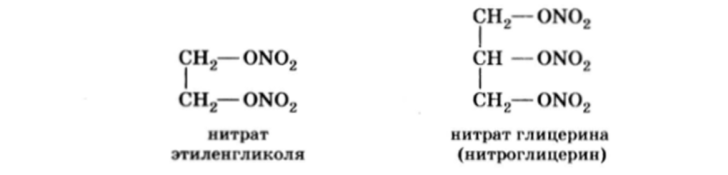
Эфиры кислородных кислот фосфора
Эфиры фосфористой кислоты — фосфиты — легко получаются при взаимодействии РС13 с алкоголятами:
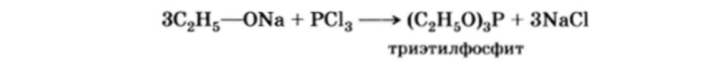
Эфиры фосфорной кислоты — фосфаты — получают действием алкоголятов на оксид-трихлорид фосфора:

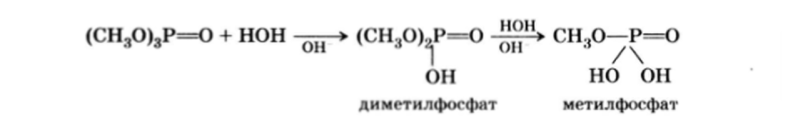
Постепенным гидролизом можно получать и кислые эфиры:
Фосфорная кислота способна к ангидридизации с образованием пирофосфорной кислоты:
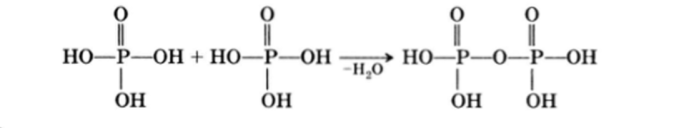
Некоторые производные сложных органических оснований, содержащие остатки фосфорной и пирофосфорной кислот, играют исключительно важную роль в биохимии (см. гл. 25). Дело в том, что связь —Р—О—Р— очень реакционноспособна, при переносе каждой молекулы фосфорной кислоты, например от аденозинтрифосфата на другую молекулу, выделяется значительное количество энергии: около 42 кДж/моль. В биохимии такие связи называются макроэргическими связями:
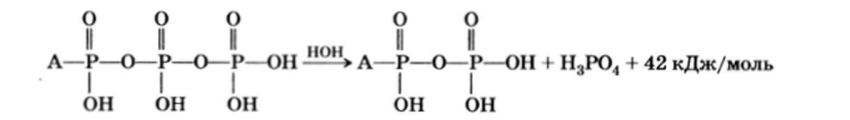
(где, А — остаток аденозина — см. гл. 25, разд. 6).
Считается, что такого рода «аномалии» связаны с так называемым отрицательным резонансом. Этот не очень удачный, но применяемый в биохимии термин можно объяснить следующим образом.
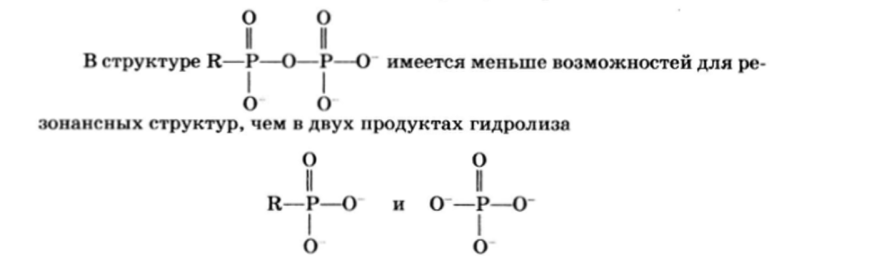
и, следовательно, продукты гидролиза более стабильны, чем исходное соединение (см. гл. 2, разд. 3).