Производство неорганических соединений

На обогатительной фабрике флотации подвергается руда, содержащая 1,3% меди. При флотации 1 т исходной руды получится 110,5 кг концентрата, содержащего 9,6% меди. Определите выход концентрата, степень извлечения и степень обогащения. В этом разделе при решение задач используют следующие понятия: выход продукта, расчет состава руды, возможность самопроизвольного протекания реакции получения… Читать ещё >
Производство неорганических соединений (реферат, курсовая, диплом, контрольная)
Металлургия
Металлургия — это наука о промышленных способах получения металлов из природного сырья. Металлургией также называю металлургическую промышленность. Сырьем в производстве металлов является металлические руды. За исключением небольшого числа металлов находящихся в природе в виде химических соединений входящих в состав металлических руд. Основной задачей металлургической промышленности является получение металлов из руд. Для этого руду подготавливают, подвергают вторичной обработке и процессу восстановления.
Задачи, которые приводятся в этом разделе являются расчетными задачами по уравнениям химических реакций. При решении задач используют основные законы и формулы химии, а также формулы которые рассматривались в предыдущих разделах (выход продукта, интенсивность, производительность и т. д.).
Одной из важнейших задач химической технологии является обогащение сырья. Для этого применяют метод флотации, который основан на различной смачиваемости водой минералов.
Выход концентрата (Вк) называется процентное отношение веса полученного концентрата к весу взятой руды.
Степень извлечения (Си) называется процентное отношение веса извлеченного элемента в концентрате к его весу в руде.
Степенью обогащения (Со) называется отношение процентного содержания элемента в концентрате к содержанию его в исходной руде.
В этом разделе при решение задач используют следующие понятия: выход продукта, расчет состава руды, возможность самопроизвольного протекания реакции получения металла, которые подробно описываются в других разделах.
Примеры решения задач.
1. Рассчитать минимальный расход магния для удаления сурьмы из 10 т чернового свинца, в котором сурьма составляет 0,5% массы. Сурьма выделяется из сплава в составе соединения Мg3Sb2
Решение:
Составим первое уравнение масса магния, добавленного в черновой сплав, равна массе магния в выделившемся из сплава соединении Mg3Sb2. Запишем второе уравнение, полагая, что масса сурьмы, содержащейся в 10 т чернового сплава, равна массе сурьмы и образовавшемся соединении Мg3Sb2.
m (Mg) = m (Mg3Sb2)*(3*M (Mg)/M (Mg3Sb2).
10*0,005 = m (Mg3Sb2)*(2*M (Sb)/M (Mg3Sb2).
Или.
m (Mg) = m (Mg3Sb2)*(3*24)/316.
0,05 = m (Mg3Sb2)*(2*122/316).
Для решения системы уравнении разделим правую и левую части первого уравнения на соответствующие части второго и обозначая (Мg) через х, получим:
x/0,05=24*3/122*2, x=0,0148.
Ответ. Минимальный расход магния— 14,8 кг.
2. На обогатительной фабрике флотации подвергается руда, содержащая 1,3% меди. При флотации 1 т исходной руды получится 110,5 кг концентрата, содержащего 9,6% меди. Определите выход концентрата, степень извлечения и степень обогащения.
Решение.
1. Вк=.
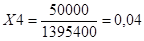
- 2. Для вычисления Си рассуждаем так
- а) в 100 кг исходной руды содержится 1,3 кг меди
в 1000 кг ————————————————— х кг меди х= 13 кг меди б) в 100 кг концентрата содержится 9,6 кг меди в 110,5 кг ————————————————— х кг меди х= 10,6 кг меди.
Следовательно, степень извлечения будет равна.
Си=.
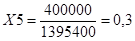
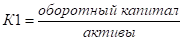
3. Со=раза.
Ответ Вк=11,05%, Си=81,5%, Со=7,4 раза.
Примеры решения задач.
- 1. Имеется титановая руда, состоящая из минералов рутила, перовскита и пустой породы. Массовая доля ТiО2 в этих минералах составляет соответственно 97% и 59%. Вычислить массовые доли названных выше минералов в руде, если известно, что содержание титана равно 27% от массы руды, а пустой породы — 38%.
- 2. Для легирования стали, требуется внести в расплав титан, чтобы его массовая доля составила 0,12%. Какую массу сплава ферротитана надо добавить к расплаву стали массой 500 кг, если массовые доли металлов в ферротитане составляют: титана — 30%, железа — 70%
- 3. Некоторая порода состоит из минералов сильвинита (KCl), каинита (MgSO4*KCl*3H2О) и карналлита (MgCl2*KCl*6H2О). Массовая доля калия в породе составляет 18%, а примесей (не содержащих калия и магния) — 12%. Вычислите возможную массу магния в 100 кг породы.
- 4. При обогащение 10 т медной сульфидной руды, содержащей 1,5% меди, получено 400 кг концентрата, содержащего 30% меди. Определить степень извлечения и степень концентрации.
- 5. При флотации 5 т цинковой руды, содержащего 3% цинка, получено 340 кг концентрата, содержащего 22% цинка. Определите выход концентрата, степень извлечения и степень концентрации.
- 6. Восстанавливая углем соединение Fe (CrO2)2 (хромистый железняк), получают сплав феррохром, используемый в металлургии. Определите массовую долю хрома в этом сплаве, считая, что других компонентов, кроме железа и хрома, он не содержит.
- 7. Железная руда имеет состав: магнетит Fе3О4 (массовая доля 55%), ильменит FеТiО3 (массовая доля 15%) и другие вещества, не содержащие железо и титан. Какую массу железа и титана можно получить из такой руды массой 300 кг?
- 8. Из медной руды массой 16 т, содержащей халькозин Cu2S и вещества, не содержащие медь, получили черновой металл массой 650 кг. Определите массовые доли меди и халькозина в руде, если массовая доля меди в черновом металле составляет 98,46%.
- 9. Для удаления висмута из черного свинца к расплавленному металлу добавляют сплав Pb — Ca, массовая доля кальция в котором составляет 0,03. Рассчитать теоретический расход сплава Pb — Ca для удаления висмута из 100 т чернового свинца, массовая доля висмута в котором равна 0,001. Висмут выделятся из сплава в составе соединения Ca3Bi2.
- 10. Медная руда содержит CuCO3*Cu (OH)2 и азурит 2CuCO3*Cu (OH)2 Какую массу меди можно получить из руды массой 5 т, если массовая доля малахита 8%, азурита 3,6%. Определите массовую долю меди в руде.