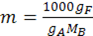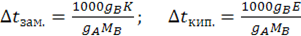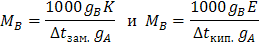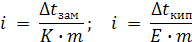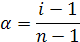Математическое выражение второго закона Рауля имеет вид:
где К — криоскопическая константа, град/моль, Е? эбулиоскопическая константа, град/моль.
m — моляльная концентрация растворенного вещества.
Согласно второму закону Рауля: понижение температуры замерзания и повышение температуры кипения растворов прямо пропорционально моляльной концентрации неэлектролита и не зависит от его природы.
Определяя экспериментально? tзам и? tкип растворов берут произвольные небольшие навески растворённого вещества В — gB и растворителя, А — gA. Тогда моляльная концентрация раствора равна:
И.
Из приведенных формул на основе второго закона Рауля можно определить молярную массу растворенного вещества МB, например:
При m = 1, Следовательно, К характеризует моляльное? tзам. раствора, Е — моляльное? tкип. раствора.
К и Е — величины условные (рассчитаны для моляльного раствора по данным разбавленных растворов). Обе константы характерны для данного растворителя, они не зависят от природы и концентрации растворенного вещества при стандартных условиях, табулированы в справочниках. Могут быть рассчитаны по формулам:
Криоскопия — метод, основанный на измерении? tзам. растворов. Служит в биологии и химии для определения суммарной концентрации клеточного сока растений, концентрации почвенных растворов, молярной массы растворенного вещества МB и т. д.
Эбулиоскопия — метод, основанный на измерении? tкип. растворов, также используется на практике для вышеуказанных целей.
Первый и второй законы Рауля справедливы для разбавленных растворов неэлектролитов. В случае электролитов число частиц в растворе за счет электролитической диссоциации резко возрастает и в расчетные формулы следует вводить поправки.
В случае растворов электролитов уравнение второго закона Рауля имеет вид:
;
где i — изотонический коэффициент.
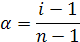
n- число ионов электролита в растворе, б — степень диссоциации электролита.
;