Соединения щелочных металлов

Сольватацию катионов щелочных металлов следует рассматривать с двух позиций: во-первых, необходимо иметь в виду количество молекул растворителя, непосредственно связанных с катионом (первая гидратная оболочка), во-вторых, сольватационное число, которое определяется как полное число молекул, на которое ион оказывает заметное удерживающее влияние. Наибольшее значение имеет строение первой гидратной… Читать ещё >
Соединения щелочных металлов (реферат, курсовая, диплом, контрольная)
Большинство соединений щелочных металлов относятся к ионному типу. Однозарядные положительные ионы этих металлов имеют на наружном уровне восемь электронов (у Na, К, Rb, Cs и Fr), а у лития — два электрона. Эти ионы обладают малым поляризующим действием и незначительной поляризуемостью.
Соединения щелочных металлов, как правило, бесцветны, термически устойчивы и в большинстве своем хорошо растворимы в воде. У лития в связи с особенностями иона (конфигурация Is2) некоторые соединения (LiOII, LiF, Li2C03, Li3P04 и др.) плохо растворимы в воде. Ионы щелочных металлов практически лишены окислительных свойств.
Для катионов щелочных металлов, имеющих восьмиэлектронную внешнюю оболочку, из-за очень незначительного поляризующего действия не характерны комплексные соединения. Даже аквакомплексы малоустойчивы, поэтому большинство солей щелочных металлов не образует кристаллогидратов. Такие кристаллогидраты, как Na2S04 • 10Н2О и Na2C03— 10Н2О, являются тектогидратами, т. е. они имеют структуру, которая стабилизируется за счет стягивающего действия электростатически взаимодействующих ионов противоположного знака.
Ион лития, имеющий наименьший по сравнению с Na+, К Rb+, Cs+ и Fr+ радиус, но наибольшее поляризующее действие, образует комплексные соединения с координационным числом 4, например [Li (H20)J~.
Сольватацию катионов щелочных металлов следует рассматривать с двух позиций: во-первых, необходимо иметь в виду количество молекул растворителя, непосредственно связанных с катионом (первая гидратная оболочка), во-вторых, сольватационное число, которое определяется как полное число молекул, на которое ион оказывает заметное удерживающее влияние. Наибольшее значение имеет строение первой гидратной оболочки.
Для иона Li+ характерна гидратная оболочка из четырех молекул воды, создающих тетраэдрическое окружение. Ионы Na+ и 1C тоже координируют четыре молекулы в первой гидратной оболочке, a Rb+ и Cs+ координируют шесть молекул воды. Однако электростатические силы, действующие между первой гидратной оболочкой и последующими, ограничивают гидратацию. Размеры этой вторичной гидратной оболочки изменяются обратно пропорционально радиусу катиона. Поэтому с увеличением кристаллических радиусов гидратационное число, радиусы гидратированного иона и энергия гидратации уменьшаются. При уменьшении радиуса гидратированного иона возрастает его подвижность.
Оксиды и гидроксиды. Оксиды щелочных металлов получаются либо путем непосредственного взаимодействия металла с кислородом (Li20), либо косвенно, например восстановлением пероксида металла этим же металлом:
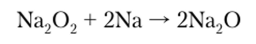
а для калия, рубидия и цезия исходят из надпероксидов (сунероксидов):
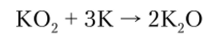
Соединения Li20, Na20 и К20 — вещества белого цвета, Rb20 — желтого, a Cs20 — оранжевого.
Оксиды щелочных металлов — реакционноспособные вещества; энергично взаимодействуя с водой, образуют соответствующие гидроксиды:
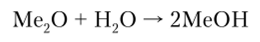
Активность оксидов усиливается в ряду Li., О — Na20 — К20 — Rb20 — Cs20, о чем можно судить по изменению значений энергии Гиббса в реакциях образования гидроксидов: для LiOLI — 46,8 кДж/моль, NaOH — 77,6 кДж/моль, КОН — 102,4 кДж/моль, RbOH — 104,5 кДж/моль, CsOH — 104,5 кДж/моль. Практического значения оксиды щелочных металлов не имеют.
Гидроксиды щелочных металлов LiOH, NaOH, КОН, RbOH и CsOH — твердые кристаллические вещества белого цвета. В природе эти соединения не встречаются, и поэтому их получают электролизом водных растворов хлоридов. Этот метод лежит в основе промышленного получения гидроксидов натрия и калия:
• электролит:
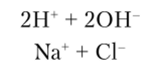
• катод:
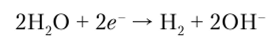
• анод:
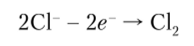
• прикатодное пространство:
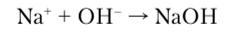
Гидроксид натрия получают также известковым способом (каустификация соды), т.с. обработкой Na., C03 гашеной известью:
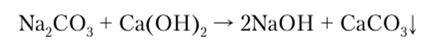
Поэтому NaOH в технике называют каустической содой.
Часто для лабораторных целей, когда требуется получить особо чистые гидроксиды, используют реакцию взаимодействия металла с водой, или гидролиз соответствующего алкоголята:
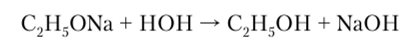
По растворимости в воде LiOH уступает остальным гидроксидам. Процесс растворения гидроксидов щелочных металлов — экзотермический. Водные растворы щелочных металлов сильно диссоциированны, но как электролит LiOH слабее остальных. Ввиду сильно выраженных основных свойств их называют щелочами.
LiOH при прокаливании разлагается, чем и отличается от остальных гидроксидов щелочных металлов:
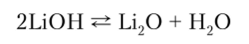
Твердые гидроксиды и их водные растворы поглощают СО., из атмосферы.
Соли щелочных металлов. Соли этих металлов известны практически для всех кислот. Как правило, они представляют собой бесцветные кристаллические вещества с преобладанием ионного типа связи. Цвет окрашенных солей обусловлен анионом, за исключением тех случаев, когда окраска вызвана дефектом решетки под воздействием некоторых внешних факторов (например, облучения).
Соединения лития по своим свойствам отличаются от аналогичных соединений других щелочных металлов, но напоминают соединения Mg2 Такая аномалия в свойствах соединений лития объясняется прежде всего особенностями строения иона Li+ и его влиянием на энергию кристаллической решетки (см. гл. 5).
Растворимость солей лития сходна с растворимостью солей Mg2+, например, LiF плохо растворим в воде (0,27 г в 100 г Н20 при 18°С). Растворимость этой соли понижается при добавлении к раствору NH4F, LiCl, LiBr, Lil и LiCl ()4 растворимы в спирте, ацетоне.
Карбонат лития при нагревании распадается на 1л20 и С09 значительно легче, чем карбонаты других щелочных металлов.
Все соли щелочных металлов характеризуются высокими температурами плавления, электрической проводимостью растворов и расплавов.
Соли щелочных металлов, образованные галогенид-анионами, обычно редко гидратируются, так как энергия гидратации ионов мала и недостаточна для компенсации затраты энергии, расходуемой для разрушения решетки. Только ион лития имеет высокую энергию гидратации, поэтому в его твердых солях он часто гидратирован, отличаясь тем самым от аналогичных солей других щелочных металлов. Из солей сильных кислот наибольшей растворимостью обладают соли лития, тогда как литиевые соли слабых кислот имеют более низкую растворимость, чем у остальных щелочных металлов.
В водных растворах соли слабых кислот подвергаются гидролизу, повышая концентрацию ионов ОН в растворе и создавая щелочную реакцию:
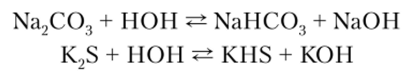
Летучие соединения щелочных металлов, а также пары самих металлов окрашивают бесцветное пламя в характерные цвета: литий — карминовокрасный, натрий — желтый, калий — фиолетовый, что широко применяется в аналитической химии и технике.
Большое значение для распознавания катионов щелочных металлов имеют реакции осаждения. Так, Li+ и Na" могут быть осаждены метанольным раствором 4,4'-диметиламинодифенилметана. Как правило, с увеличением радиуса иона в ряду щелочных металлов число нерастворимых солей увеличивается. Например, смешанные уранилацетаты натрия и цинка [NaZn (U09):i(CH:iC00)9-6H., 0] или натрия и магния почти количественно осаждаются из разбавленных растворов уксусной кислоты. Соли более тяжелых ионов — К+, Rb+ и Cs+ с такими анионами, как С104; [PtClG]2-; [Co (N02)g]3_, сравнительно плохо растворимы в воде, поэтому их и используют для аналитических определений.
Щелочные металлы находят широкое применение. Натрий в больших количествах используют в промышленном органическом синтезе (получение красителей), в производстве синтетических моющих средств, в производстве тетраэтилсвинца. Как твердый, так и жидкий натрий вследствие высокой теплопроводности применяют в качестве теплоносителя (например, в атомных реакторах).