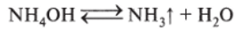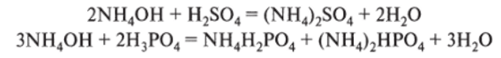Другие работы

Чтобы задать функцию, нужно указать способ, с помощью которого для каждого значения аргумента можно найти соответствующее значение функции. Наиболее употребительным является способ задания функции с помощью формулы у=f (x), где f (x) — с переменной х. В таком случае говорят, что функция задана формулой или что функция задана аналитически. Пусть n — произвольное четное число, большее двух: 4,6,8…
Реферат 
Геометрически это означает, что нужно найти кривую y = F (x) некоторого определенного типа, проходящую через заданную систему точек Mi (xi, yi) для i =. Полученная таким образом интерполяционная формула y = F (x) обычно используется для вычисления значений исходной функции f (x) для значений аргумента x, отличных от узлов интерполяции. Такая операция называется интерполированием функции f (x). При…
Реферат 
Действие сериновых протеаз, таких как трипсин, химотрипсин и тромбин, — пример механизма ковалентного катализа, когда ковалентная связь образуется между субстратом и аминокислотным остатком серина активного центра фермента. Термин «сериновые протеазы» связан с тем, что аминокислотный остаток серина входит в состав активного центра всех этих ферментов и участвует непосредственно в катализе…
Реферат 
Анализ данных выражений показывает, что коэффициент прохождения D существенно зависит от массы т и разности энергий UQ — ?, так как квадрат гиперболического синуса резко увеличивается с увеличением аргумента. При некотором значении энергии Е увеличение высоты (U0) и ширины (d) барьера уменьшает коэффициент прохождения. Для заметного туннельного эффекта должно соблюдаться неравенство…
Реферат 
Свойства ферромагнитных веществ связаны с наличием спонтанно (самопроизвольно) намагниченных участков (доменов). В отсутствие внешнего магнитного поля вектора намагниченности доменов ориентированы хаотично. При появлении внешнего магнитного поля и его возрастании происходит перестройка доменов вдоль поля. Состояние насыщения намагничивания означает, что векторы магнитных моментов всех доменов…
Реферат 
При нормальном состоянии изоляции всех элементов гирлянды или колонки штыревых изоляторов на каждый элемент приходится определенная величина рабочего напряжения. Если же какой-либо элемент пробит, то напряжение на нем будет равно нулю, а если изоляция понижена, то меньше нормального. На остальных элементах при этом напряжение превысит нормальную величину. Построив кривую распределения напряжения…
Реферат 
Очевидная ошибка Лоренца заключается в том, что он, скорей всего непроизвольно, не обратил внимания на существование области определения коэффициента пропорциональности в своих преобразованиях. Эта ошибка, не замеченная Пуанкаре, публично подтвердившим преобразования Лоренца, и послужила причиной появления в физике стараниями Эйнштейна недоразумения, именуемого «специальная теория…
Реферат 
Основную относительную погрешность рассчитываем для максимального входного сопротивления, т. к на четвертом пределе будет наибольшая погрешность. Отношение токов определим по формуле (1.14). В качестве источника питания омметра выберем никель-металл-гидридный аккумулятор с артикулом ACCU-BPH12 с емкостью 2100 мАч, которого хватит примерно на 10 часов непрерывной работы прибора. Данная схема имеет…
Реферат 
За последние 100 лет средняя температура на планете выросла на 0,6 °С. Для суточного колебания температуры эта величина ничтожна, но для глобальных климатических характеристик это очень много. За последние 20 лет скорость изменения температуры увеличилась в 20 раз. Максимальное потепление зафиксировано в самых холодных регионах, где сконцентрированы основные запаса льда, а именно: на Аляске…
Реферат 
Классификация ДВС Как было выше сказано, в качестве энергетических установок автомобилей наибольшее распространение поучили ДВС, в которых процесс сгорания топлива с выделением теплоты и превращением ее в механическую работу происходит непосредственно в цилиндрах. Но в большинстве современных автомобилей установлены двигатели внутреннего сгорания, которые классифицируются по различным признакам…
Реферат 
Важнейшие природные минералы серы: FeS2 — железный колчедан или пирит, ZnS — цинковая обманка или сфалерит (вюрцит), PbS — свинцовый блеск или галенит, HgS — киноварь, Sb2S3 — антимонит. Кроме того, сера присутствует в нефти, природном угле, природных газах и сланцах. Сера — шестой элемент по содержанию в природных водах, встречается в основном в виде сульфат-иона и обусловливает «постоянную…
Реферат 
Изотопный анализ кислорода проводился в ДВГИ ДВО РАН. Как известно, кислород присутствует в опалах в разных соединениях. Большая его часть входит в структуру кремнекислородных тетраэдров, однако он присутствует и в кристаллизационной, и в поровой воде, которой насыщен опал. Кислород воды способен к изотопному обмену с метеорными водами в ходе процессов, происходящих уже после формирования опалов…
Реферат 
Они образуются при обезвоживании ортофосфорной кислоты. Все конденсированные фосфорные кислоты содержат в качестве структурной единицы ортофосфатный тетраэдр РО4, который может иметь один, два или три общих атома кислорода с соседними тетраэдрами. Соединяясь, тетраэдры образуют цепи, циклы и разветвленные структуры. По структуре молекул конденсированные фосфорные кислоты делят па полифосфориые…
Реферат 
Какую массу воды следует прибавить к 200 мл 30%-ного раствора гидроксида калия плотностью 1,33 г/см3, чтобы получить раствор с массовой долей КОН 10% и с = 1,08 г/см3? Рассчитайте: См, Сн полученного раствора КОН. Какую массу раствора хлорида кальция с массовой долей 22% надо прибавить к воде массой 500 г для получения раствора с массовой долей соли 12% и плотностью 1,102 г/см3 Рассчитайте См…
Реферат 
Так, например, изоморфны (эквивалентны) все конечные, следовательно, дискретные множества с равным количеством элементов. Для таких множеств изоморфизм устанавливается простым перечислением соответствующих пар элементов, начиная, например, с наименьших. Вопрос любознательному Читателю: можно ли доказать, что для каждого дискретного бесконечного множества М можно выбрать порядок р такой, что…
Реферат