Элементы 2-й группы.
Кальций

В кристаллической решетке металлического кальция связь между атомами осуществляется не одним, как у натрия, а двумя электронами (см. параграф 6.4), что определяет и более высокую температуру плавления кальция (842°С), и большую твердость. Константа равновесия равна единице при -1100 К, и процесс легко идет при 800—900°С. Оксид кальция термически чрезвычайно устойчив, температура его плавления… Читать ещё >
Элементы 2-й группы. Кальций (реферат, курсовая, диплом, контрольная)
В атомах элементов 2-й группы на ns-АО находится два электрона, т. е. она заполнена полностью. Исходя из этого можно ожидать повышенной инертности элементов, однако наличие близко лежащих пр-АО позволяет электронам легко переходить на гибридные sp-орбитали и участвовать в образовании двух связей. Такой переход характерен для первого элемента группы — бериллия и, отчасти, для магния. Остальные элементы ковалентных связей практически не образуют и в своих соединениях находятся исключительно в форме двухзарядных катионов М2+. Эти элементы — Са, Sr, Ва — объединены общим названием щелочноземельные металлы. Наиболее важным из них является кальций.
По содержанию в земной коре кальций занимает третье место среди металлов после алюминия и железа. Основное его количество сосредоточено в форме кальцита СаС03 (мел, мрамор, известняк).
Получают кальций, как и другие щелочноземельные металлы, электролизом расплавленного хлорида. В свободном состоянии кальций — блестящий серебристый металл, быстро тускнеющий на воздухе из-за реакций с кислородом и влагой:
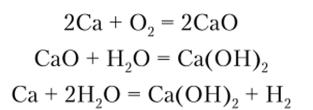
Хранят кальций, подобно натрию, без доступа воздуха.
Кальций является важным биогенным элементом — на основе СаС03 строится скелет беспозвоночных, а на основе Са3(Р04)2 — позвоночных животных.
В кристаллической решетке металлического кальция связь между атомами осуществляется не одним, как у натрия, а двумя электронами (см. параграф 6.4), что определяет и более высокую температуру плавления кальция (842°С), и большую твердость.
В своих соединениях кальций существует исключительно в состоянии Са2+. Энергия ионных кристаллических решеток, образованных двухзарядными катионами, велика и не всегда перекрывается энергией гидратации ионов. Поэтому многие соли кальция тугоплавки и малорастворимы. К их числу относятся СаС03, CaF2, Са3(Р04)2.
Реакционная способность кальция очень велика. Подобно натрию, он уже при обычных условиях легко реагирует с водой и некоторыми неметаллами — кислородом, галогенами.
Оксид кальция — негашеную известь — получают в громадных количествах разложением карбоната.
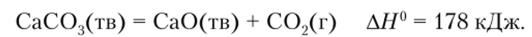
Константа равновесия равна единице при -1100 К, и процесс легко идет при 800—900°С. Оксид кальция термически чрезвычайно устойчив, температура его плавления превышает 2500 °C. С водой он легко и экзотермически реагирует, образуя гидроксид:
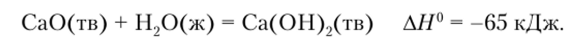
Хотя растворимость Са (ОН)2 невелика (—0,02 моль/л), его растворы имеют отчетливую щелочную реакцию (в насыщенном растворе pH = 12). Гидроксид кальция — гашеная известь — широко применяется в строительстве в качестве вяжущего материала. Суспензия Са (ОН)2 в воде — известковое молоко — используется в промышленности как наиболее дешевая щелочь.
Кальций легко реагирует не только с кислородом, но и горит в водороде, образуя гидрид:
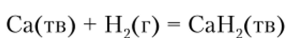
Соли кальция с однозарядными анионами — С1, В г, I, N03 — хорошо растворимы, но CaF2 (минерал флюорит) практически нерастворим.
Важное значение имеет равновесие.
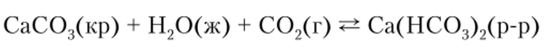
В избытке С02 образуется более растворимый гидрокарбонат, но уменьшение парциального давления С02 ведет к сдвигу равновесия влево и выделению нерастворимого карбоната. Это равновесие в значительной степени определяет жесткость воды, лежит в основе карстовых явлений, позволяет кораллам создавать острова в океане, а птицам окружать яйца защитной скорлупой.
Более тяжелые, чем кальций, элементы 2-й группы — Sr, Ва, Ra — подобны кальцию, но химически активнее его. Более легкие — Be и Mg — заметно отличаются большей склонностью к образованию ковалентных связей. В частности, Mg, подобно Li, образует большое число магнийорганических соединений, например (C2H5)2Mg. Оксид бериллия практически не реагирует с водой, и поверхностная пленка ВеО защищает металл (подобно алюминию) от дальнейшего окисления. Сплавы на основе бериллия и магния используются как очень легкие конструкционные материалы.
Соединения бериллия и бария крайне ядовиты!
Резюме
Свойства элементов, в атомах которых присутствуют только s-валентные электроны, конечно, отличаются от свойств остальных элементов. Необходимо понимать, почему свойства водорода так резко отличаются от свойств остальных элементов группы и как меняются свойства элементов, но мере увеличения заряда ядра при движении по группе сверху вниз.
Практикум
Вопросы для самоконтроля
- 1. Если гидридный анион взаимодействует с кислым раствором, то реакцию можно записать так: Н + Н+ = Н2|. А как записать его реакцию со щелочным раствором?
- 2. Жесткая вода содержит растворенный гидрокарбонат кальция. Для ее «смягчения» к пей добавляют немного соды, и кальций «уходит» из раствора. Что происходит?
Аналитические задания
- 1. Приведите примеры реакций, в которых молекулярный водород Н2 выступает: а) в роли восстановителя; б) в роли окислителя.
- 2. При взаимодействии с простыми веществами вода может выступать либо в роли окислителя, либо в роли восстановителя. Напишите реакции взаимодействия воды с натрием и хлором.
3. Равновесие карбонат — гидрокарбонат кальция играет важную роль в геологических и биологических процессах. Рассмотрите факторы, влияющие на смещение этого равновесия.
Задачи для самостоятельного решения.
- 1. Исходя из электронного строения молекулы воды покажите, почему только в случае воды может существовать общая система водородных связей.
- 2. В ионе Na+ валентные электроны отсутствуют. Используя метод ВС, покажите, за счет каких орбиталей координационное число иона натрия может достигать шести.
- 3. В промышленном производстве соды из раствора осаждается гидрокарбонат натрия, который при прокаливании (кальцинации) переходит в карбонат. Напишите реакцию кальцинации соды.