Оксиды.
Общая и неорганическая химия для медиков и фармацевтов

По способности образовывать соли с кислотами или основаниями при обычных температурах оксиды делятся на солеобразующие (MgO, ZnO, S02) и несолеобразующие, или безразличные (СО, NO, N20). В свою очередь солеобразующие оксиды подразделяют на основные, кислотные и амфотерные. Кислотными называются оксиды, которым соответствуют гидроксиды кислотного характера (кислоты) и которые образуют соли… Читать ещё >
Оксиды. Общая и неорганическая химия для медиков и фармацевтов (реферат, курсовая, диплом, контрольная)
Наиболее простым по составу классом неорганических соединений являются оксиды.
Оксиды — это химические соединения, состоящие из двух элементов, одним из которых является кислород в степени окисления (-2). Из;
(c)вестны и другие бинарные соединения кислорода: пероксиды (Н202, Na202), надпероксиды (К02) и озониды (К03), в которых атом кислорода имеет формальные степени окисления (-1), (-½) и (-1/3) соответственно.
Если элемент образует с кислородом одно соединение, то его называют оксидом соответствующего элемента: Li20 — оксид лития, MgO — оксид магния. Если элемент образует несколько оксидов, то после названия элемента указывается степень его окисления (римской цифрой в скобках): S02 — оксид серы (1У), S03 — оксид серы (У1). Возможно употребление систематической номенклатуры, требующей полного отражения состава соединения: Р205 — дифосфор пентаоксид, Мп207 — димарганец гептаоксид. У многих оксидов существуют и тривиальные названия: S02 — сернистый газ, СО — угарный газ.
По способности образовывать соли с кислотами или основаниями при обычных температурах оксиды делятся на солеобразующие (MgO, ZnO, S02) и несолеобразующие, или безразличные (СО, NO, N20). В свою очередь солеобразующие оксиды подразделяют на основные, кислотные и амфотерные.
Основными называются оксиды, которым соответствуют гидроксиды основного характера (основания) и которые образуют соли при взаимодействии с кислотами или кислотными оксидами. Все они являются оксидами металлов (Na20, MgO, Ag20):
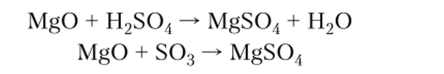
Большинство основных оксидов не растворяются в воде и нс взаимодействуют с ней. Соответствующие им основания получают косвенным путем.
Кислотными называются оксиды, которым соответствуют гидроксиды кислотного характера (кислоты) и которые образуют соли с основаниями или основными оксидами. Это оксиды неметаллов (S02, С02, Р205), а также оксиды металлов с высокими степенями окисления (СгОя, Мп207):
Большинство кислотных оксидов растворяется в воде и взаимодействует с ней с образованием кислородсодержащих кислот, поэтому их часто называют ангидридами соответствующих кислот:
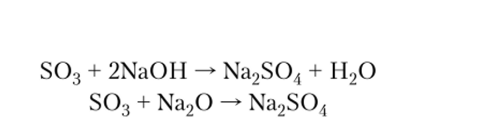
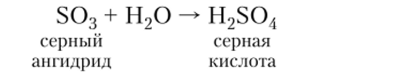
Некоторые оксиды в зависимости от условий могут присоединять разное число молекул воды, образуя метаи ортокислоты. Способность образовывать метаили ортогидроксиды зависит от радиуса атома: чем меньше радиус, тем устойчивее метаформа. Например, радиус атома N меньше радиуса атома Р, поэтому при гидратации N205 образуется только один гидроксид:

Кислотные оксиды, содержащие атом элемента в промежуточной степени окисления (например, N02), при взаимодействии с водой часто образуют смесь двух кислот, а с основаниями или основными оксидами — смесь соответствующих солей:
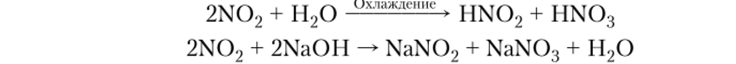
Амфотерными называются оксиды, образующие соли и с кислотами, и с основаниями. Такими оксидами являются оксиды металлов (BeO, ZnO, РЬО, А1203, Сг203, Fe203).
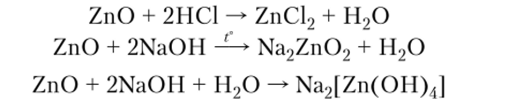
Физические свойства. Все основные и амфотерные оксиды являются твердыми веществами, имеющими ионную (для s-металлов) или ионную со значительной ковалентностью (для р- и d-металлов) кристаллическую решетку и вследствие этого высокие температуры плавления. Кислотные оксиды, как правило, имеют молекулярное строение, поэтому их температуры плавления и кипения невысоки: С02 и S02 — газы, S03 — летучая жидкость, Р205 — твердое вещество с относительно невысокой температурой плавления. Исключение составляет Si02, который вследствие своего атомного строения имеет высокую температуру плавления.
Получают оксиды следующими способами.
1. Взаимодействие простых веществ с кислородом:
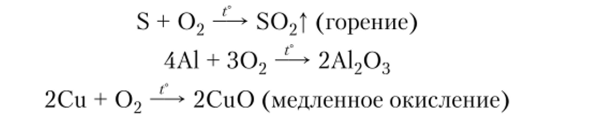
2. Окисление сложных веществ кислородом:
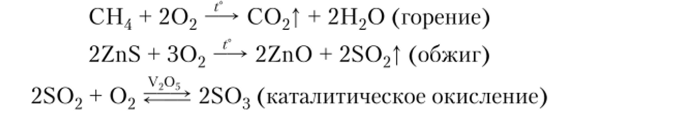
3. Окисление простых и сложных веществ другими окислителями:
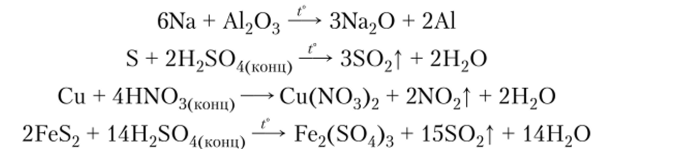
4. Термическое разложение сложных веществ (солей, оснований, кислот):
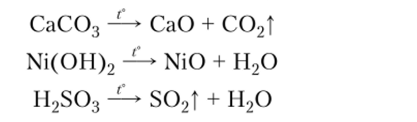
5. Взаимодействие солей неустойчивых кислородсодержащих кислот с сильными кислотами и с кислотными или амфотерными оксидами:

6. Восстановление высших оксидов до низших:
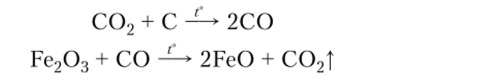
Рассмотрим химические свойства кислотных оксидов.
- 1. Большинство кислотных оксидов реагируют с водой с образованием кислородсодержащих кислот (см. определение кислотных оксидов). Немногие кислотные оксиды, например Si02, не растворяются в воде и с ней не взаимодействуют. Соответствующие им кислоты получают косвенным путем.
- 2. Кислотные оксиды взаимодействуют с основными и амфотерными оксидами с образованием солей:
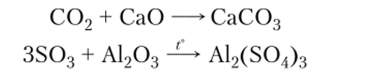
3. Все кислотные оксиды реагируют со щелочами с образованием соли и воды: 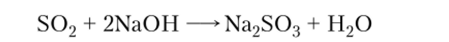
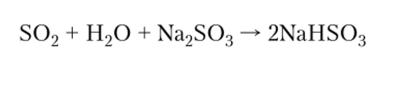
Следует отметить, что в избытке кислотного оксида, соответствующего многоосновной кислоте, возможна дальнейшая реакция с образованием кислой соли:
4. При сплавлении нелетучие оксиды способны вытеснять более летучие кислотные оксиды из их солей:
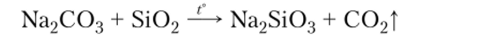
5. Некоторые кислотные оксиды при нагревании взаимодействуют с простыми веществами — восстановителями:
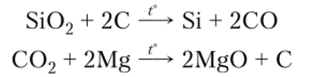
6. Отдельные кислотные оксиды разлагаются при нагревании:
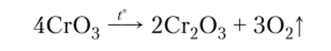
Рассмотрим химические свойства основных оксидов.
1. Оксиды щелочных и щелочноземельных металлов взаимодействуют с водой с образованием растворимых оснований (щелочей):

2. Основные оксиды реагируют с кислотными и амфотерными оксидами с образованием солей: 
3. Все основные оксиды реагируют с кислотами с образованием солей и воды: 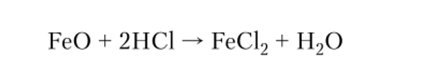
4. Основные оксиды взаимодействуют с кислыми солями с образованием средних солей и воды: 
5. Под действием различных восстановителей основные оксиды способны восстанавливаться до металлов:

6. Оксиды металлов, стоящих в ряду активности после меди, при нагревании разлагаются па металл и кислород:
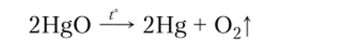
Рассмотрим химические свойства амфотерных оксидов.
1. Амфотерные оксиды реагируют с кислотными и основными оксидами с образованием солей:
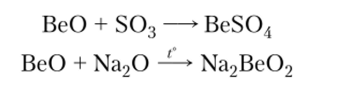
2. Амфотерные оксиды взаимодействуют с кислотами с образованием солей и воды. В этих реакциях они проявляют свойства основных оксидов:
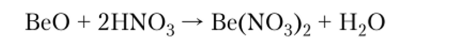
3. При сплавлении амфотерных оксидов с твердыми щелочами они проявляют свойства кислотных оксидов и образуют соответствующие соли и воду: 
При взаимодействии с водными растворами щелочей образуются комплексные соли:
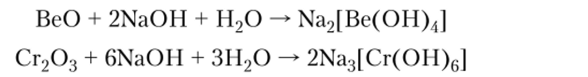
4. Под действием различных восстановителей амфотерные оксиды способны восстанавливаться до металла:
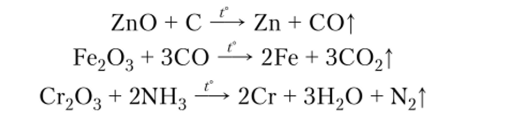
5. При сплавлении с солями амфотерные оксиды вытесняют летучие кислотные оксиды из солей: