Актиноиды.
Получение строение атомов

Остальные актиноиды — от нептуния (№ 93) до лоуренсия (№ 103) — были получены искусственным путем посредством ядерных реакций в период с 1940 по 1961 гг. усилиями различных групп исследователей, в основном в США, а также в СССР. Основной способ синтеза трансурановых элементов — бомбардировка ядер тяжелых элементов нейтронами или ядрами легких элементов, за которой следует соответствующая цепочка… Читать ещё >
Актиноиды. Получение строение атомов (реферат, курсовая, диплом, контрольная)
Актиноиды — ближайшие аналоги лантаноидов, однако различия между этими семействами элементов весьма значительны, они затрагивают не только электроные оболочки, но и ядра атомов. Все изотопы актиноидов радиоактивны. В связи с этим они сразу же после открытия явления радиоактивности (см. разд. 3.1) привлекли к себе устойчивый интерес не только химиков, но и физиков, занимающихся проблемами превращения массы в энергию. Интенсивное изучение этих элементов привело за короткое время к получению огромного фактического материала по их весьма сложному химическому поведению, несмотря на то, что многие из них удалось получить лишь в количестве нескольких миллиграммов или даже нескольких атомов. Были также сделаны важнейшие теоретические обобщения в области ядерной физики, послужившие основой для создания ядерно го оружия и ядерной энергетики — наиболее важных и, к сожалению, наиболее опасных достижений человечества в середине XX в. Огромное практическое значение актиноидов как ядерного взрывчатого вещества и ядерного горючего дополнительно стимулировало их исследования и, в частности, привело к созданию специальных методов работы с практически невесомыми количествами высокорадиоактивных веществ.
К наиболее долгоживущим изотопам актиноидов принадлежат некоторые изотопы тория и урана; в частности, период полураспада 232Th составляет 1,4 • Ю10, а 238 0 — 4,5 • 109 лет. Эти элементы не успели полностью распасться за время существования Земли и встречаются в природе в значительных количествах в основном в виде оксидов Th02, U308, UOj или солей Th (IV) и U (V[). В минералах, содержащих торий и уран, естественно, встречаются и продукты их распадаактиний и протактиний.
Остальные актиноиды — от нептуния (№ 93) до лоуренсия (№ 103) — были получены искусственным путем посредством ядерных реакций в период с 1940 по 1961 гг. усилиями различных групп исследователей, в основном в США, а также в СССР. Основной способ синтеза трансурановых[1] элементов — бомбардировка ядер тяжелых элементов нейтронами или ядрами легких элементов, за которой следует соответствующая цепочка распада получаемых радиоактивных ядер. Например, бомбардировка нейтронами 238U и получающегося плутония приводит к следующим превращениям:

Здесь над стрелкой указан вид ядерных превращений (пу — захват нейтрона, сопровождаемый испусканием 7-кванта; 0″ - 0-распад), а под стрелкой — период полураспада изотопа.
Подобным образом получают значительные количества (тонны) некоторых искусственных элементов. Отметим, что их практическое применение не ограничивается получением больших количеств энергии за счет реакции деления ядер. При радиоактивном а-распадс 238Ри выделяется относительно небольшая энергия, но поскольку его период полураспада составляет 90 лет, а ота-лучей очень легко защититься, то он представляет очень удобный стабильный и экологически чистый автономный источник энергии для автоматических устройств, работающих в космосе, на метеостанциях и даже вживляемых в человеческий организм.
Более тяжелые трансамсрициевые элементы получают, бомбардируя ядра плутония, америция, кюрия, урана и т. п. ядрами 4 Не (а-частицы),[1]}В,[1]JC. 14 N, 14 О.
Таблица 33.2. Характеристика актиноидов.
Элемент. | Электронная конфигурация атома. | Состояния окисления*. | Радиус иона м3 нм. | Стандартный потенциал. ^М3*/М* в | Плотность металла, г/см3 | ^пл металла,. °С. |
Ac (Rnl6/‘7s5 | 0,107. | — 2,6. | 10,1. | * 1 050. | ||
Th. | 6d7 Is* | (3), 4. | 0,105. | — 1,90. | 11.7. | 1 750. |
Ра. | 5p6dl Is7, sped7 Is7 | (3), 4, 5. | 0,103. | —. | ; | |
и. | sped1 Is7 | 3,4, 5,6. | 0,101. | — 1,78. | 19,0. | 1 134. |
Np. | Spls7, Sped1 Is7 | 3,4,5,6, (7). | 0,099. | — 1,82. | 20,4. | |
Pu. | Sp Is7 | 3,4, 5,6, 7. | 0,097. | — 2,03. | 19,8. | |
Am. | Sfls7 | 2.3. (4X5,6. (7). | 0,096. | — 2,31. | 13,7. | 1 180. |
Cm. | sped1 is7 | 2.4, (5), 6. | 0,095. | — 2,69. | 19,3. | 1 340. |
Bk. | Sped1 7s3, spls7 | 2.4. | 0,094. | — 2,40. | 14,8. | |
Cf. | sp°ls7 | 2.2.4. | 0,0%. | ; | 15,0. | |
Es. | SP’ls7 | 2.2. | 0,095. | —. | 8,8. | |
Fm. | Sp7ls7 | 2,2. | 0,094. | |||
Md. | SP’ls7 | 1,2.3. | 0,093. | |||
No. | SP4 Is7 | 2,2. | 0,093. | |||
Lr. | sp4edi is7, Sp4 Is7 Ip1 | 0,092. | ||||
? В скобках приведены малоустойчивые состояния, подчеркнуты наиболее распространенные. | ||||||
и даже «Ne. Так, сотый элемент — фермий — может быть получен по реакции 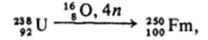 а самый тяжелый актиноид — лоуренсий — по реакции:
а самый тяжелый актиноид — лоуренсий — по реакции:
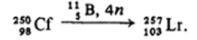
В принципе, подобными способами получают и более тяжелые элементы.
Наряду с радиоактивностью всех изотопов другим важным отличием актиноидов от лантаноидов является значительно большая способность 5/-электронов принимать участие в образовании ковалентных связей, способность, обусловленная большей радиальной протяженностью 5/юрбиталей по сравнению с 4/орбиталями.
Следствием энергетической близости 5/-, 6с/-, Is- и 7р-уровней, а также повышенной способности 5/-электронов к образованию химических связей является большое разнообразие состояний окисления у актиноидов и общее стремление их к реализации высоких состояний окисления (табл. 33.2). Из таблицы видно, что по набору состояний окисления актиноиды имеют черты сходства и с /-элементами — число состояний окисления и высшее состояние (+7) проходят через максимум, и с лантаноидами — почти у всех актиноидов устойчиво состояние +3. Радиусы ионов М3* у актиноидов близки к радиусам соответствующих лантаноидов и также монотонно уменьшаются с ростом атомного номера.