Калифорний.
Фундаментальная радиохимия

Изотоп 252Cf оказался полезен для многих физических исследований. Хотя основной вид его распада — а-распад, интенсивность параллельного спонтанного деления достаточно велика (3,08%). Главное применение калифорния — изготовление источников нейтронов. Благодаря испусканию мощного потока нейтронов 2,2Cf применяют в нейтронно-активационном анализе, в нейтронной радиографии, в геологоразведке и при… Читать ещё >
Калифорний. Фундаментальная радиохимия (реферат, курсовая, диплом, контрольная)
Калифорний (californium) Cf, Z = 98, атомная масса 251,0796. Синтезирован в 1950 г. на циклотроне С. Томпсоном, А. Гиорсо, К. Стритом и Г. Сиборгом по ядерной реакции 242Сm (d, я)245Cf. Назван в честь Калифорнийского университета в Беркли (США), где и был получен.
Известно 19 радиоактивных изотопов калифорния: самый легкий 2;, 7Cf (Г½ = 2,1 с), самый тяжелый 256Cf (Г½ = 12,3 м), имеет один ядерный изомер. Наиболее устойчив изотоп 25lCf (а-распад в 247Сш, Г½ = 898 л). Относительно устойчивы и могут быть получены в макроколичествах при длительном облучении урана или плутония нейтронами: 249Cf (а-распад в 245Ст, Г, 2 = 352 л; вероятность самопроизвольного деления (СД) — 5, i ? 10 7%), 250Cf (а-расиад в 246Ст, Г, 2 = 13,08 л; вероятность СД — 0,079%) и 252Cf (а-распад в 248Ст, Т½ = 2,645 л; вероятность СД — 3,08%). 24fiCf, 248Cf, 249Cf — СД. Средняя энергия a-излучения 244Cf, 246Cf, 248Cf, 249Cf, 250Cf, 25lCf, 252Cf, 253Cf, 254Cf равна соответственно 7,32; 6,86; 6,36; 5,92; 6,12; 5,88; 6,02; 1,88−10 2; 1,84−10 2 МэВ). 252Cf подвергается спонтанному тройному делению с образованием трех осколков: |0Ве, 96Sr и 146Ва. При спонтанном делении ядер 252Cf образуются нейтроны; 1 г 252Cf испускает 3 • 1012 нейтронов в 1 с.
252Cf обладает малой критической массой. Число вторичных нейтронов при спонтанном делении у него велико: на акт деления приходится 3,82 нейтрона, но относительно маленький период полураспада 2,>2Cf (Г½ = 2,6 л), интенсивное нейтронное излучение, высокая тепловая мощность делают его малопригодным для оружейного использования.
Изотопы калифорния получают при длительном (3 года) облучении урана, плутония, америция или кюрия в ядерных реакторах е высокой плотностью потока нейтронов. Изотопы калифорния также могут быть получены в ходе термоядерной реакции. В настоящее время 252Cf получают в ядерных реакторах при длительном облучении 239Ри. Полный выход изотопа составляет 3−10 3, т. е. из 1 кг 239Ри можно получить 3 г 252Cf. Выделение изотопа из смеси трапсплутониевых элементов осуществляют ионообменным или хроматографическим методом либо электрофорезом и экстракцией.
Калифорний — металл серебристо-белого цвета, мощный источник нейтронов. Радиус атома 0,295 нм, электронная конфигурация | Rn ]5/'°7.v2, электроотрцательность по Полингу 1,3, электродный потенциал Cf — Cf3+ -1,93, Cf <�— Cf2+ -2,1 В, степени окисления +2, +3 п +4, плотность 15,1 г/см3, Тпл = = 900 °C, Ткпп = 1227 °C, молярная теплоемкость 29 ДжДК-моль). Существует в двух полиморфных модификациях. Ниже 600 °C устойчива a-модификация с гексагональной решеткой (параметры а = 0,339 нм, с = 1,101 нм), выше 600 °C — р-модификация с ГЦК решеткой.
Калифорний получают восстановлением фторида калифорния CfF3 литием:

или оксида калифорния Cf203 кальцием:
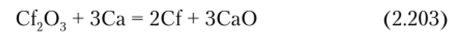
По химическим свойствам калифорний подобен лантанидам. Единственным стабильным состоянием калифорния является трехвалентное. Синтезированы галогениды калифорния — СШа13, оксигалогениды — CfOHal. Для получения диоксида калифорния СЮ2 оксид Cf203 окисляют при нагревании кислородом под давлением 10 МПа. В растворах Cf (IV) получают, действуя на соединения Cf (III) сильными окислителями. Синтезирован твердый дииодид калифорния Cfl2. Из водных растворов Cf (III) восстанавливается до Cf (II) электрохимически. Калифорний образует соединения с кислородом (Cf203, Cf203jt, Cf02), серой (Cf2S3), галогенами: галогениды (CfF3, CfCl3, CfBr3, Cfl3, CfF4), оксигалогениды (CfOF, CfOCl, CfOBr). Получены металлоорганические соединения — Cf (C5H5)3 и комплексные соединения со многими минеральными и органическими кислотами.
В растворе ионы Cf (III) в зависимости от pH и наличия лигандов могут быть гидратированы или находиться в комплексе с другими соединениями. В очень кислых растворах, в среде НСЮ4 и в отсутствие комплексообразователей ионы элемента гидратированы. С ростом pH раствора степень гидролиза ионов калифорния, как и других трапсплутониевых элементов, возрастает. В щелочной среде большая часть их гидролизована.
Идентификация и количественное определение наиболее удобного для химических исследований изотопа 249Cf с удельной активностью 9,05* 103 расп/(мин-мкг) проводится после его выделения в радиохимически чистом состоянии на а-спектрометре по энергии наиболее интенсивной группы а-частиц, равной 5,806 МэВ. Кроме того, у-излучение, сопровождающее а-распад, также может быть использовано для его определения. Для изучения химических свойств этого элемента часто используется смесь тяжелых изотопов калифорния с массовыми числами от 250 до 252, получающаяся при длительном облучении плутония нейтронами. Радиометрическое определение калифорния в этом случае можно проводить по 2;, 2Cf, который обладает наибольшей скоростью спонтанного деления. Для быстрого определения 252Cf в присутствии других актинидов и осколков деления без разрушения образца используется метод, основанный на измерении мгновенного у-излучения большой энергии (>2,8 МэВ) при спонтанном делении. 252,254Cf можно определять измерением числа нейтронов спонтанного деления в счетчике, наполненном BF3, после их предварительного замедления в полиэтилене или парафине. Более точным и чувствительным методом определения 252Cf с удельной активностью 1,2 10° расиДмин мкг) является измерение интенсивности его a-излучения на а-спектрометре. В этом случае необходимо полное отделение калифорния от всех других а-излучателей.
Изотоп 252Cf оказался полезен для многих физических исследований. Хотя основной вид его распада — а-распад, интенсивность параллельного спонтанного деления достаточно велика (3,08%). Главное применение калифорния — изготовление источников нейтронов. Благодаря испусканию мощного потока нейтронов [2,3 -1012 н/(с*г)] 2,2Cf применяют в нейтронно-активационном анализе, в нейтронной радиографии, в геологоразведке и при добыче полезных ископаемых, в сталелитейной, химической, нефтеперерабатывающей, угледобывающей промышленности, в ядерной энергетике и авиационно-космической технике. Апробирован метод контактной терапии злокачественных опухолей с использованием источников 252Cf. Применяется для производства компонентов ядерного оружия (ядерные и термоядерные заряды малой мощности).
Радионуклид 252Cf высокотоксичен. ПДК в воде открытых водоемов 1,33−10-4 Бк/л.
Снижение удержания радионуклида в легких человека описывается суммой двух экспонент: 17% радионуклида выводится с Гэфф, равным 25 дней, 83% — 1210 дней (через 7 дней после инъекции). Биологический эффект обусловливается ионизирующим излучением, образующимся при ядерных превращениях изотопов калифорния. Ядерные превращения 252Cf сопровождаются образованием осколков с высокой энергией, испусканием а-частиц, нейтронов, у-излучения спонтанного деления, а также у-, p-излучения образующихся осколочных элементов.
При поступлении 252Cf в организм человека дозовую нагрузку в тканях создают a-излучение и высокоэнергетические осколки деления. В тех ситуациях, когда 252Cf является источником внешнего облучения, поглощенная доза обусловлена нейтронами, у-излучением спонтанного деления, а при небольших расстояниях от источника (несколько сантиметров) и р-излучением.
Высокая проникающая способность у-нейтронного излучения 252Cf — основной радиационный фактор при работе с закрытыми источниками радионуклида. При этом вклад нейтронной компоненты в суммарный биологический эффект является самым важным. Вклад у-компоненты возрастает с увеличением размеров объекта. Эффективность у-нейтронного излучения 252Cf в отличие от чистого у-излучения мало зависит от мощности дозы. По подавлению репродуктивной способности опухолевых и нормальных клеток разных культур доза у-нейтронного излучения, приводящая к выживанию 37% клеток в диапазоне мощности дозы 0,0015—2,8 Гр/ч, практически одинакова и составляет 1,0 Гр.
Относительная биологическая эффективность у-нейтронного излучения 252Cf увеличивается с уменьшением суммарной поглощенной дозы, что объясняется слабой степенью восстановления повреждений тканей от нейтронного воздействия.
Для 249.250.251.252,253.254Cf Группа раДИаЦИОННОЙ ОПаСНОСТИ А, М3 А = 3,7 • 103 Бк.
Для количественного определения изотопов калифорния необходимо получение их в чистом виде, что требует отделения от сопутствующих лантанидов и актинидов. Учитывая небольшие весовые количества изотопов калифорния, основными методами анализа являются спектрометрические.